名校
1 . N-Zn/TiO2光催化氧化可用于工业上含硫废液的处理,光生电子(e-)与水电离出的H+、O2作用生成过羟基自由基(HO2·),空穴(h+)与水电离出的OH-作用生成羟基自由基(·OH),HO2·和·OH分别与 反应生成
反应生成 ,变化过程如下图所示。下列说法错误的是
,变化过程如下图所示。下列说法错误的是
 反应生成
反应生成 ,变化过程如下图所示。下列说法错误的是
,变化过程如下图所示。下列说法错误的是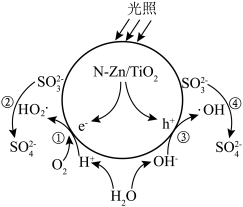
A.·OH氧化 的反应为 的反应为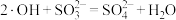 |
B.①②过程和③④过程产生的 之比为1:1 之比为1:1 |
| C.pH过低或过高均会影响催化剂的催化效果 |
D.氧化含硫废液的总反应为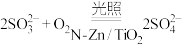 |
您最近半年使用:0次
2024-04-21更新
|
135次组卷
|
2卷引用:东北三省四市2024届高三教研联合体高考模拟(一)化学试卷
名校
解题方法
2 .  是一种广谱型的消毒剂,根据世界环保联盟的要求,
是一种广谱型的消毒剂,根据世界环保联盟的要求, 将逐渐取代
将逐渐取代 成为生产自来水的消毒剂。工业上
成为生产自来水的消毒剂。工业上 常用
常用 和
和 溶液混合并加
溶液混合并加 酸化后反应制得,在以上反应中氧化剂与还原剂的个数之比为
酸化后反应制得,在以上反应中氧化剂与还原剂的个数之比为
 是一种广谱型的消毒剂,根据世界环保联盟的要求,
是一种广谱型的消毒剂,根据世界环保联盟的要求, 将逐渐取代
将逐渐取代 成为生产自来水的消毒剂。工业上
成为生产自来水的消毒剂。工业上 常用
常用 和
和 溶液混合并加
溶液混合并加 酸化后反应制得,在以上反应中氧化剂与还原剂的个数之比为
酸化后反应制得,在以上反应中氧化剂与还原剂的个数之比为A. | B. | C. | D. |
您最近半年使用:0次
2023-11-05更新
|
83次组卷
|
2卷引用:黑龙江省克东县“五校联谊”2023-2024学年高一上学期期中考试化学试题
3 . 由实验操作和现象,可得出相应正确结论的是
| 实验操作 | 现象 | 结论 | |
| A | 向某钠盐粉末上滴加浓盐酸,将产生的气体通入品红溶液 | 品红溶液褪色 | 该钠盐只能为 、 、 或 或 |
| B | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的 悬浊液 悬浊液 | 无砖红色沉淀 | 蔗糖未发生水解 |
| C | 铝粉与氧化铁发生铝热反应,冷却后将固体溶于盐酸,向所得溶液滴加 溶液 溶液 | 溶液颜色无明显变化 | 氧化铁已经完全被铝粉还原 |
| D | 石蜡油加强热,将产生的气体通入 的 的 溶液 溶液 | 溶液由橙红色变为无色 | 气体中含不饱和烃 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
4 . 下列有关物质的性质与用途不具有对应关系的是
| A.碳化硅硬度大,可用于制作砂轮磨料 |
| B.Na2SO3有还原性,可用于水处理中脱氯 |
| C.NH4HCO3受热易分解,可用作氮肥 |
| D.硫酸钡不溶于水和酸,且不容易被X射线透过,医疗上可用作消化系统X射线检测的内服药剂 |
您最近半年使用:0次
2023-10-08更新
|
120次组卷
|
2卷引用:黑龙江省齐齐哈尔普高联谊校2023-2024学年高三上学期11月期中考试化学试题
解题方法
5 . 磷酸亚铁锂(LiFePO4)能可逆地嵌入、脱出锂,使其作为锂离子电池的正极材料的研究及应用得到广泛关注。通过水热法制备磷酸亚铁锂的一种方法如下(装置如图所示):
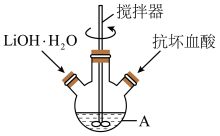
Ⅰ.在A中加入40 mL蒸馏水、0.015 mol H3PO4和0.01 mol FeSO4·7H2O,用搅拌器搅拌溶解后,缓慢加入0.015mol LiOH·H2O,继续搅拌。
Ⅱ.向反应液中加入少量抗坏血酸(即维生素C),继续搅拌5 min。
Ⅲ.快速将反应液装入反应釜中,保持170℃恒温5 h。
Ⅳ.冷却至室温,过滤。
Ⅴ.用蒸馏水洗涤沉淀。
Ⅵ.干燥,得到磷酸亚铁锂产品。
回答下列问题
(1)装置图中仪器A的名称是_______ 。
(2)根据上述实验药品的用量,仪器A的最适宜规格为_______(填标号)。
(3)步骤Ⅱ中,抗坏血酸的作用是_______ 。也可以用Na2SO3代替抗坏血酸,其原理是_______ (用离子方程式表示)。
(4)步骤Ⅴ检验LiFePO4是否洗涤干净的方法是_______
(5)干燥后称量,产品的质量是1.2 g,本实验的产率为_______ %(保留1位小数)。

Ⅰ.在A中加入40 mL蒸馏水、0.015 mol H3PO4和0.01 mol FeSO4·7H2O,用搅拌器搅拌溶解后,缓慢加入0.015mol LiOH·H2O,继续搅拌。
Ⅱ.向反应液中加入少量抗坏血酸(即维生素C),继续搅拌5 min。
Ⅲ.快速将反应液装入反应釜中,保持170℃恒温5 h。
Ⅳ.冷却至室温,过滤。
Ⅴ.用蒸馏水洗涤沉淀。
Ⅵ.干燥,得到磷酸亚铁锂产品。
回答下列问题
(1)装置图中仪器A的名称是
(2)根据上述实验药品的用量,仪器A的最适宜规格为_______(填标号)。
| A.100 mL | B.250 mL | C.500 mL | D.1000 mL |
(3)步骤Ⅱ中,抗坏血酸的作用是
(4)步骤Ⅴ检验LiFePO4是否洗涤干净的方法是
(5)干燥后称量,产品的质量是1.2 g,本实验的产率为
您最近半年使用:0次
2023-09-20更新
|
76次组卷
|
2卷引用:黑龙江省哈尔滨市德强高级中学2023-2024学年高三上学期期中考试化学试题
6 . 下列说法与盐类的水解有关的有几项
①氯化铵与氯化锌溶液可作焊接金属过程中的除锈剂
②用 晶体配制溶液时,先将其溶于较浓的盐酸中
晶体配制溶液时,先将其溶于较浓的盐酸中
③保存硫酸亚铁溶液时需加入少量铁粉
④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤判断氯化铵和硫化钠等盐溶液的酸碱性
⑥草木灰与铵态氮肥不能混合施用
⑦ 溶液蒸干后得到
溶液蒸干后得到 固体
固体
①氯化铵与氯化锌溶液可作焊接金属过程中的除锈剂
②用
 晶体配制溶液时,先将其溶于较浓的盐酸中
晶体配制溶液时,先将其溶于较浓的盐酸中③保存硫酸亚铁溶液时需加入少量铁粉
④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤判断氯化铵和硫化钠等盐溶液的酸碱性
⑥草木灰与铵态氮肥不能混合施用
⑦
 溶液蒸干后得到
溶液蒸干后得到 固体
固体| A.4项 | B.5项 | C.6项 | D.7项 |
您最近半年使用:0次
名校
7 . 回答下列问题:
(1)写出下列实验事实与所给酸对应的性质(填序号)
A.酸性 B.挥发性 C.吸水性 D.脱水性 E.不稳定性 F.氧化性
①浓硝酸使紫色石蕊试液先变红后褪色___________
②浓硫酸可作氯气的干燥剂___________
③浓硫酸加到蔗糖中,蔗糖变黑___________
(2)“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物。下列化学反应符合“绿色化学”理念的是___________
①制 :
: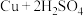 (浓)
(浓)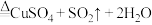
②制 ;
;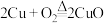 ;
; (稀)
(稀)
③制 :
: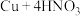 (浓)
(浓)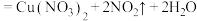
④制 :
: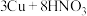 (稀)
(稀)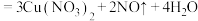
(3)某同学向 溶液中通入
溶液中通入 ,未观察到白色沉淀生成,由此可知酸性强弱:
,未观察到白色沉淀生成,由此可知酸性强弱:
___________ HCl(填“>”或“<”)。取上述所得溶液进行下列操作,能观察到白色沉淀生成的___________ (填字母)。
A.通入 B.滴加
B.滴加 溶液 C.滴加稀盐酸 D.滴加NaOH溶液
溶液 C.滴加稀盐酸 D.滴加NaOH溶液
(4) 中有+4价的硫,它既有氧化性又有还原性,现有试剂:溴水、
中有+4价的硫,它既有氧化性又有还原性,现有试剂:溴水、 溶液、
溶液、 、NaOH溶液、氨水。
、NaOH溶液、氨水。
①要证明 具有还原性,应选用的试剂是
具有还原性,应选用的试剂是___________ ,看到的现象是___________ 。
②选用 与
与 反应,反应的现象是
反应,反应的现象是___________ ,反应的离子方程式为___________ 。
(1)写出下列实验事实与所给酸对应的性质(填序号)
A.酸性 B.挥发性 C.吸水性 D.脱水性 E.不稳定性 F.氧化性
①浓硝酸使紫色石蕊试液先变红后褪色
②浓硫酸可作氯气的干燥剂
③浓硫酸加到蔗糖中,蔗糖变黑
(2)“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物。下列化学反应符合“绿色化学”理念的是
①制
 :
: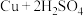 (浓)
(浓)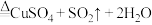
②制
 ;
;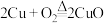 ;
; (稀)
(稀)
③制
 :
: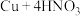 (浓)
(浓)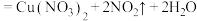
④制
 :
: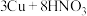 (稀)
(稀)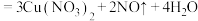
(3)某同学向
 溶液中通入
溶液中通入 ,未观察到白色沉淀生成,由此可知酸性强弱:
,未观察到白色沉淀生成,由此可知酸性强弱:
A.通入
 B.滴加
B.滴加 溶液 C.滴加稀盐酸 D.滴加NaOH溶液
溶液 C.滴加稀盐酸 D.滴加NaOH溶液(4)
 中有+4价的硫,它既有氧化性又有还原性,现有试剂:溴水、
中有+4价的硫,它既有氧化性又有还原性,现有试剂:溴水、 溶液、
溶液、 、NaOH溶液、氨水。
、NaOH溶液、氨水。①要证明
 具有还原性,应选用的试剂是
具有还原性,应选用的试剂是②选用
 与
与 反应,反应的现象是
反应,反应的现象是
您最近半年使用:0次
名校
解题方法
8 . 依据下列各项实验操作和现象,分析并推出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向 溶液中滴加少量KSCN溶液 溶液中滴加少量KSCN溶液 | 溶液出现浅红色 | 配制 溶液时应加入少量铁粉 溶液时应加入少量铁粉 |
| B | ①向某溶液中加入 溶液 溶液②再加足量盐酸 | ①产生白色沉淀 ②仍有白色沉淀 | 原溶液中有 |
| C | 将足量 通入 通入 溶液中,逸出的气体先通过酸性 溶液中,逸出的气体先通过酸性 溶液,再通入澄清石灰水中 溶液,再通入澄清石灰水中 | 澄清石灰水变浑浊 | 酸性: |
| D | 向蔗糖固体中加入适量浓硫酸,并充分搅拌 | 出现疏松多孔的黑色固体,并闻到刺激性气味 | 浓硫酸只表现脱水性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
9 . 下列指定反应的离子方程式正确的是
A.用 溶液吸收少量 溶液吸收少量 : : |
B. 通入足量的NaClO溶液中: 通入足量的NaClO溶液中: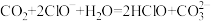 |
C. 溶液中加过量 溶液中加过量 溶液: 溶液: |
D. 溶液中加过量 溶液中加过量 溶液: 溶液: |
您最近半年使用:0次
2023-05-16更新
|
379次组卷
|
2卷引用:黑龙江省双鸭山市第一中学2023-2024学年高三上学期开学考试化学试题
10 . 下列由实验现象所得结论错误的是
A.向 溶液中通入 溶液中通入 ,产生淡黄色沉淀,说明 ,产生淡黄色沉淀,说明 具有氧化性 具有氧化性 |
B.向酸性 溶液中加入 溶液中加入 粉末,紫色褪去,证明 粉末,紫色褪去,证明 中含Fe(Ⅱ) 中含Fe(Ⅱ) |
C.向浓硝酸中插入红热的木炭,可观察到有红棕色气体产生,证明木炭与浓硝酸反应生成 |
D.向某溶液中滴加盐酸放出能使品红溶液褪色的气体,证明该溶液中可能含有 |
您最近半年使用:0次
2023-03-18更新
|
202次组卷
|
2卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高一下学期4月月考化学试题



