2024高三下·全国·专题练习
解题方法
1 . 纯ClO2遇热易发生分解,工业上通常制成NaClO2固体以便运输和储存。制备NaClO2的实验装置如图所示(夹持装置省略),其中A装置制备ClO2,C装置用于制备NaClO2。回答下列问题:_______ 。
(2)装置A中发生反应的离子方程式为_______ 。向装置A中通入空气的目的是_______ 。
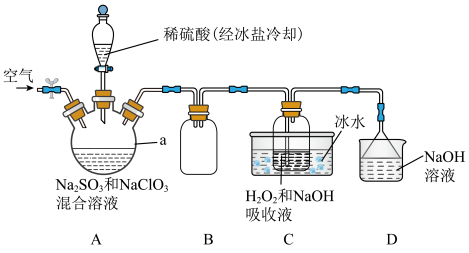
(2)装置A中发生反应的离子方程式为
您最近半年使用:0次
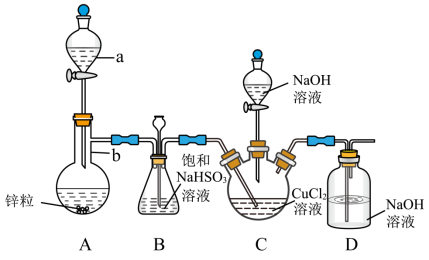
2 . CuCl是一种难溶于水和乙醇的白色固体,可溶于浓盐酸或者浓氨水(形成络合物),易被氧化为高价绿色铜盐,见光受热易分解。在催化领域广泛应用,纺织工业中常作脱色剂,可利用如图装置(夹持装置略去)将SO2通入新制氢氧化铜悬浊液中制备CuCl。
①向C中先加入10.00mL0.5mol•L-1CuCl2溶液,再加入30mL0.6mol•L-1NaOH溶液;
②取下A中分液漏斗上的玻璃塞,然后打开分液漏斗的活塞,产生SO2气体至过量,直至C中出现较多的白色沉淀,上层是淡绿色的溶液;
③将C中混合物过滤,依次用水和乙醇洗涤低温晾干,精确称量所得固体质量为0.398g。
回答下列问题:
(1)针对步骤2中的现象查阅资料得知:
i.白色沉淀为CuCl;
ii.上层淡绿色溶液中的主要溶质为NaCl和少量Cu(HSO3)2。
结论:本实验中较多量的新制氢氧化铜与二氧化硫发生了氧化还原反应,少量与之发生了复分解反应,二者为竞争关系。检验淡绿色溶液中含有 的操作方法是
的操作方法是_______ 。
①向C中先加入10.00mL0.5mol•L-1CuCl2溶液,再加入30mL0.6mol•L-1NaOH溶液;
②取下A中分液漏斗上的玻璃塞,然后打开分液漏斗的活塞,产生SO2气体至过量,直至C中出现较多的白色沉淀,上层是淡绿色的溶液;
③将C中混合物过滤,依次用水和乙醇洗涤低温晾干,精确称量所得固体质量为0.398g。
回答下列问题:
(1)针对步骤2中的现象查阅资料得知:
i.白色沉淀为CuCl;
ii.上层淡绿色溶液中的主要溶质为NaCl和少量Cu(HSO3)2。
结论:本实验中较多量的新制氢氧化铜与二氧化硫发生了氧化还原反应,少量与之发生了复分解反应,二者为竞争关系。检验淡绿色溶液中含有
 的操作方法是
的操作方法是
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
3 . 钒酸钇(YVO4)广泛应用于光纤通信领域,一种用废钒催化剂(含 V2O5、K2O、SiO2少量Fe2O3制取YVO4的工艺流程如下:
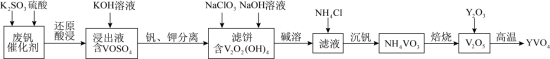
已知:V2O2(OH)4既能与强酸反应,又能与强碱反应。 回答下列问题:
(1)“还原酸浸”时,钒以VO2+浸出,“浸出液”中还含有的金属离子是___________ 。V2O5被还原的离子方程式为___________ 。
(2)结合“碱溶”和“沉钒”可知,ClO 、VO
、VO 氧化性更强的是
氧化性更强的是___________ ,“沉钒”时发生反应的化学方程式为___________ 。
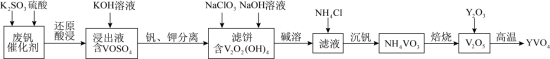
已知:V2O2(OH)4既能与强酸反应,又能与强碱反应。 回答下列问题:
(1)“还原酸浸”时,钒以VO2+浸出,“浸出液”中还含有的金属离子是
(2)结合“碱溶”和“沉钒”可知,ClO
 、VO
、VO 氧化性更强的是
氧化性更强的是
您最近半年使用:0次
4 . “价—类”二维图是研究物质性质的一种方法,图中a~f表示的均是含硫物质。下列说法正确的是

| A.a可用硫化亚铁与稀硝酸反应制取 |
B.可发生反应: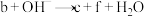 (未配平) (未配平) |
| C.c能使溴水褪色,证明c有漂白性 |
| D.f既有氧化性又有还原性 |
您最近半年使用:0次
2024-02-14更新
|
576次组卷
|
4卷引用:河北省承德市2023-2024学年高一上学期期末考试化学试题
河北省承德市2023-2024学年高一上学期期末考试化学试题(已下线)专题01 硫及其化合物(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)河北省石家庄市第二十三中学2023-2024学年高一下学期第一次月考(3月)化学试题安徽省淮南市第二中2023-2024学年高一下学期第一次月考化学试题
23-24高一上·江苏盐城·期末
5 . 物质类别与元素价态是学习元素及其化合物性质的重要认识视角。下图是硫元素的“价类二维图”,下列说法不正确 的是


| A.a和c反应可以生成b | B.d能使品红溶液褪色 |
| C.酸性:e>g | D.h暴露空气中可转化为f |
您最近半年使用:0次
2023高三·全国·专题练习
6 .  是一种压电材料。以
是一种压电材料。以 为原料,采用下列路线可制备粉状
为原料,采用下列路线可制备粉状 。
。
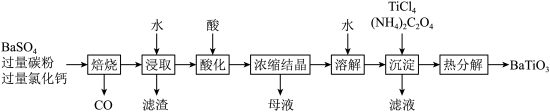
回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是___________ 。
(2)“焙烧”后固体产物有 、易溶于水的
、易溶于水的 和微溶于水的
和微溶于水的 。“浸取”时主要反应的离子方程式为
。“浸取”时主要反应的离子方程式为___________ 。
(3)“酸化”步骤应选用的酸是___________ (填标号)。
a.稀硫酸 b.浓硫酸 c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行?___________ ,其原因是___________ 。
(5)“沉淀”步骤中生成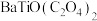 的化学方程式为
的化学方程式为___________ 。
 是一种压电材料。以
是一种压电材料。以 为原料,采用下列路线可制备粉状
为原料,采用下列路线可制备粉状 。
。
回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是
(2)“焙烧”后固体产物有
 、易溶于水的
、易溶于水的 和微溶于水的
和微溶于水的 。“浸取”时主要反应的离子方程式为
。“浸取”时主要反应的离子方程式为(3)“酸化”步骤应选用的酸是
a.稀硫酸 b.浓硫酸 c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行?
(5)“沉淀”步骤中生成
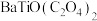 的化学方程式为
的化学方程式为
您最近半年使用:0次
名校
7 . 下列溶液中,能大量共存的离子组是
A.含有 的溶液中: 的溶液中: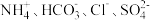 |
B.加入足量 的溶液中: 的溶液中: |
C.在透明的溶液中: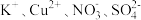 |
D.强碱性溶液中: |
您最近半年使用:0次
2024-01-07更新
|
165次组卷
|
3卷引用:江西省南昌市第十九中学2023-2024学年高一下学期3月月考化学试题
江西省南昌市第十九中学2023-2024学年高一下学期3月月考化学试题(已下线)期中测试卷一【测试范围:第五、六章】-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)重庆市第一中学校2023-2024学年高一上学期期中(半期)考试化学试卷
解题方法
8 . 下列关于氢硫酸、亚硫酸、硫酸的叙述正确的是
| A.它们都是酸,因此彼此不发生反应 |
| B.只有亚硫酸可以露置在空气中,其他酸不可以 |
| C.鉴别三种酸溶液时,只要分别滴加BaCl2溶液即可 |
| D.它们都是二元酸,酸性:H2S<H2SO3<H2SO4 |
您最近半年使用:0次
解题方法
9 . 如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题。
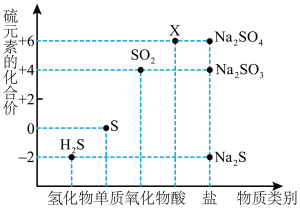
(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的_______ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有___________ (填化学式)。
(3)将H2S与SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为___________ 。
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目____________ 。
____Na2S+____Na2SO3+___H2SO4=____Na2SO4+____S↓+____H2O
(5)下列关于硫及其化合物的叙述正确的是
(6)设NA为阿伏加德罗常数的值。下列说法正确的是

(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有
(3)将H2S与SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目
____Na2S+____Na2SO3+___H2SO4=____Na2SO4+____S↓+____H2O
(5)下列关于硫及其化合物的叙述正确的是
| A.试管内壁残留的硫可用酒精洗涤 | B.SO2的水溶液长期放置,酸性会增强 |
| C.SO2有毒,不可以做食品添加剂 | D.浓硫酸在空气中敞口放置,质量会减小 |
(6)设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1 mol铁单质与足量的硫单质充分反应,转移电子的数目为3NA |
| B.常温下,22.4 L SO2与足量的O2反应,生成的SO3分子数为NA |
| C.常温下,将5.6 g铁片投入足量的浓硫酸中,铁失去的电子数为0.3NA |
| D.1 mol Na2O2与足量H2O反应,转移的电子数为NA |
您最近半年使用:0次
10 . 化学实验小组在实验室中利用某化工厂排出的废渣[主要成分为BaCO3、Ba(FeO2)2、BaSO3]制备Ba(NO3)2晶体的流程如图所示。
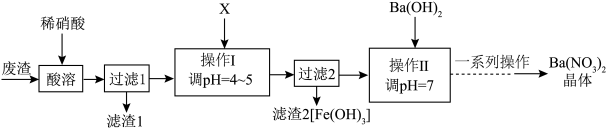
已知:Ba(NO3)2的溶解度受温度影响较大。下列说法错误的是

已知:Ba(NO3)2的溶解度受温度影响较大。下列说法错误的是
| A.酸溶时,Ba(FeO2)2、BaSO3都能与稀硝酸发生氧化还原反应 |
| B.滤渣1的主要成分是BaSO4 |
| C.试剂X可选择BaCO3 |
| D.流程中“一系列操作”有蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
您最近半年使用:0次



