名校
解题方法
1 . 实验小组探究 与
与 的反应。向盛有
的反应。向盛有 的烧瓶中加入
的烧瓶中加入 固体,测得反应体系中
固体,测得反应体系中 含量的变化如图。
含量的变化如图。

下列说法不正确 的是
 与
与 的反应。向盛有
的反应。向盛有 的烧瓶中加入
的烧瓶中加入 固体,测得反应体系中
固体,测得反应体系中 含量的变化如图。
含量的变化如图。
下列说法
A.有 生成推测发生了反应: 生成推测发生了反应: |
B.bc段 含量下降与反应 含量下降与反应 有关 有关 |
C.可用 酸化的 酸化的 溶液检验b点固体中是否含有 溶液检验b点固体中是否含有 |
D.产物 也可能是 也可能是 与 与 直接化合生成的 直接化合生成的 |
您最近半年使用:0次
2 . 某学生对 与
与 不同的
不同的 下反应进行探究。
下反应进行探究。
(1)调节pH,实验记录如下:
查阅资料得知:
i. :白色,难溶于水,溶于过量
:白色,难溶于水,溶于过量 溶液;
溶液;
ii. :棕黑色,不溶于水,能和酸反应。
:棕黑色,不溶于水,能和酸反应。
①推测a中白色沉淀为 ,离子方程式是
,离子方程式是___________ 。
②推测a中白色沉淀为 ,推测的依据是
,推测的依据是___________ 。
(2)取 中白色沉淀,置于过量
中白色沉淀,置于过量 溶液中,沉淀溶解。该同学设计实验确认了白色沉淀不是
溶液中,沉淀溶解。该同学设计实验确认了白色沉淀不是 ,实验方法是:另取
,实验方法是:另取 固体置于
固体置于___________ 溶液中,未溶解。
(3)将c中 滤出、洗净,为确认其组成,实验如下:
滤出、洗净,为确认其组成,实验如下:
Ⅰ.向 中滴加稀盐酸,无明显变化;
中滴加稀盐酸,无明显变化;
Ⅱ.向 中加入过量浓
中加入过量浓 产生红棕色气体;
产生红棕色气体;
Ⅲ.用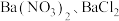 检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀。
检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀。
①实验I的目的是___________
②根据上述现象,分析X的性质和元素组成是___________
③Ⅱ中反应的化学方程式是___________ 。
(4)该同学综合以上实验,分析X产生的原因,认为随着酸性的增强,体系还原性增强。通过进一步实验确认了这种可能性,实验如下:
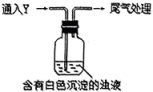
①气体Y是___________ 。
②白色沉淀转化为X的化学方程式是___________ 。
 与
与 不同的
不同的 下反应进行探究。
下反应进行探究。(1)调节pH,实验记录如下:
| 实验 |  | 现象 |
| a | 10 | 产生白色沉淀,稍后溶解,溶液澄清 |
| b | 6 | 产生白色沉淀,一段时间后,沉淀未溶解 |
| c | 2 | 产生大量白色沉淀,一段时间后,产生海绵状棕黑色物质 |
i.
 :白色,难溶于水,溶于过量
:白色,难溶于水,溶于过量 溶液;
溶液;ii.
 :棕黑色,不溶于水,能和酸反应。
:棕黑色,不溶于水,能和酸反应。①推测a中白色沉淀为
 ,离子方程式是
,离子方程式是②推测a中白色沉淀为
 ,推测的依据是
,推测的依据是(2)取
 中白色沉淀,置于过量
中白色沉淀,置于过量 溶液中,沉淀溶解。该同学设计实验确认了白色沉淀不是
溶液中,沉淀溶解。该同学设计实验确认了白色沉淀不是 ,实验方法是:另取
,实验方法是:另取 固体置于
固体置于(3)将c中
 滤出、洗净,为确认其组成,实验如下:
滤出、洗净,为确认其组成,实验如下:Ⅰ.向
 中滴加稀盐酸,无明显变化;
中滴加稀盐酸,无明显变化;Ⅱ.向
 中加入过量浓
中加入过量浓 产生红棕色气体;
产生红棕色气体;Ⅲ.用
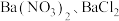 检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀。
检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀。①实验I的目的是
②根据上述现象,分析X的性质和元素组成是
③Ⅱ中反应的化学方程式是
(4)该同学综合以上实验,分析X产生的原因,认为随着酸性的增强,体系还原性增强。通过进一步实验确认了这种可能性,实验如下:

①气体Y是
②白色沉淀转化为X的化学方程式是
您最近半年使用:0次
名校
3 . 书写下列反应的离子 方程式:
(1)以NaIO3为原料制备I2的方法是:先向NaIO3溶液中加入计量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2.上述制备I2的总反应___________ 。
(2)在酸性条件下,黄铁矿(FeS2,其中S为-1价)催化氧化的反应转化如图所示。
总反应:2FeS2+7O2+2H2O=2Fe2++4 +4H+
+4H+
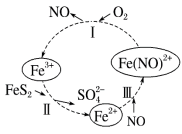
①反应I:___________ 。
②反应II:___________ 。
(3)红磷充分燃烧的产物与足量热的NaOH溶液反应,该反应的离子方程式是___________ 。
(4)取FeSO4溶液,调pH约为7,加入淀粉KI溶液和H2O2,溶液呈褐色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是___________ 。
(5)NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图所示:
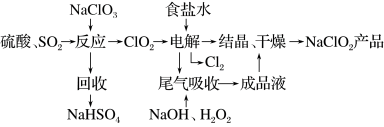
①写出“反应”步骤中生成ClO2的化学方程式:___________ 。
② “电解”过程阴极主反应的方程式:___________ 。
③“尾气吸收”是吸收“电解”过程排出的少量ClO2,写出此吸收反应的离子方程式:___________ 。
(1)以NaIO3为原料制备I2的方法是:先向NaIO3溶液中加入计量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2.上述制备I2的总反应
(2)在酸性条件下,黄铁矿(FeS2,其中S为-1价)催化氧化的反应转化如图所示。
总反应:2FeS2+7O2+2H2O=2Fe2++4
 +4H+
+4H+
①反应I:
②反应II:
(3)红磷充分燃烧的产物与足量热的NaOH溶液反应,该反应的离子方程式是
(4)取FeSO4溶液,调pH约为7,加入淀粉KI溶液和H2O2,溶液呈褐色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是
(5)NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图所示:

①写出“反应”步骤中生成ClO2的化学方程式:
② “电解”过程阴极主反应的方程式:
③“尾气吸收”是吸收“电解”过程排出的少量ClO2,写出此吸收反应的离子方程式:
您最近半年使用:0次
4 . 下列物质的水溶液蒸干后充分灼烧,最终能得到该溶质固体的是
A. | B. | C. | D. |
您最近半年使用:0次
名校
5 . “以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如下:

(1)为加快工业废碱渣中Na2CO3的溶解,可采取的措施是___________ (写出一种即可)。
(2)将碳酸钠溶液吸收烟气中的SO2的化学方程式补充完整:___________ 。
SO2+Na2CO3+______=NaHSO3+CO2
(3)上述流程中,加入NaOH后,发生反应的化学方程式为___________ 。
(4)亚硫酸钠(Na2SO3)中硫的化合价是___________ 。亚硫酸钠粗品中常含有少量的硫酸钠,可能的原因是___________ 。

(1)为加快工业废碱渣中Na2CO3的溶解,可采取的措施是
(2)将碳酸钠溶液吸收烟气中的SO2的化学方程式补充完整:
SO2+Na2CO3+______=NaHSO3+CO2
(3)上述流程中,加入NaOH后,发生反应的化学方程式为
(4)亚硫酸钠(Na2SO3)中硫的化合价是
您最近半年使用:0次
6 . 某小组探究不同阴离子与 的结合倾向并分析相关转化。
的结合倾向并分析相关转化。
资料:ⅰ. 和
和 均为白色,难溶于水。
均为白色,难溶于水。
ⅱ. 与
与 、
、 能生成
能生成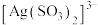 、
、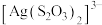 。
。
ⅲ.与 结合倾向
结合倾向 。
。
(1)探究 、
、 与
与 的结合倾向
的结合倾向
①由实验Ⅰ推测:与 结合倾向
结合倾向
______  (填“>”或“<”)。
(填“>”或“<”)。
②取两等份 浊液,分别滴加等浓度、等体积的
浊液,分别滴加等浓度、等体积的 和
和 溶液,前者无明显现象,后者浊液变澄清,澄清溶液中
溶液,前者无明显现象,后者浊液变澄清,澄清溶液中 价银的主要存在形式
价银的主要存在形式_______ (填化学式)。推测:与 结合倾向
结合倾向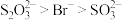 。查阅资料证实了上述推测。
。查阅资料证实了上述推测。
(2) 的转化
的转化
①写出实验Ⅲ中白色沉淀消失的离子方程式___________ 。
②查阅资料:实验Ⅳ中黑色沉淀是 ,
, 中S元素的化合价分别为
中S元素的化合价分别为 和
和 。写出实验Ⅳ中白色沉淀变为黑色的化学方程式:
。写出实验Ⅳ中白色沉淀变为黑色的化学方程式:___________ 。
③ 溶液可用作定影液。向
溶液可用作定影液。向 溶液溶解
溶液溶解 之后的废定影液中,加入
之后的废定影液中,加入___________ (填试剂和操作),可重新得到 。
。
(3) 的转化
的转化

分析试管1出现银镜的原因___________ 。
(4)资料显示: 与
与 结构相似,
结构相似, 可看作
可看作 外围的一个O被S替换的结果。但与
外围的一个O被S替换的结果。但与 的配位倾向:
的配位倾向: ,试从结构角度解释原因
,试从结构角度解释原因___________ 。
 的结合倾向并分析相关转化。
的结合倾向并分析相关转化。资料:ⅰ.
 和
和 均为白色,难溶于水。
均为白色,难溶于水。ⅱ.
 与
与 、
、 能生成
能生成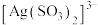 、
、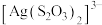 。
。ⅲ.与
 结合倾向
结合倾向 。
。(1)探究
 、
、 与
与 的结合倾向
的结合倾向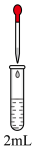 | 实验 | 滴管 | 试管 | 现象 |
| Ⅰ | 10滴 溶液 溶液 | 等浓度的 和 和 溶液 溶液 | 黄色沉淀 | |
| Ⅱ | 等浓度的 和 和 溶液 溶液 | 黄色沉淀 |
 结合倾向
结合倾向
 (填“>”或“<”)。
(填“>”或“<”)。②取两等份
 浊液,分别滴加等浓度、等体积的
浊液,分别滴加等浓度、等体积的 和
和 溶液,前者无明显现象,后者浊液变澄清,澄清溶液中
溶液,前者无明显现象,后者浊液变澄清,澄清溶液中 价银的主要存在形式
价银的主要存在形式 结合倾向
结合倾向 。查阅资料证实了上述推测。
。查阅资料证实了上述推测。(2)
 的转化
的转化 | 实验 | 滴管 | 试管 | 现象 |
| Ⅲ |  溶液 溶液 | 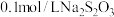 溶液 溶液 | 白色沉淀,振荡后消失 | |
| Ⅳ | 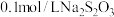 溶液 溶液 |  溶液 溶液 | 白色沉淀,逐渐变为灰色,最终为黑色沉淀 |
②查阅资料:实验Ⅳ中黑色沉淀是
 ,
, 中S元素的化合价分别为
中S元素的化合价分别为 和
和 。写出实验Ⅳ中白色沉淀变为黑色的化学方程式:
。写出实验Ⅳ中白色沉淀变为黑色的化学方程式:③
 溶液可用作定影液。向
溶液可用作定影液。向 溶液溶解
溶液溶解 之后的废定影液中,加入
之后的废定影液中,加入 。
。(3)
 的转化
的转化
分析试管1出现银镜的原因
(4)资料显示:
 与
与 结构相似,
结构相似, 可看作
可看作 外围的一个O被S替换的结果。但与
外围的一个O被S替换的结果。但与 的配位倾向:
的配位倾向: ,试从结构角度解释原因
,试从结构角度解释原因
您最近半年使用:0次
名校
解题方法
7 . 下列方程式能准确解释相应事实的是
A.硫酸型酸雨的形成: |
B.84消毒液不能与洁厕灵混用: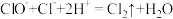 |
C.和面时在小苏打中加少量醋酸,增强效果: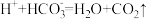 |
D.向 溶液中加入足量 溶液中加入足量 溶液,得到白色沉淀: 溶液,得到白色沉淀: |
您最近半年使用:0次
名校
解题方法
8 . 化学是一门以实验为基础的学科,某同学为探究 溶液的性质进行如下实验,操作如图所示。查阅资料可知:
溶液的性质进行如下实验,操作如图所示。查阅资料可知:
① 可将
可将 氧化为S,
氧化为S, 也可以把
也可以把 氧化为
氧化为
②电解质可使胶体发生聚沉
③亚铁离子和硫离子在溶液中可生成 为黑色沉淀,该沉淀能溶于盐酸。
为黑色沉淀,该沉淀能溶于盐酸。
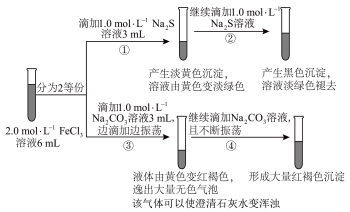
根据实验现象,下列分析正确的是
 溶液的性质进行如下实验,操作如图所示。查阅资料可知:
溶液的性质进行如下实验,操作如图所示。查阅资料可知:①
 可将
可将 氧化为S,
氧化为S, 也可以把
也可以把 氧化为
氧化为
②电解质可使胶体发生聚沉
③亚铁离子和硫离子在溶液中可生成
 为黑色沉淀,该沉淀能溶于盐酸。
为黑色沉淀,该沉淀能溶于盐酸。
根据实验现象,下列分析正确的是
| A.向②后试管加入足量稀盐酸,沉淀全部溶解 |
| B.根据反应现象分析,①~④的变化中,只有1处涉及氧化还原反应 |
C.若将 溶液滴加到 溶液滴加到 溶液中,产生的现象与图中①、②现象相同 溶液中,产生的现象与图中①、②现象相同 |
D.若将 溶液更换成 溶液更换成 溶液,可产生相同的现象 溶液,可产生相同的现象 |
您最近半年使用:0次
2023-11-25更新
|
230次组卷
|
2卷引用:北京市海淀区第二十中学2022-2023学年高一上学期11月月考化学试题
名校
解题方法
9 . 设计实验探究NO的氧化性。
实验Ⅰ:用排水法收集一瓶NO,将其倒扣在盛有碱性 溶液的水槽中,振荡,观察到集气瓶中液面上升。
溶液的水槽中,振荡,观察到集气瓶中液面上升。
资料:ⅰ.NO与碱性 溶液会发生氧化还原反应,
溶液会发生氧化还原反应, 被还原为
被还原为 。
。
ⅱ. 与
与 反应生成黄色沉淀。
反应生成黄色沉淀。
某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验Ⅱ:取饱和 溶液,加入少量冰醋酸,再滴加5滴
溶液,加入少量冰醋酸,再滴加5滴 的
的 溶液,无明显变化。
溶液,无明显变化。
实验Ⅲ:
(1)取少量实验Ⅰ反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴 的
的 溶液,
溶液,___________ (填实验现象)。
上述实验证明NO有氧化性。
(2)实验Ⅱ的目的是___________
(3)写出NO与碱性 溶液反应的离子方程式
溶液反应的离子方程式___________
(4)一个氧化还原反应可以看成“氧化”和“还原”两个半反应,试用此角度分析NO与碱性 溶液的反应。若还原反应为:
溶液的反应。若还原反应为: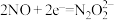 ,则氧化反应为:
,则氧化反应为:___________ 。
(5)某同学结合所学知识设计处理工业废气中 和NO的实验方案,达到消除污染,保护环境的目的。
和NO的实验方案,达到消除污染,保护环境的目的。
①先用饱和纯碱溶液吸收废气中的 ,生成
,生成 ,写出该反应的离子方程式
,写出该反应的离子方程式___________
②再向生成的溶液中加入一定量___________ ,以此溶液来吸收NO气体。
实验Ⅰ:用排水法收集一瓶NO,将其倒扣在盛有碱性
 溶液的水槽中,振荡,观察到集气瓶中液面上升。
溶液的水槽中,振荡,观察到集气瓶中液面上升。资料:ⅰ.NO与碱性
 溶液会发生氧化还原反应,
溶液会发生氧化还原反应, 被还原为
被还原为 。
。ⅱ.
 与
与 反应生成黄色沉淀。
反应生成黄色沉淀。某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验Ⅱ:取饱和
 溶液,加入少量冰醋酸,再滴加5滴
溶液,加入少量冰醋酸,再滴加5滴 的
的 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ:
(1)取少量实验Ⅰ反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴
 的
的 溶液,
溶液,上述实验证明NO有氧化性。
(2)实验Ⅱ的目的是
(3)写出NO与碱性
 溶液反应的离子方程式
溶液反应的离子方程式(4)一个氧化还原反应可以看成“氧化”和“还原”两个半反应,试用此角度分析NO与碱性
 溶液的反应。若还原反应为:
溶液的反应。若还原反应为: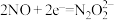 ,则氧化反应为:
,则氧化反应为:(5)某同学结合所学知识设计处理工业废气中
 和NO的实验方案,达到消除污染,保护环境的目的。
和NO的实验方案,达到消除污染,保护环境的目的。①先用饱和纯碱溶液吸收废气中的
 ,生成
,生成 ,写出该反应的离子方程式
,写出该反应的离子方程式②再向生成的溶液中加入一定量
您最近半年使用:0次
名校
解题方法
10 . 某同学从物质类别、元素价态的角度,预测 和
和 部分化学性质。
部分化学性质。
(1)从物质类别角度, 属于酸性氧化物,预测
属于酸性氧化物,预测 可以和强碱反应,将少量
可以和强碱反应,将少量 通入NaOH溶液中,反应的离子方程式为
通入NaOH溶液中,反应的离子方程式为___________ 。
(2)从硫元素的价态角度分析, 既有氧化性又有还原性,
既有氧化性又有还原性,___________ 。
①将 通入酸性
通入酸性 溶液中,溶液紫色褪去,生成
溶液中,溶液紫色褪去,生成 。反应结束后,硫元素存在形式应该是
。反应结束后,硫元素存在形式应该是___________ 。
A. B.S C.
B.S C. D.
D.
② 还能和
还能和 反应,生成硫单质和水,反应的化学方程式为
反应,生成硫单质和水,反应的化学方程式为___________ 。
(3)查阅资料后发现, 的部分化学性质与
的部分化学性质与 类似。该同学向
类似。该同学向 溶液中加入稀硝酸,预测能产生一种刺激性气味的气体,该气体是
溶液中加入稀硝酸,预测能产生一种刺激性气味的气体,该气体是___________ 。但在实验过程中,他并没有检测到该气体生成,可能的原因是___________ 。
 和
和 部分化学性质。
部分化学性质。(1)从物质类别角度,
 属于酸性氧化物,预测
属于酸性氧化物,预测 可以和强碱反应,将少量
可以和强碱反应,将少量 通入NaOH溶液中,反应的离子方程式为
通入NaOH溶液中,反应的离子方程式为(2)从硫元素的价态角度分析,
 既有氧化性又有还原性,
既有氧化性又有还原性,①将
 通入酸性
通入酸性 溶液中,溶液紫色褪去,生成
溶液中,溶液紫色褪去,生成 。反应结束后,硫元素存在形式应该是
。反应结束后,硫元素存在形式应该是A.
 B.S C.
B.S C. D.
D.
②
 还能和
还能和 反应,生成硫单质和水,反应的化学方程式为
反应,生成硫单质和水,反应的化学方程式为(3)查阅资料后发现,
 的部分化学性质与
的部分化学性质与 类似。该同学向
类似。该同学向 溶液中加入稀硝酸,预测能产生一种刺激性气味的气体,该气体是
溶液中加入稀硝酸,预测能产生一种刺激性气味的气体,该气体是
您最近半年使用:0次



