名校
解题方法
1 . 下列有关实验操作、现象和结论都正确的是
| 实验操作 | 现象 | 解释或结论 | |
| A. | 向某无色溶液中通入过量的CO2气体 | 产生白色沉淀 | 该溶液中可能含有 |
| B | Cu与浓硫酸反应,冷却后,再将冷水缓慢加入盛有反应混合物的试管中 | 溶液变蓝 | 证明反应生成了Cu2+ |
| C | 向亚硫酸钠溶液中依次滴加稀盐酸和硝酸钡溶液 | 产生白色沉淀 | 亚硫酸钠溶液已变质 |
| D. | 某铁的氧化物样品用足量浓盐酸溶解后,再滴入少量酸性高锰酸钾 | 紫红色褪去 | 铁的氧化物中含+2价铁 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
2 . 氯、硫元素的价类二维图如图所示。下列说法正确的是
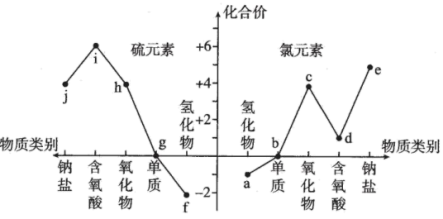

| A.i与j能发生氧化还原反应 |
| B.d、h的水溶液在空气中久置,溶液酸性均减弱 |
| C.Fe分别与b、g反应,产物中铁元素的化合价相同 |
D.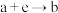 反应的离子方程式为 反应的离子方程式为 |
您最近半年使用:0次
3 . 过碳酸钠 外观为白色晶体,是无毒漂白剂和供氧剂,还有去污杀菌作用,工业常用
外观为白色晶体,是无毒漂白剂和供氧剂,还有去污杀菌作用,工业常用 和双氧水化合制备:
和双氧水化合制备: ,下列说法不正确的是
,下列说法不正确的是
 外观为白色晶体,是无毒漂白剂和供氧剂,还有去污杀菌作用,工业常用
外观为白色晶体,是无毒漂白剂和供氧剂,还有去污杀菌作用,工业常用 和双氧水化合制备:
和双氧水化合制备: ,下列说法不正确的是
,下列说法不正确的是| A.过碳酸钠具有强氧化性 |
| B.生产过程中采用较低温度,目的是防止产品及反应物的分解 |
| C.过碳酸钠和过氧化钠漂白原理相同 |
D.将过碳酸钠溶液和亚硫酸氢钠溶液混合,发生反应: |
您最近半年使用:0次
2023-10-11更新
|
172次组卷
|
2卷引用:湖北省武汉市第三中学2023-2024学年高一上学期10月月考化学试题
名校
4 . 已知还原性: >I->Fe2+>Br-。某溶液中可能含有
>I->Fe2+>Br-。某溶液中可能含有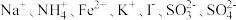 ,且所有离子个数相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是(已知溴水、碘水有色)
,且所有离子个数相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是(已知溴水、碘水有色)
 >I->Fe2+>Br-。某溶液中可能含有
>I->Fe2+>Br-。某溶液中可能含有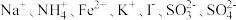 ,且所有离子个数相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是(已知溴水、碘水有色)
,且所有离子个数相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是(已知溴水、碘水有色)A.肯定不含 | B.肯定不含 | C.可能含有 | D.肯定含有 |
您最近半年使用:0次
名校
解题方法
5 . CoCl2可用于电镀,是一种性能优越的电池前驱材料,由含钴矿(Co 元素主要以Co2O3、 CoO 的形式存在,还含有Fe、Si、Cu、Zn、Mn、Ni、Mg、Ca 元素,碳及有机物等)制取氯化钴晶体的一种工艺流程如图:

已知:①焦亚硫酸钠(Na2S2O5)常作食品抗氧化剂。CaF2、MgF2 难溶于水。
②CoCl2∙6H2O 的熔点为 86℃,易溶于水、乙醚等;常温下稳定无毒,加热至 110~120℃时, 失去结晶水变成有毒的无水氯化钴。
③部分金属阳离子形成氢氧化物的 pH 见表:
回答下列问题:
(1)“550℃焙烧”的目的是_______ 。
(2)“浸取”的过程中,用离子方程式表示 Na2S2O5的主要作用是_______ 。
(3)滤液 1 中加入 NaClO3溶液的作用是_______ 。
(4)加入Na2CO3 溶液生成滤渣 2 的主要离子方程式为_______ 。
滤液 3 经过多次萃取与反萃取制备CoCl2 晶体:
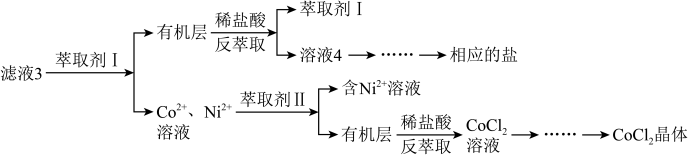
(5)滤液 3 中加入萃取剂 I,然后用稀盐酸反萃取的目的是_______ 。
(6)制备晶体CoCl2∙6H2O,需在减压环境下烘干的原因是_______ 。
(7)测定产品的纯度:称取 CoCl2∙6H2O 样品,将其用适当试剂转化为 CoC2O4,再转化为(NH4)2C2O4溶液,稀硫酸酸化后用高锰酸钾标准溶液滴定,滴定终点的判定_______ 。

已知:①焦亚硫酸钠(Na2S2O5)常作食品抗氧化剂。CaF2、MgF2 难溶于水。
②CoCl2∙6H2O 的熔点为 86℃,易溶于水、乙醚等;常温下稳定无毒,加热至 110~120℃时, 失去结晶水变成有毒的无水氯化钴。
③部分金属阳离子形成氢氧化物的 pH 见表:
| Co3+ | Fe3+ | Cu2+ | Co2+ | Fe2+ | Zn2+ | Mn2+ | Mg2+ | |
| 开始沉淀 pH | 0.3 | 2.7 | 5.5 | 7.2 | 7.6 | 7.6 | 8.3 | 9.6 |
| 完全沉淀 pH | 1.1 | 3.2 | 6.6 | 9.2 | 9.6 | 9.2 | 9.3 | 11.1 |
(1)“550℃焙烧”的目的是
(2)“浸取”的过程中,用离子方程式表示 Na2S2O5的主要作用是
(3)滤液 1 中加入 NaClO3溶液的作用是
(4)加入Na2CO3 溶液生成滤渣 2 的主要离子方程式为
滤液 3 经过多次萃取与反萃取制备CoCl2 晶体:

(5)滤液 3 中加入萃取剂 I,然后用稀盐酸反萃取的目的是
(6)制备晶体CoCl2∙6H2O,需在减压环境下烘干的原因是
(7)测定产品的纯度:称取 CoCl2∙6H2O 样品,将其用适当试剂转化为 CoC2O4,再转化为(NH4)2C2O4溶液,稀硫酸酸化后用高锰酸钾标准溶液滴定,滴定终点的判定
您最近半年使用:0次
名校
解题方法
6 . 氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。工业以硫化铜精矿为原料,设计符合绿色化学理念的制备CuCl的流程如图:

已知:CuCl难溶于水和乙醇,潮湿时易水解氧化。
下列说法正确的是

已知:CuCl难溶于水和乙醇,潮湿时易水解氧化。
下列说法正确的是
| A.步骤①焙烧产生的有毒气体,可以使紫色石蕊溶液先变红后褪色,体现了漂白性 |
| B.步骤②中可以用硝酸代替硫酸,不影响后续处理 |
C.步骤③离子方程式: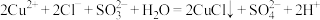 |
| D.步骤④用的乙醇洗涤,也可以使用蒸馏水洗涤 |
您最近半年使用:0次
2023-06-29更新
|
137次组卷
|
2卷引用:湖北省咸宁市2022-2023学年高一下学期期末考试化学试题
名校
7 . 用下图装置进行实验,对应实验现象正确的是
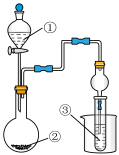

| 选项 | ① | ② | ③ | ③中实验现象 |
| A | 稀硫酸 | FeS固体 | CuSO4溶液 | 黑色沉淀 |
| B | 稀硫酸 | Na2SO3 | BaCl2溶液 | 出现浑浊 |
| C | 稀氨水 | 石灰石 | 酚酞溶液 | 出现红色 |
| D | 稀盐酸 | MnO2 | 品红溶液 | 溶液褪色 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
8 . 下列离子方程式正确的是
A.两种含氯物质发生化合反应: |
B.两种盐恰好发生氧化还原反应: |
C.证明氧化性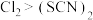 的反应: 的反应: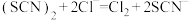 |
D.在足量烧碱溶液中氯元素发生歧化反应: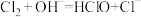 |
您最近半年使用:0次
2023-04-27更新
|
253次组卷
|
2卷引用:湖北省十堰市2023届高三下学期调研考试化学试题
解题方法
9 . 二氧化硫既能污染环境,又在生活、生产中有着广泛的作用,根据要求回答问题。
Ⅰ.如图所示是酸雨的形成示意图,根据图示回答下列问题。

(1)某实验小组采集硫酸型酸雨样品,随着时间的变化多次测定该样品的 ,得到表中数据:酸雨样品放置时
,得到表中数据:酸雨样品放置时 变化的主要原因是
变化的主要原因是_______ (用化学方程式表示)。
(2)你认为减少酸雨的产生可采取的措施是_______(填字母)。
①减少用煤作燃料 ②开发新能源 ③燃料脱硫 ④在已酸化的土壤中洒石灰
⑤监测并治理汽车排出的大量尾气 ⑥收集大气中氮氧化物制硝酸
Ⅱ.他们设计如下实验装置研究二氧化硫的性质,请你参与探究。

(3)实验开始前需进行的操作是_______ ,装置①试管中发生反应的化学方程式为_______ 。
(4)装置②用于检验 的漂白性,其中所盛试剂为
的漂白性,其中所盛试剂为_______ 。
(5)能说明二氧化硫具有氧化性的实验现象为_______ 。
(6)装置⑤中氨水的作用是_______ ,装置⑤中倒置漏斗的作用是_______ 。
Ⅰ.如图所示是酸雨的形成示意图,根据图示回答下列问题。

(1)某实验小组采集硫酸型酸雨样品,随着时间的变化多次测定该样品的
 ,得到表中数据:酸雨样品放置时
,得到表中数据:酸雨样品放置时 变化的主要原因是
变化的主要原因是| 测定时间/h | 0 | 1 | 2 | 3 | 4 |
雨水的 | 4.75 | 4.60 | 4.58 | 4.50 | 4.50 |
①减少用煤作燃料 ②开发新能源 ③燃料脱硫 ④在已酸化的土壤中洒石灰
⑤监测并治理汽车排出的大量尾气 ⑥收集大气中氮氧化物制硝酸
| A.①②③④⑤⑥ | B.②③⑤⑥ | C.①②③⑤ | D.①②③④⑤ |
Ⅱ.他们设计如下实验装置研究二氧化硫的性质,请你参与探究。

(3)实验开始前需进行的操作是
(4)装置②用于检验
 的漂白性,其中所盛试剂为
的漂白性,其中所盛试剂为(5)能说明二氧化硫具有氧化性的实验现象为
(6)装置⑤中氨水的作用是
您最近半年使用:0次
名校
解题方法
10 . 下列各离子组在给定条件下能大量共存的是
A.使pH试纸显蓝色的溶液中: 、 、 、 、 、 、 |
B.0.1mo/L 溶液中: 溶液中: 、 、 、 、 、 、 |
C.滴加KSCN显红色的溶液中: 、 、 、 、 、 、 |
D.能与铝反应放出 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次



