1 . Fe3S4固体是一种重要的磁性材料,以它为原料实现如下化合物的转化: 的形式存在,溶液呈亮黄色。
的形式存在,溶液呈亮黄色。
请回答:
(1)依据B→C→D的现象,判断Cl-、SCN-、CN-与Fe3+的配位能力由强到弱依次为___________ ,无色酸性溶液F中的含硫阴离子有___________ 。
(2)Fe3S4能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标准状况下的密度为1.518g∙L-1),写出该反应的离子方程式___________ 。
(3)下列说法正确的是___________。
(4)写出F→G反应的化学方程式___________ 。请设计实验方案确定溶液G中的阴离子___________ 。

 的形式存在,溶液呈亮黄色。
的形式存在,溶液呈亮黄色。请回答:
(1)依据B→C→D的现象,判断Cl-、SCN-、CN-与Fe3+的配位能力由强到弱依次为
(2)Fe3S4能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标准状况下的密度为1.518g∙L-1),写出该反应的离子方程式
(3)下列说法正确的是___________。
| A.固体A中可能含有FeO | B.无色气体E能完全溶于水 |
| C.溶液C呈酸性,是由于Fe3+水解 | D.溶液B可溶解铜 |
(4)写出F→G反应的化学方程式
您最近半年使用:0次
解题方法
2 . 化合物X是一种蓝黑色(有时是粉红色)的固体,是一种由趋磁细菌制造的生物矿。某研究小组按如下流程探究该固体的组成:

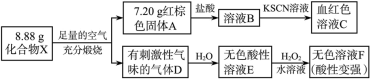
请回答:
(1)X的化学式为___________ 。
(2)请写出E反应生成F的化学方程式:___________ 。
(3)化合物X(只含两种元素)与盐酸反应,反应后得到浅绿色溶液,同时生成一种浅黄色不溶物和一种臭鸡蛋气味气体,请写出该反应的离子方程式:___________ 。


请回答:
(1)X的化学式为
(2)请写出E反应生成F的化学方程式:
(3)化合物X(只含两种元素)与盐酸反应,反应后得到浅绿色溶液,同时生成一种浅黄色不溶物和一种臭鸡蛋气味气体,请写出该反应的离子方程式:
您最近半年使用:0次
名校
3 . 下列实验有关离子检验的操作及现象与结论之间对应关系正确的是
实验操作及现象 | 结论 | |
| A | 向某溶液中加入 溶液,有白色沉淀生成,再加稀盐酸,沉淀不消失 溶液,有白色沉淀生成,再加稀盐酸,沉淀不消失 | 该溶液中含 |
| B | 向某溶液中加入过量盐酸,产生能使澄清石灰水变浑浊的气体 | 该溶液中含 |
| C | 向某溶液中加入酸性 溶液,溶液紫红色褪去 溶液,溶液紫红色褪去 | 该溶液中含有 |
| D | 用洁净的铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色 | 该溶液中含有 不确定是否有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
4 . 下列除杂试剂或方法正确的是
| 选项 | 被提纯物质 | 杂质 | 除杂试剂或方法 |
| A |  溶液 溶液 |  | 加入过量 溶液并过滤、洗涤 溶液并过滤、洗涤再将沉淀溶于适量盐酸 |
| B | 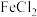 溶液 溶液 |  | 加入过量铜粉并过滤、洗涤 |
| C |  |  | 在空气中灼烧至质量不再变化 |
| D |  |  | 在空气中灼烧至质量不再变化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
5 . 下列反应的离子方程式不正确 的是
A. 溶液与足量澄清石灰水混合: 溶液与足量澄清石灰水混合: |
B. 溶液中加入过量 溶液中加入过量 溶液: 溶液: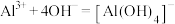 |
C.浓硝酸与铜的反应: |
D.少量的 通入亚硫酸钠溶液: 通入亚硫酸钠溶液: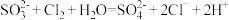 |
您最近半年使用:0次
6 . 某研究小组同学为探究锌与硫酸反应生成 、
、 的临界浓度(浓硫酸能与锌反应生成
的临界浓度(浓硫酸能与锌反应生成 的最低浓度)设计了如图实验(加热和夹持装置已省略)。
的最低浓度)设计了如图实验(加热和夹持装置已省略)。
已知:锌与浓硫酸开始时反应缓慢,可以适当加热以加速其反应,当有大量气泡生成时,该反应速率会明显加快并伴有大量的热放出。
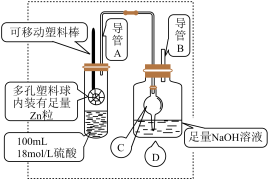
移动塑料棒,使锌浸没到硫酸中充分反应,反应结束后向D装置中加入足量的 溶液,再加入足量的
溶液,再加入足量的 溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a g。
溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a g。
(1)加入H₂O₂溶液发生反应的离子方程式是___________ 。
(2)浓硫酸与锌反应的临界浓度为___________ mol·L-1(用含a的计算式表示,忽略溶液体积变化)。
 、
、 的临界浓度(浓硫酸能与锌反应生成
的临界浓度(浓硫酸能与锌反应生成 的最低浓度)设计了如图实验(加热和夹持装置已省略)。
的最低浓度)设计了如图实验(加热和夹持装置已省略)。已知:锌与浓硫酸开始时反应缓慢,可以适当加热以加速其反应,当有大量气泡生成时,该反应速率会明显加快并伴有大量的热放出。

移动塑料棒,使锌浸没到硫酸中充分反应,反应结束后向D装置中加入足量的
 溶液,再加入足量的
溶液,再加入足量的 溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a g。
溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a g。(1)加入H₂O₂溶液发生反应的离子方程式是
(2)浓硫酸与锌反应的临界浓度为
您最近半年使用:0次
7 . 下列说法正确的是
A.蒸发 溶液可获得较为纯净的 溶液可获得较为纯净的 晶体 晶体 |
| B.阴离子交换膜法电解饱和食盐水可制备较纯净的烧碱 |
C.酸式滴定管内的油污可用热的饱和 溶液洗去 溶液洗去 |
| D.用NaOH溶液滴定未知浓度的醋酸,可用酚酞做指示剂 |
您最近半年使用:0次
8 . 某研究小组探究白色难溶盐X(含五种元素,M<200 g•mol-1)的组成,进行如图实验:
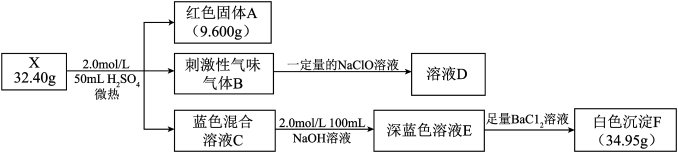
已知:固体A为常见单质:气体B能使品红褪色,实验测得气体体积为3.36L(标准状况),为防止污染环境,实验过程中用NaClO溶液吸收;溶液E中含有两种溶质,且阴离子相同。
请回答下列问题:
(1)X除含有H、O元素,还含有_________ 元素。
(2)混合溶液C中的溶质主要有_________ (填化学式)。
(3)可用气体B通入深蓝色溶液E制备X,写出相应的离子方程式________ 。
(4)设计实验方案证明吸收气体B的NaClO溶液已过量:_________ 。

已知:固体A为常见单质:气体B能使品红褪色,实验测得气体体积为3.36L(标准状况),为防止污染环境,实验过程中用NaClO溶液吸收;溶液E中含有两种溶质,且阴离子相同。
请回答下列问题:
(1)X除含有H、O元素,还含有
(2)混合溶液C中的溶质主要有
(3)可用气体B通入深蓝色溶液E制备X,写出相应的离子方程式
(4)设计实验方案证明吸收气体B的NaClO溶液已过量:
您最近半年使用:0次
解题方法
9 . 下列反应离子方程式不正确 的是
A.过量CO2通入NaOH 溶液:CO2+OH−=HCO |
| B.向血红色Fe(SCN)3溶液加入过量铁粉:2Fe3++Fe=3Fe2+ |
| C.苯酚的悬浊液中滴加氢氧化钠溶液:C6H5OH+OH-→C6H5O-+H2O |
D.Na2SO3溶液中滴入足量氯水:SO +H2O+Cl2=SO +H2O+Cl2=SO +2H++2Cl- +2H++2Cl- |
您最近半年使用:0次
解题方法
10 . 固体混合物X可能含有Na2SO3、K2CO3、Na2SO4、Fe2O3和Fe3O4中的几种。为确定其组成,做如下实验:
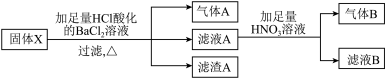
以下说法不正确 的是

以下说法
| A.气体A可能是混合物 | B.滤渣A一定为BaSO4 |
| C.固体X中一定含有Fe3O4 | D.无法确定X是否含有Na2SO4 |
您最近半年使用:0次




 ,
,


