名校
1 . 下列指定反应的离子方程式正确的是
A.用惰性电极电解CuCl2溶液: 2H2O + Cu2++ 2Cl- Cu(OH)2+ H2↑+ Cl2↑ Cu(OH)2+ H2↑+ Cl2↑ |
B.将少量氯气通入NaHSO3溶液中:HSO + H2O +Cl2=2Cl-+ 3H++SO + H2O +Cl2=2Cl-+ 3H++SO |
C.0.1mol/L AgNO3溶液中加入过量浓氨水:Ag+ + 2NH3·H2O =Ag(NH3)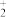 + 2H2O + 2H2O |
D.将NaHSO3溶液滴入Ba(NO3)2溶液产生白色沉淀:2HSO + Ba2+ =H2O+SO2↑+BaSO3↓ + Ba2+ =H2O+SO2↑+BaSO3↓ |
您最近半年使用:0次
名校
解题方法
2 . Ni、Co均是重要的战略性金属。从处理后的矿石硝酸浸取液(含Ni2+、Co2+、Al3+、Mg2+)中,利用氨浸工艺可提取Ni、Co,并获得高附加值化工产品。工艺流程如下:
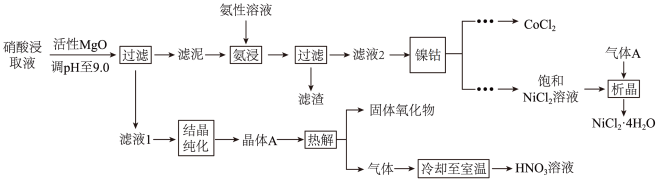
已知:氨性溶液由NH3·H2O、(NH4)2SO3和(NH4)2CO3配制。常温下,Ni2+、Co2+、Co3+与NH3形成可溶于水的配离子:lgKb(NH3·H2O)=-4.7;Co(OH)2易被空气氧化为Co(OH)3;部分氢氧化物的Ksp如下表。
回答下列问题:
(1)常温下,pH=9.9的氨性溶液中,c(NH3·H2O)_______ c( )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。
(2)“氨浸”时,由Co(OH)3转化为[Co(NH3)6]2+的离子方程式为_______ ,“滤渣”的成分是_______ 。
(3)(NH4)2CO3会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。(NH4)2CO3提高了Ni、Co的浸取速率,其原因是_______ 。
(4)“析晶”过程中通入的酸性气体A为_______ 。
(5)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得HNO3溶液中n(HNO3)与n(H2O)的比值,理论上最高为_______ 。
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用_______ 和_______ (填化学式)。

已知:氨性溶液由NH3·H2O、(NH4)2SO3和(NH4)2CO3配制。常温下,Ni2+、Co2+、Co3+与NH3形成可溶于水的配离子:lgKb(NH3·H2O)=-4.7;Co(OH)2易被空气氧化为Co(OH)3;部分氢氧化物的Ksp如下表。
| 氢氧化物 | Co(OH)2 | Co(OH)3 | Ni(OH)2 | Al(OH)3 | Mg(OH)2 |
| Ksp | 5.9×10-15 | 1.6×10-44 | 5.5×10-16 | 1.3×10-33 | 5.6×10-12 |
(1)常温下,pH=9.9的氨性溶液中,c(NH3·H2O)
 )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。(2)“氨浸”时,由Co(OH)3转化为[Co(NH3)6]2+的离子方程式为
(3)(NH4)2CO3会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。(NH4)2CO3提高了Ni、Co的浸取速率,其原因是
(4)“析晶”过程中通入的酸性气体A为
(5)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得HNO3溶液中n(HNO3)与n(H2O)的比值,理论上最高为
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用
您最近半年使用:0次
名校
解题方法
3 . 由海绵铜(主要含 和少量
和少量 )制取氯化亚铜
)制取氯化亚铜 的流程如下:
的流程如下:

已知:溶解过程中主要发生的反应: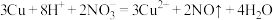
氯化亚铜微溶于水,不溶于稀酸,可溶于 浓度较大的体系,在潮湿空气中易被氧化。
浓度较大的体系,在潮湿空气中易被氧化。
下列关于说法正确的是
 和少量
和少量 )制取氯化亚铜
)制取氯化亚铜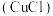 的流程如下:
的流程如下:
已知:溶解过程中主要发生的反应:
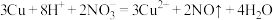
氯化亚铜微溶于水,不溶于稀酸,可溶于
 浓度较大的体系,在潮湿空气中易被氧化。
浓度较大的体系,在潮湿空气中易被氧化。下列关于说法正确的是
A.“溶解”时, 参与反应,生成 参与反应,生成 气体 气体 |
B.“还原”时,反应的离子方程式为: |
C.“过滤”时,可以搅拌加速滤液与 的分离 的分离 |
| D.“酸洗”时,最适宜选用的是稀盐酸 |
您最近半年使用:0次
名校
解题方法
4 . 在无色透明强酸性溶液中,能大量共存的离子组是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近半年使用:0次
5 . 类比推理是化学解题中常用的一种思维方法,下列有关类推正确的是
| 选项 | 已知 | 类推 |
| A | 用一束光照射淀粉溶液,可以看到一条光亮的“通路” | 用一束光照射硫酸钠溶液,也可以看到一条光亮的“通路” |
| B |  溶液在空气中不易变质 溶液在空气中不易变质 |  溶液在空气中也不易变质 溶液在空气中也不易变质 |
| C | 大理石与稀盐酸能快速产生 | 大理石与稀硫酸也能快速产生 |
| D | 不能用带橡胶塞的试剂瓶存放稀硫酸 |  溶液也不能用带橡胶塞的试剂瓶存放 溶液也不能用带橡胶塞的试剂瓶存放 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
6 . 下列过程涉及的离子方程式正确的是
| A.向BaCl2溶液中通入SO2气体:Ba2++SO2+H2O=BaSO3↓+2H+ |
| B.磁性氧化铁溶于稀硝酸溶液:Fe3O4+8H+=2Fe3++Fe2++4H2O |
C.同浓度同体积的NH4HSO4溶液与NaOH溶液混合: +OH-=NH3·H2O +OH-=NH3·H2O |
D.Na2S2O3溶液与稀硫酸混合:S2O +2H+=S↓+SO2↑+H2O +2H+=S↓+SO2↑+H2O |
您最近半年使用:0次
7 . 下列实验操作、现象和所得结论均正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 常温下将Al片放入浓硝酸中,无明显变化 | Al与浓硝酸不反应 |
| B | 将两根一样的Cu丝分别与浓硝酸和稀硝酸反应,浓硝酸反应更加剧烈 | 氧化性:浓硝酸>稀硝酸 |
| C | 加热NH4Cl固体,未能收集到能使湿润的红色石蕊试纸变蓝的气体 | NH4Cl未分解 |
| D | 向久置的Na2SO3溶液中加入足量BaCl2溶液,出现白色沉淀;再加入足量稀硝酸,部分沉淀溶解 | 部分Na2SO3被氧化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
8 . 下列表述正确的是
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中久置是否变质,可以先加硝酸酸化,再加氯化钡溶液
③锌与稀硝酸反应主要得到氢气
④足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸只能将铁氧化为Fe2+
⑤二氧化硫和二氧化氮都能形成酸雨,酸雨的pH等于5.6
⑥制玻璃的主要原料是纯碱、石灰石和石英砂
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中久置是否变质,可以先加硝酸酸化,再加氯化钡溶液
③锌与稀硝酸反应主要得到氢气
④足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸只能将铁氧化为Fe2+
⑤二氧化硫和二氧化氮都能形成酸雨,酸雨的pH等于5.6
⑥制玻璃的主要原料是纯碱、石灰石和石英砂
| A.①③④ | B.①②③ | C.①⑥ | D.①②⑥ |
您最近半年使用:0次
名校
解题方法
9 . 为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3溶液,再分别滴加下图所示的试剂:
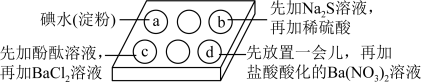
对实验现象的“解释或结论”错误的是

对实验现象的“解释或结论”错误的是
| 选项 | 实验现象 | 解释或结论 |
| A | a中溶液褪色 | 还原性: |
| B | b中加硫酸后产生淡黄色沉淀 |  和 和 在酸性条件下发生反应 在酸性条件下发生反应 |
| C | c中滴入酚酞溶液变红,再加BaCl2溶液后产生白色沉淀且红色褪去 | Na2SO3类似Na2CO3显碱性,所以滴入酚酞变红; 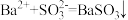 (白),Na2SO3反应完,红色褪去 (白),Na2SO3反应完,红色褪去 |
| D | d中产生白色沉淀 | Na2SO3溶液已变质 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
10 . 请根据硫元素的价类二维图,回答下列问题:___________ ,Z转化为X所加试剂为___________ (填“氧化剂”或“还原剂”)。
(2)W的浓溶液与铜反应的化学方程式___________ 。
(3)欲制备 ,从氧化还原角度分析,合理的是___________(填字母)。
,从氧化还原角度分析,合理的是___________(填字母)。
(4)Y转化为W可以选择下列试剂___________ 。
A.酸性 溶液B.
溶液B. 溶液C.
溶液C. 溶液D.X的水溶液
溶液D.X的水溶液
写出你所选试剂将Y转化为W的离子方程式___________ 。
(5)将X与Z、W的稀溶液混合,可生成淡黄色固体,则在该反应中还原产物与氧化产物的质量之比为___________ 。

(2)W的浓溶液与铜反应的化学方程式
(3)欲制备
 ,从氧化还原角度分析,合理的是___________(填字母)。
,从氧化还原角度分析,合理的是___________(填字母)。A. | B. | C. | D. |
A.酸性
 溶液B.
溶液B. 溶液C.
溶液C. 溶液D.X的水溶液
溶液D.X的水溶液写出你所选试剂将Y转化为W的离子方程式
(5)将X与Z、W的稀溶液混合,可生成淡黄色固体,则在该反应中还原产物与氧化产物的质量之比为
您最近半年使用:0次
2023-03-21更新
|
531次组卷
|
3卷引用:四川省成都市第七中学2022-2023学年高一下学期3月月考化学试题



