解题方法
1 . 下列离子方程式书写正确的是
A.向次氯酸钠溶液中通入少量CO2: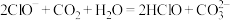 |
B.将少量氯气通入 溶液中: 溶液中: |
C.用铜作电极电解硫酸铜溶液: |
D.向 溶液中滴加少量的 溶液中滴加少量的 溶液: 溶液: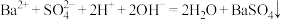 |
您最近半年使用:0次
名校
解题方法
2 . 下列离子方程式中正确的是
A.在足量烧碱溶液中氯气发生歧化反应: |
B.将氯气通入 溶液中: 溶液中: |
C.能证明氧化性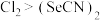 的反应: 的反应: |
D.次氯酸钠与亚硫酸钠反应: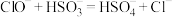 |
您最近半年使用:0次
2023-09-28更新
|
39次组卷
|
2卷引用:湖南省三湘创新发展联合体2023-2024学年高三上学期9月月考化学试题
3 . 在“价-类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及其定量关系。图中的字母分别代表硫及其常见化合物,f、g均为含钠元素的正盐,请回答:___________ ;
(2)固体f露置在空气中易变质转化为g,该转化的化学方程式为___________ ;
(3)某同学利用下列装置测定空气中 的含量。
的含量。___________ ,该装置中 与碘(
与碘( )溶液发生反应的离子方程式为:
)溶液发生反应的离子方程式为:___________ 。若空气流速为 ,当
,当 与碘(
与碘( )溶液恰好完全反应时,耗时10 min,则该空气样品中
)溶液恰好完全反应时,耗时10 min,则该空气样品中 的含量是
的含量是___________  。(用含V的最简表达式表示)。
。(用含V的最简表达式表示)。
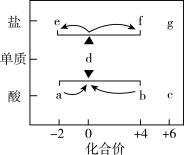
(2)固体f露置在空气中易变质转化为g,该转化的化学方程式为
(3)某同学利用下列装置测定空气中
 的含量。
的含量。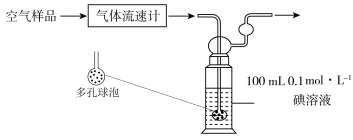
 与碘(
与碘( )溶液发生反应的离子方程式为:
)溶液发生反应的离子方程式为: ,当
,当 与碘(
与碘( )溶液恰好完全反应时,耗时10 min,则该空气样品中
)溶液恰好完全反应时,耗时10 min,则该空气样品中 的含量是
的含量是 。(用含V的最简表达式表示)。
。(用含V的最简表达式表示)。
您最近半年使用:0次
2023-09-08更新
|
249次组卷
|
2卷引用:湖南省邵阳市第二中学2023-2024学年高一下学期第一次月考化学试题
名校
4 . 硫元素的“价-类二维图”如图所示。下列有关叙述正确的是
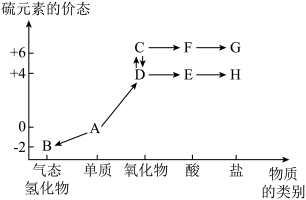

| A.硫元素的性质活泼,自然界中不存在物质A |
| B.气体D具有强还原性,不能用F的浓溶液干燥 |
| C.向H溶液中滴加G溶液并加热,可能生成气体D |
D.可用盐酸酸化的 溶液检验G中的阴离子 溶液检验G中的阴离子 |
您最近半年使用:0次
2023-04-12更新
|
593次组卷
|
3卷引用:湖南省邵阳市绥宁县第一中2022-2023学年高一下学期期中考试化学试题
5 . 亚硫酸钠(Na2SO3)是重要的工业原料,可用作织物漂白剂、染漂脱氧剂、香料和染料还原剂、造纸木质素脱除剂等。长期存放的亚硫酸钠可能会被部分氧化,某化学实验小组设计了如图实验方案测定某无水亚硫酸钠样品的纯度。

a、如图所示组装好实验装置;
b、……;
c、装好药品后通一段时间N2;
d、打开分液漏斗活塞和下口旋塞,缓慢滴入70%CuSO4至不再产生气体,关闭分液漏斗旋塞;
e、再次通入一段时间N2;
f、称量装置C的质量为m2g(实验前的质量为m1g)。
请回答下列问题:
(1)A中盛装样品的仪器名称是_____ ,B中盛放的试剂是_____ 。
(2)步骤b的操作为_____ ,步骤d产生的气体是____ 。
(3)步骤e再次通入氮气的目的是_____ 。
(4)亚硫酸钠的纯度为_____ 。(用含a、m1、m2的式子表示)
(5)有同学认为装置D多余,可否将装置D去掉?并请说出你的理由_____ 。

a、如图所示组装好实验装置;
b、……;
c、装好药品后通一段时间N2;
d、打开分液漏斗活塞和下口旋塞,缓慢滴入70%CuSO4至不再产生气体,关闭分液漏斗旋塞;
e、再次通入一段时间N2;
f、称量装置C的质量为m2g(实验前的质量为m1g)。
请回答下列问题:
(1)A中盛装样品的仪器名称是
(2)步骤b的操作为
(3)步骤e再次通入氮气的目的是
(4)亚硫酸钠的纯度为
(5)有同学认为装置D多余,可否将装置D去掉?并请说出你的理由
您最近半年使用:0次
2023-04-09更新
|
429次组卷
|
2卷引用:湖南省岳阳教研联盟2022-2023学年高一下学期联考联评化学试题
名校
解题方法
6 . 由下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向某溶液中加入适量 溶液,产生白色沉淀;将该白色沉淀加入到足量稀盐酸中,产生能使品红溶液褪色的气体 溶液,产生白色沉淀;将该白色沉淀加入到足量稀盐酸中,产生能使品红溶液褪色的气体 | 原溶液中一定含有大量的 |
| B | 向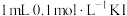 溶液中加入 溶液中加入 溶液,充分反应后,用 溶液,充分反应后,用 萃取分液, 萃取分液, 层呈紫红色;向水层中滴加KSCN溶液,溶液呈红色 层呈紫红色;向水层中滴加KSCN溶液,溶液呈红色 |  与 与 的反应是可逆反应 的反应是可逆反应 |
| C | 向蔗糖溶液中加入少量稀硫酸,水浴加热5min,加氢氧化钠溶液至溶液呈碱性,再加入少量新制的 ;继续加热5min,生成砖红色沉淀 ;继续加热5min,生成砖红色沉淀 | 蔗糖完全水解 |
| D | 取少量实验室保存的 固体溶于蒸馏水,加入过量稀盐酸,再加入 固体溶于蒸馏水,加入过量稀盐酸,再加入 溶液,有白色沉淀产生 溶液,有白色沉淀产生 |  固体样品已经变质 固体样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-03-10更新
|
497次组卷
|
2卷引用:湖南省名校联盟2023届高三下学期3月调研考试化学试题
7 . 某化学学习小组利用 溶液氧化环己醇(
溶液氧化环己醇( 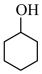 )制备环己酮(
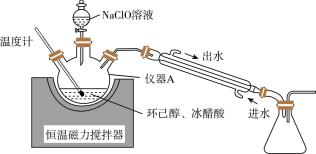
)制备环己酮( 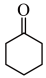 )的装置如图所示。
)的装置如图所示。
操作步骤如下:
ⅰ.向三颈烧瓶内加入环己醇、冰醋酸,逐滴加入NaClO溶液, 条件下反应30分钟后冷却。
条件下反应30分钟后冷却。
ⅱ.向三颈烧瓶内加入适量饱和NaHSO3溶液,用NaOH调节溶液显中性后加入饱和氯化钠溶液,然后经分液、干燥、蒸馏得到环己酮。
下列叙述错误的是
 溶液氧化环己醇(
溶液氧化环己醇(  )制备环己酮(
)制备环己酮(  )的装置如图所示。
)的装置如图所示。操作步骤如下:
ⅰ.向三颈烧瓶内加入环己醇、冰醋酸,逐滴加入NaClO溶液,
 条件下反应30分钟后冷却。
条件下反应30分钟后冷却。ⅱ.向三颈烧瓶内加入适量饱和NaHSO3溶液,用NaOH调节溶液显中性后加入饱和氯化钠溶液,然后经分液、干燥、蒸馏得到环己酮。

下列叙述错误的是
A.冰醋酸既作为溶剂,同时可增强 溶液的还原性 溶液的还原性 |
B.若 溶液滴加过快,三颈烧瓶中会产生少量黄绿色气体 溶液滴加过快,三颈烧瓶中会产生少量黄绿色气体 |
C.饱和亚硫酸氢钠的主要作用是除去 |
| D.饱和氯化钠可促进有机相和无机相分层 |
您最近半年使用:0次
解题方法
8 . 化学实验中常涉及除杂,下列关于除杂试剂的选择正确的是(括号内为杂质)
A. (气态的 (气态的 ):浓硫酸 ):浓硫酸 | B.亚硫酸钡(碳酸钡):稀盐酸 |
| C.氯气(乙烯):酸性高锰酸钾溶液 | D.镁粉(二氧化锰):浓盐酸、加热 |
您最近半年使用:0次
名校
解题方法
9 . 已知NH4CuSO3与足量的10mol/L硫酸混合微热,产生下列现象:
①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是
①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是
| A.反应中只有铜元素化合价发生变化 |
| B.1molNH4CuSO3完全反应转移1mol电子 |
| C.刺激性气味的气体可能是硫酸的还原产物 |
| D.刺激性气味的气体可能是氨气 |
您最近半年使用:0次
2022-11-01更新
|
164次组卷
|
3卷引用:湖南省衡阳市衡阳县第四中学2023-2024学年高三上学期11月期中化学试题
解题方法
10 . 磺酰氯 可用于制造锂电池的正极材料。实验室用
可用于制造锂电池的正极材料。实验室用 和
和 在活性炭催化下反应制取少量
在活性炭催化下反应制取少量 ,该反应为放热反应,装置如图所示(部分夹持装置省略)。回答下列问题:
,该反应为放热反应,装置如图所示(部分夹持装置省略)。回答下列问题:
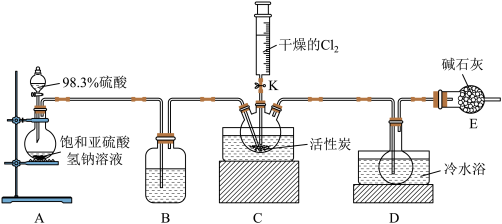
已知: 熔点为
熔点为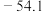 ℃,沸点为69.1℃,密度为
℃,沸点为69.1℃,密度为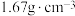 ,常温下较稳定,遇水剧烈反应,100℃以上易分解。
,常温下较稳定,遇水剧烈反应,100℃以上易分解。
(1)A装置中盛装硫酸的仪器名称是________ 。
(2)A装置中硫酸在该反应中表现出来的性质有________ (填标号)。
a.强氧化性 b.酸性 c.吸水性 d.脱水性
(3)B装置中试剂是________ (填名称)。实验前烘热C装置中三颈瓶和活性炭,其目的是________ 。
(4)D装置中冷水浴的作用是________ 。
(5)E装置的作用是________ 。
(6) 遇水生成两种强酸,写出发生反应的化学方程式:
遇水生成两种强酸,写出发生反应的化学方程式:________ 。
(7)标准状况下,通入C装置中的 和
和 的体积分别为2.24L和3.36L,最终得到
的体积分别为2.24L和3.36L,最终得到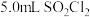 。则
。则 的产率为
的产率为________ (保留4位有效数字)。
 可用于制造锂电池的正极材料。实验室用
可用于制造锂电池的正极材料。实验室用 和
和 在活性炭催化下反应制取少量
在活性炭催化下反应制取少量 ,该反应为放热反应,装置如图所示(部分夹持装置省略)。回答下列问题:
,该反应为放热反应,装置如图所示(部分夹持装置省略)。回答下列问题:
已知:
 熔点为
熔点为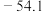 ℃,沸点为69.1℃,密度为
℃,沸点为69.1℃,密度为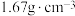 ,常温下较稳定,遇水剧烈反应,100℃以上易分解。
,常温下较稳定,遇水剧烈反应,100℃以上易分解。(1)A装置中盛装硫酸的仪器名称是
(2)A装置中硫酸在该反应中表现出来的性质有
a.强氧化性 b.酸性 c.吸水性 d.脱水性
(3)B装置中试剂是
(4)D装置中冷水浴的作用是
(5)E装置的作用是
(6)
 遇水生成两种强酸,写出发生反应的化学方程式:
遇水生成两种强酸,写出发生反应的化学方程式:(7)标准状况下,通入C装置中的
 和
和 的体积分别为2.24L和3.36L,最终得到
的体积分别为2.24L和3.36L,最终得到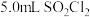 。则
。则 的产率为
的产率为
您最近半年使用:0次
2022-10-10更新
|
268次组卷
|
3卷引用:湖南省株洲市攸县第三中学2023届高三上学期第三次月考化学试题



