1 . 关于Na2SO3的说法错误的是
| A.Na2SO3溶液可用于吸收尾气中的SO2 |
| B.Na2SO3与Cl2共用不会增强漂白效果 |
| C.Na2SO3可通过灼烧NaHSO3固体的方法制得 |
| D.Na2SO3是否变质可利用BaCl2溶液和盐酸检验 |
您最近半年使用:0次
2 .  是一种常用的杀菌剂和催化剂。工业上制取
是一种常用的杀菌剂和催化剂。工业上制取 的工艺如图所示(制取
的工艺如图所示(制取 时需补加
时需补加 以保持反应在弱酸性条件下进行)。
以保持反应在弱酸性条件下进行)。

已知:溶液A的主要溶质M为酸式盐;化合物C为正盐;当溶液酸性减弱到一定程度时, 部分转化为
部分转化为 沉淀且满足
沉淀且满足 。
。
回答下列问题:
(1)M的化学式为___________ ;“真空蒸发”的原因是___________ 。
(2)溶液 发生反应的离子方程式为
发生反应的离子方程式为___________ ;若 产量不变,参与反应的化合物
产量不变,参与反应的化合物 与
与 物质的量之比减小时,需补加
物质的量之比减小时,需补加 的量
的量___________ (填“增大”、“减小”或“不变”)。
(3)为探究 的还原性,将一定量
的还原性,将一定量 与某浓度的硝酸反应,溶液的体积为
与某浓度的硝酸反应,溶液的体积为 ,溶液中
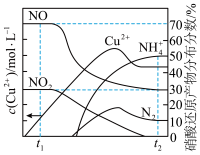
,溶液中 与硝酸还原产物的分布分数随时间的变化如图所示。则
与硝酸还原产物的分布分数随时间的变化如图所示。则 时刻,溶液中发生反应的化学方程式为
时刻,溶液中发生反应的化学方程式为___________ ; 时刻,测得溶液中
时刻,测得溶液中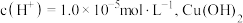 沉淀的质量为
沉淀的质量为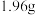 ,则此时溶液中
,则此时溶液中 为
为___________  (忽略溶液体积变化)。
(忽略溶液体积变化)。
 是一种常用的杀菌剂和催化剂。工业上制取
是一种常用的杀菌剂和催化剂。工业上制取 的工艺如图所示(制取
的工艺如图所示(制取 时需补加
时需补加 以保持反应在弱酸性条件下进行)。
以保持反应在弱酸性条件下进行)。
已知:溶液A的主要溶质M为酸式盐;化合物C为正盐;当溶液酸性减弱到一定程度时,
 部分转化为
部分转化为 沉淀且满足
沉淀且满足 。
。回答下列问题:
(1)M的化学式为
(2)溶液
 发生反应的离子方程式为
发生反应的离子方程式为 产量不变,参与反应的化合物
产量不变,参与反应的化合物 与
与 物质的量之比减小时,需补加
物质的量之比减小时,需补加 的量
的量(3)为探究
 的还原性,将一定量
的还原性,将一定量 与某浓度的硝酸反应,溶液的体积为
与某浓度的硝酸反应,溶液的体积为 ,溶液中
,溶液中 与硝酸还原产物的分布分数随时间的变化如图所示。则
与硝酸还原产物的分布分数随时间的变化如图所示。则 时刻,溶液中发生反应的化学方程式为
时刻,溶液中发生反应的化学方程式为 时刻,测得溶液中
时刻,测得溶液中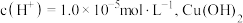 沉淀的质量为
沉淀的质量为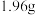 ,则此时溶液中
,则此时溶液中 为
为 (忽略溶液体积变化)。
(忽略溶液体积变化)。
您最近半年使用:0次
3 . 下列对物质检验或性质验证的实验操作不能达到实验目的的是
| 选项 | A | B | C | D |
| 目的 | 检验补铁剂中的 | 检验 是否沉淀完全 是否沉淀完全 | 验证 能否与水发生反应 能否与水发生反应 | 验证+4价硫元素的氧化性 |
| 操作 | 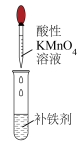 |  | 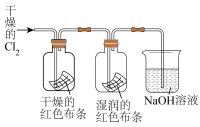 | 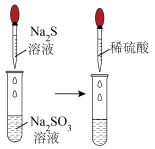 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
4 . 下列描述对应的离子方程式书写正确的是
A.利用覆铜板制作印刷电路板: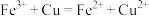 |
B.用 溶液吸收少量 溶液吸收少量 : : |
C. 溶于水: 溶于水: |
D.向澄清石灰水中滴入过量碳酸氢钠溶液: |
您最近半年使用:0次
名校
解题方法
5 . 在指定溶液中,下列离子一定能大量共存的是
A.透明澄清的溶液: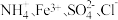 |
B.加入 NaHCO₃放出无色无味气体的溶液中: |
C.使酚酞变红的溶液: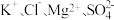 |
D.通入Cl₂至饱和的溶液: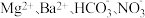 |
您最近半年使用:0次
6 . 下列事实涉及的化学反应错误的是
A.以赤铁矿为原料高炉炼铁: |
B.工业冶炼Mg: |
C.侯氏制碱法: |
D.用 溶液吸收少量 溶液吸收少量 : :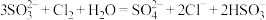 |
您最近半年使用:0次
名校
7 . 下列关于实验现象的描述错误的是
| A.将氯化铁溶液滴加到淀粉碘化钾试纸上,试纸变蓝 |
| B.向氢氧化铁胶体中滴加稀硫酸至过量,最终生成黄色溶液 |
| C.向亚硫酸中滴加氯水后,继续滴加氯化钡溶液,产生白色沉淀 |
| D.将SO2气体通入紫色石蕊试液中,溶液先变红后褪色 |
您最近半年使用:0次
8 . 下列有关物质的性质与用途不具有对应关系的是
| A.碳化硅硬度大,可用于制作砂轮磨料 |
| B.Na2SO3有还原性,可用于水处理中脱氯 |
| C.NH4HCO3受热易分解,可用作氮肥 |
| D.硫酸钡不溶于水和酸,且不容易被X射线透过,医疗上可用作消化系统X射线检测的内服药剂 |
您最近半年使用:0次
2023-10-08更新
|
120次组卷
|
2卷引用:山东省部分学校2024届高三上学期十月联考化学试题
名校
解题方法
9 . 下列除去杂质的方法正确的是
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | Cl2(HCl) | 饱和食盐水、洗气 |
| B | Na2SO3(NaHSO3) | 空气中加热 |
| C | CO2(SO2) | 品红溶液、洗气 |
| D | NO2(NO) | 水、洗气 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-09-15更新
|
237次组卷
|
2卷引用:山东省枣庄市第八中学2022-2023学年高一上学期期末考试化学试题
10 . 硫代硫酸钠(Na2S2O3)在纺织业、造纸业等领域有广泛应用。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O)。
【查阅资料】
ⅰ.Na2S2O3•5H2O易溶于水,遇酸易分解生成S和SO2。
ⅱ.向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3,所得产品常含有少量Na2SO3和Na2SO4。
ⅲ.Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
【制备产品】
实验装置如图所示(省略夹持装置):
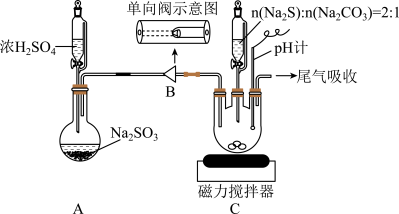
实验步骤:
ⅰ.检查装置气密性,按图示加入试剂。
ⅱ.先向C中烧瓶加入Na2S和Na2CO3混合溶液,再向A中烧瓶滴加浓H2SO4.装置A产生的SO2经过单向阀通入装置C中的混合溶液,加热、搅拌,至溶液pH约为7时,停止通入SO2气体,得产品混合溶液,结束反应。
ⅲ.过滤C中混合溶液,滤液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到Na2S2O3•5H2O产品。
请回答下列问题:
(1)反应开始后,C中先有浑浊产生,后又变澄清。此浑浊物是___________ (写化学式)。
(2)步骤Ⅰ单向阀的作用是___________ ;装置C中的反应混合溶液pH过高将导致产率降低,原因是___________ 。
(3)制备完成后,兴趣小组选用下列试剂设计实验方案检验硫代硫酸钠中含有硫酸根杂质:
试剂:稀盐酸、稀H2SO4、BaCl2溶液、Na2CO3溶液、H2O2溶液
(4)为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验步骤(ii)进行了改进,改进后的操作是___________ 。
【查阅资料】
ⅰ.Na2S2O3•5H2O易溶于水,遇酸易分解生成S和SO2。
ⅱ.向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3,所得产品常含有少量Na2SO3和Na2SO4。
ⅲ.Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
【制备产品】
实验装置如图所示(省略夹持装置):

实验步骤:
ⅰ.检查装置气密性,按图示加入试剂。
ⅱ.先向C中烧瓶加入Na2S和Na2CO3混合溶液,再向A中烧瓶滴加浓H2SO4.装置A产生的SO2经过单向阀通入装置C中的混合溶液,加热、搅拌,至溶液pH约为7时,停止通入SO2气体,得产品混合溶液,结束反应。
ⅲ.过滤C中混合溶液,滤液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到Na2S2O3•5H2O产品。
请回答下列问题:
(1)反应开始后,C中先有浑浊产生,后又变澄清。此浑浊物是
(2)步骤Ⅰ单向阀的作用是
(3)制备完成后,兴趣小组选用下列试剂设计实验方案检验硫代硫酸钠中含有硫酸根杂质:
试剂:稀盐酸、稀H2SO4、BaCl2溶液、Na2CO3溶液、H2O2溶液
| 实验步骤 | 现象 |
| ①取少量样品,加入除氧蒸馏水 | ②固体完全溶解得无色澄清溶液 |
| ③ | ④ |
| ⑤静置, | ⑥ |
您最近半年使用:0次



