名校
1 . W、X、Y、Z、M、R、Q均为短周期主族元素,其原子序数与原子半径关系如图所示。

请回答下列问题:
(1)R在元素周期表中的位置是_______ ;X的质量数分别为16和18的两种核素互为_______ 。
(2)Z与X形成的原子个数比为1:1的化合物与水反应的化学方程式为_______ 。
(3)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,被称为“对角线规则”,根据元素周期表的“对角线规则”,W单质及其化合物与M单质及其化合物的性质相似,写出W的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的离子方程式_______ 。
(4)用电子式表示 形成过程
形成过程_______ , 与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式
与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式_______ 。

请回答下列问题:
(1)R在元素周期表中的位置是
(2)Z与X形成的原子个数比为1:1的化合物与水反应的化学方程式为
(3)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,被称为“对角线规则”,根据元素周期表的“对角线规则”,W单质及其化合物与M单质及其化合物的性质相似,写出W的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的离子方程式
(4)用电子式表示
 形成过程
形成过程 与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式
与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式
您最近一年使用:0次
名校
2 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答问题:
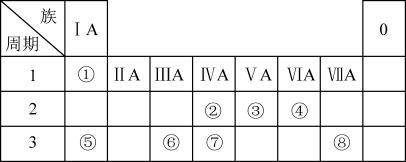
(1)地壳中含量居于第二位的元素在周期表中的位置是___________ 。
(2)⑦的最高价氧化物的水化物的分子式为___________ 。
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
(4)已知Cs元素位于元素周期表中第六周期第ⅠA族,请回答下列问题:
①铯的原子序数为___________ 。
②预测铯单质的还原性比钠单质的还原性___________ (填“弱”或“强”)。
③下列推断正确的是___________ (填字母)。
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,写出Y的原子序数b与a可能存在的所有的关系___________ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)⑦的最高价氧化物的水化物的分子式为
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
| A.最高正化合价为+6 |
| B.气态氢化物比H2S稳定 |
| C.最高价氧化物对应水化物的酸性比硫酸弱 |
| D.单质在常温下可与氢气化合 |
①铯的原子序数为
②预测铯单质的还原性比钠单质的还原性
③下列推断正确的是
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,写出Y的原子序数b与a可能存在的所有的关系
您最近一年使用:0次
2022-01-03更新
|
410次组卷
|
2卷引用:黑龙江省鹤岗市第一中学2021-2022学年高一上学期期末考试化学试题
名校
3 . 磷、硫元素的单质及其化合物应用广泛。
(1)磷元素在元素周期表中的位置是____ 。
(2)磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某微粒的浓度占各微粒浓度之和的分数)与pH的关系如图所示。
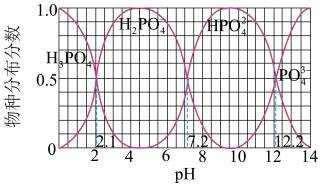
①为获得尽可能纯的NaH2PO4,pH应控制在____ ;pH=8时,溶液中主要含磷微粒浓度大小关系为c(HPO )
)____ c(H2PO )。(填“>”、“<”或“=”)
)。(填“>”、“<”或“=”)
②Na2HPO4溶液显碱性,试用数据及文字简述其原因____ 。
(3)H2O2的一种衍生物(NH4)2S2O8(过二硫酸铵),阴离子结构式为(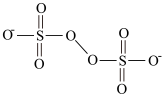 ),其S元素的化合价为
),其S元素的化合价为____ ;其溶液加热至沸后,S2O 与H2O反应,使溶液pH降低,写出S2O
与H2O反应,使溶液pH降低,写出S2O 与H2O反应的离子方程式:
与H2O反应的离子方程式:____ 。
(4)电解(NH4)2SO4和稀硫酸的混合溶液,常被用于电解产生(NH4)2S2O8,电解时均用惰性电极,阳极发生的电极反应式可表示为____ ;阴极生成的气体单质分子式为____ 。
(1)磷元素在元素周期表中的位置是
(2)磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某微粒的浓度占各微粒浓度之和的分数)与pH的关系如图所示。

①为获得尽可能纯的NaH2PO4,pH应控制在
 )
) )。(填“>”、“<”或“=”)
)。(填“>”、“<”或“=”)②Na2HPO4溶液显碱性,试用数据及文字简述其原因
(3)H2O2的一种衍生物(NH4)2S2O8(过二硫酸铵),阴离子结构式为(
 ),其S元素的化合价为
),其S元素的化合价为 与H2O反应,使溶液pH降低,写出S2O
与H2O反应,使溶液pH降低,写出S2O 与H2O反应的离子方程式:
与H2O反应的离子方程式:(4)电解(NH4)2SO4和稀硫酸的混合溶液,常被用于电解产生(NH4)2S2O8,电解时均用惰性电极,阳极发生的电极反应式可表示为
您最近一年使用:0次
名校
解题方法
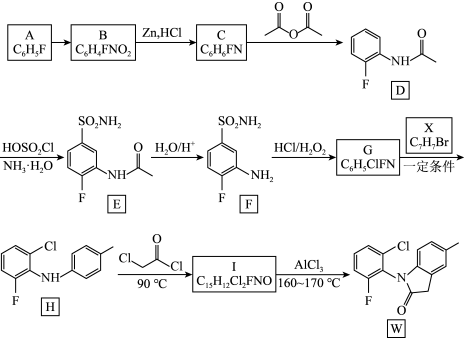
4 . 罗美昔布是一种抗炎药,临床用于治疗风湿性关节炎、牙痛等,化合物W是合成罗美昔布的一种中间体,W合成路线如下:
已知:(ⅰ)
(ⅱ)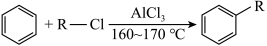
回答下列问题:
(1)A的化学名称为_______ ,B中含氧官能团的名称为_______ 。
(2)由C生成D的反应类型为_______ ;D中所含元素(H除外)第一电离能由大到小的顺序为_______ 。
(3)设置D→E和F→G两步反应的作用是_______ 。
(4)写出由G生成H的化学方程式_______ 。
(5)写出Ⅰ的结构简式_______ 。
(6)M为D的同系物,相对分子质量比D大14。M的同分异构体中同时满足下列条件的共有_______ 种(不考虑立体异构)。
①属于芳香族化合物;
②苯环上含有两个取代基,且位置相对;
③含有 ;
;
④能发生银镜反应。
满足上述条件的同分异构体中,核磁共振氢谱为3∶2∶2∶2∶1的同分异构体为_______ (写出其中两种的结构简式)。

已知:(ⅰ)

(ⅱ)
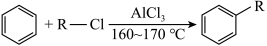
回答下列问题:
(1)A的化学名称为
(2)由C生成D的反应类型为
(3)设置D→E和F→G两步反应的作用是
(4)写出由G生成H的化学方程式
(5)写出Ⅰ的结构简式
(6)M为D的同系物,相对分子质量比D大14。M的同分异构体中同时满足下列条件的共有
①属于芳香族化合物;
②苯环上含有两个取代基,且位置相对;
③含有
 ;
;④能发生银镜反应。
满足上述条件的同分异构体中,核磁共振氢谱为3∶2∶2∶2∶1的同分异构体为
您最近一年使用:0次
2023-04-14更新
|
955次组卷
|
2卷引用:黑龙江省大庆市大庆中学2023届高三下学期模拟预测理综化学试题
名校
5 . 已知气体A能使溴水褪色,B、D、E、F能与Na反应,G具有水果香味的液体。转化关系如下图所示。
(1)A→B的反应类型___________ 。
(2)B的结构简式___________ 。
(3)D+F→G的化学方程式___________ 。
(4)A→G的七种物质中能与银氨溶液发生银镜反应的是___________ (填字母)。
(5)写出D的某种符合下列条件的同分异构体的结构简式的___________ 。
①具有水果香味;②能发生水解反应;③结构中含有3种等效氢。
(6)已知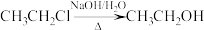 ,试写出以
,试写出以 为原料合成
为原料合成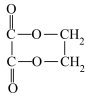 的路线(用流程图表示,无机试剂任选)
的路线(用流程图表示,无机试剂任选)___________ (流程图格式表示如下: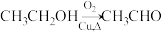 )
)

(1)A→B的反应类型
(2)B的结构简式
(3)D+F→G的化学方程式
(4)A→G的七种物质中能与银氨溶液发生银镜反应的是
(5)写出D的某种符合下列条件的同分异构体的结构简式的
①具有水果香味;②能发生水解反应;③结构中含有3种等效氢。
(6)已知
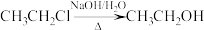 ,试写出以
,试写出以 为原料合成
为原料合成 的路线(用流程图表示,无机试剂任选)
的路线(用流程图表示,无机试剂任选)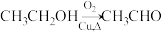 )
)
您最近一年使用:0次
2023-08-21更新
|
191次组卷
|
2卷引用:黑龙江省佳木斯高中教学联合体佳木斯八中等学校联考2023-2024学年高三上学期10月月考化学试题
解题方法
6 . 研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价—物质类别关系图如下。
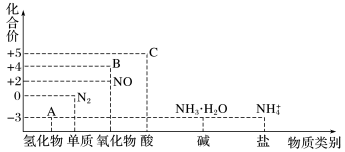
回答下列问题:
(1)氮气是空气的主要成分,性质十分稳定。氮元素在元素周期表中的位置是_______ 。
(2)物质A中的化学键为_______ 。(填极性键或非极性键)
(3)物质A与物质C反应生成的化合物属于_______ 化合物。(填离子或共价)
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:_______ 。当反应消耗3.36L(标准状况)物质B时,转移电子的物质的量为_______ mol。

回答下列问题:
(1)氮气是空气的主要成分,性质十分稳定。氮元素在元素周期表中的位置是
(2)物质A中的化学键为
(3)物质A与物质C反应生成的化合物属于
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:
您最近一年使用:0次
名校
解题方法
7 . Ⅰ.某气态烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,以A为原料的有机合成路线如下:

已知: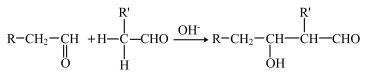
(1)D的核磁共振氢谱中有_______ 组峰,E中官能团名称_______ ,F的结构简式为_______ 。
(2)B→C的化学反应方程式为_______ 。
(3)F→G的反应类型为_______ 。
(4)H→I的化学反应方程式为_______ 。
Ⅱ.碳元素不仅可以形成大量的有机物,也可以形成无机物,例如金刚石。氮化硼晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被B原子代替。根据所学知识回答以下问题。
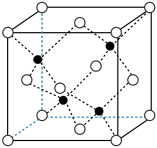
(5)BN晶体其晶胞参数为a pm,与同一个B原子相连的N原子构成的空间结构为_______ ,相邻的N与B之间的最近距离为_______ pm。BN的摩尔质量为M g·mol-1,阿伏加德罗常数的值为 ,则BN晶体的密度为
,则BN晶体的密度为_______ g·cm-3。
(6)晶体中距离同一个B原子最近的其他B原子个数为_______ 。
(7)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如图,1原子的分数坐标为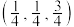 ,则4原子的分数坐标是
,则4原子的分数坐标是_______ 。


已知:

(1)D的核磁共振氢谱中有
(2)B→C的化学反应方程式为
(3)F→G的反应类型为
(4)H→I的化学反应方程式为
Ⅱ.碳元素不仅可以形成大量的有机物,也可以形成无机物,例如金刚石。氮化硼晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被B原子代替。根据所学知识回答以下问题。

(5)BN晶体其晶胞参数为a pm,与同一个B原子相连的N原子构成的空间结构为
 ,则BN晶体的密度为
,则BN晶体的密度为(6)晶体中距离同一个B原子最近的其他B原子个数为
(7)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如图,1原子的分数坐标为
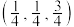 ,则4原子的分数坐标是
,则4原子的分数坐标是
您最近一年使用:0次
名校
8 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答问题:
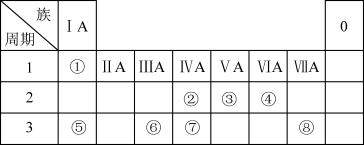
(1)地壳中含量居于第二位的元素在周期表中的位置是___________ 。
(2)②的最高价氧化物的结构式为___________ ;⑦的最高价氧化物的水化物的分子式为___________ 。
(3)④、⑤元素可形成既含离子键又含非极性共价键的离子化合物,写出该化合物的电子式:___________ ;写出⑥的氧化物与⑤的最高价氧化物的水化物反应的离子方程式___________ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________ (填字母)。
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
(5)已知Cs元素位于元素周期表中第六周期第ⅠA族,请回答下列问题:
①铯的原子序数为___________ 。
②预测铯单质的还原性比钠单质的还原性___________ (填“弱”或“强”)。
③下列推断正确的是___________ (填字母)。
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(6)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,写出Y的原子序数b与a可能存在的所有的关系___________ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)②的最高价氧化物的结构式为
(3)④、⑤元素可形成既含离子键又含非极性共价键的离子化合物,写出该化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
(5)已知Cs元素位于元素周期表中第六周期第ⅠA族,请回答下列问题:
①铯的原子序数为
②预测铯单质的还原性比钠单质的还原性
③下列推断正确的是
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(6)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,写出Y的原子序数b与a可能存在的所有的关系
您最近一年使用:0次
9 . 乙烯和丙烯是工业生产中非常重要的化工基本原料。
I.丙烯( )是一种重要的化工原料,它存在如下转化关系:
)是一种重要的化工原料,它存在如下转化关系:_______ 。
(2)在120℃、 条件下时,取一定体积的丙烯和足量的氧气混合点燃,相同条件下测得反应前后气体体积将
条件下时,取一定体积的丙烯和足量的氧气混合点燃,相同条件下测得反应前后气体体积将_______ (填“变大”“变小”或“不变”)。
(3)丙烯能使溴水褪色,其反应的化学方程式为_______ ,反应类型为_______ 。
Ⅱ.以乙烯为原料制备一种工业增塑剂的合成路线如图:_______ 。
(5)有机物B与足量金属钠反应的化学方程式为_______ 。
(6)合成增塑剂的化学方程式为_______ ,反应类型是_______ 。
I.丙烯(
 )是一种重要的化工原料,它存在如下转化关系:
)是一种重要的化工原料,它存在如下转化关系: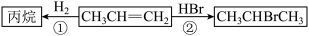
(2)在120℃、
 条件下时,取一定体积的丙烯和足量的氧气混合点燃,相同条件下测得反应前后气体体积将
条件下时,取一定体积的丙烯和足量的氧气混合点燃,相同条件下测得反应前后气体体积将(3)丙烯能使溴水褪色,其反应的化学方程式为
Ⅱ.以乙烯为原料制备一种工业增塑剂的合成路线如图:
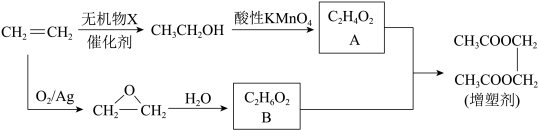
(5)有机物B与足量金属钠反应的化学方程式为
(6)合成增塑剂的化学方程式为
您最近一年使用:0次
2023-01-09更新
|
1271次组卷
|
4卷引用:黑龙江省哈尔滨市第一二二中学2021-2022学年高一下学期期末考试化学试题
黑龙江省哈尔滨市第一二二中学2021-2022学年高一下学期期末考试化学试题(已下线)专题06 乙醇、乙酸、糖、油、蛋白质(知识串讲+专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册)名校期末好题汇编-有机化合物(非选择题)新疆塔城地区第一高级中学2023-2024学年高二下学期5月期中考试化学试题
解题方法
10 . 根据如图,已知有机物A,B,C,D,E,F有以下转化关系。A是分子量为28的气体烯烃,其产量是衡量一个国家石油化工生产水平的标志;D是食醋的主要成分,E是不溶于水且具有香味的无色液体,相对分子质量是C的2倍,F是一种高分子化合物。结合如图关系回答问题:
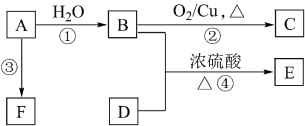
(1)写出B、D中官能团的名称:B_______ 、D_______ ;
(2)写出下列反应的化学方程式:
①_______ ;②_______ ;④_______ 。
(3)F是常见的高分子材料,合成F的化学方程式是_______ 。
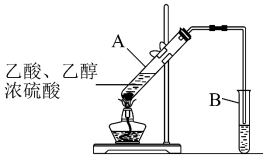
(4)根据下图,实验室用该装置制备E,试管A中浓硫酸的作用是_______ ;B中的试剂是_______ ;B中导管的位置在液面上方,目的是:_______ 。

(1)写出B、D中官能团的名称:B
(2)写出下列反应的化学方程式:
①
(3)F是常见的高分子材料,合成F的化学方程式是
(4)根据下图,实验室用该装置制备E,试管A中浓硫酸的作用是

您最近一年使用:0次
2021-09-06更新
|
39次组卷
|
2卷引用:黑龙江省齐齐哈尔三立高级中学2021-2022学年高二上学期期初考化学试题



