解题方法
1 . 废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备ZnSO4·7H2O和CuSO4·5H2O的部分实验步骤如下:
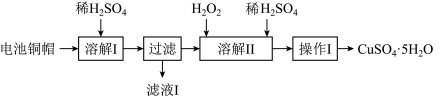
(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是_______ (任写一种方法)。
(2)从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为_______ 、_______ 、过滤、冰水洗涤、低温干燥。
(3)仔细分析流程,在“溶解II”步骤中,发生反应的化学方程式为_______ (用双线桥标出电子转移的方向和数目)。
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol/LNa2S2O3标准溶液至滴定终点,消耗Na2S2O3溶液25.00mL。
已知:2CuSO4+4KI=2CuI(白色)+I2+2K2SO4;2Na2S2O3+I2=2NaI+Na2S4O6
请依据实验数据计算样品中CuSO4·5H2O的质量分数_______ (写出计算过程,结果用百分数表示,小数点后保留1位有效数字)。

(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是
(2)从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为
(3)仔细分析流程,在“溶解II”步骤中,发生反应的化学方程式为
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol/LNa2S2O3标准溶液至滴定终点,消耗Na2S2O3溶液25.00mL。
已知:2CuSO4+4KI=2CuI(白色)+I2+2K2SO4;2Na2S2O3+I2=2NaI+Na2S4O6
请依据实验数据计算样品中CuSO4·5H2O的质量分数
您最近一年使用:0次
名校
解题方法
2 . I.现有一定量含有Na2O杂质的Na2O2试样,用如图所示的实验装置测定Na2O2试样的纯度(通过CO2与样品反应后生成O2的量测定Na2O2的含量。可供选用的反应物:CaCO3固体、盐酸、硫酸溶液和蒸馏水)。回答下列问题:
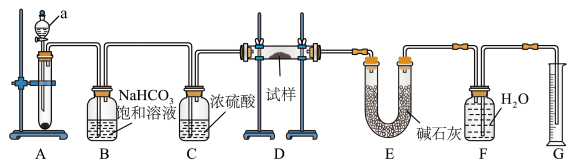
(1)装置a的名称为_____ 。
(2)装置B中除杂反应的离子方程式为_________ 。
(3)装置D中反应的化学方程式为_______ 。
(4)装置E中碱石灰的主要作用是________ 。
(5)已知装置D中试样质量为19.5g,装置G中所得O2体积为1120mL(已折算成标准状况下体积,且O2全部逸出)。求试样中Na2O2的质量分数___________ 。
Ⅱ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
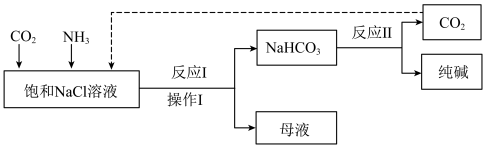
(6)为提高NaHCO3的产量,CO2和NH3通入饱和NaCl溶液的先后顺序为_____ 。
A.先通CO2再通NH3 B.先通NH3再通CO2

(1)装置a的名称为
(2)装置B中除杂反应的离子方程式为
(3)装置D中反应的化学方程式为
(4)装置E中碱石灰的主要作用是
(5)已知装置D中试样质量为19.5g,装置G中所得O2体积为1120mL(已折算成标准状况下体积,且O2全部逸出)。求试样中Na2O2的质量分数
Ⅱ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:

(6)为提高NaHCO3的产量,CO2和NH3通入饱和NaCl溶液的先后顺序为
A.先通CO2再通NH3 B.先通NH3再通CO2
您最近一年使用:0次
名校
解题方法
3 . 硫氰化钾(KSCN)是一种用途广泛的化学药品,常用于合成树脂、杀虫杀菌剂等。某化学小组用下图实验装置模拟工业制备硫氰化钾。
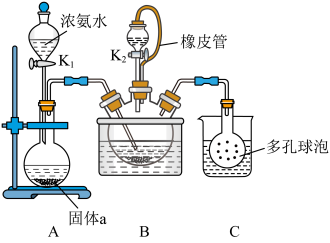
已知:①CS2为不溶于水且密度比水大的非极性试剂。
②NH4HS、(NH4)2S 在热水中易分解生成NH3和H2S。
③装置B中,滴液漏斗中装有一定体积5mol/L KOH溶液。
回答下列问题:
(1)制备NH4SCN溶液:
①三颈烧瓶内盛放有76g CS2、水和难溶于水的固体做催化剂。实验开始时,打开K1,水浴加热装置B,发生反应CS2+ 3NH3 NH4SCN + NH4HS, 则装置A中固体a的成分为
NH4SCN + NH4HS, 则装置A中固体a的成分为 _______ 。
②一段时间后,当观察到三颈烧瓶内_______ 时,关闭K1,停止通入气体,反应完成,将三颈烧瓶继续加热一段时间。
(2)制备KSCN晶体:打开K2,_______ , 干燥得到硫氰化钾晶体。(须用的试剂:5mol/LKOH、蒸馏水、稀硫酸)
(3)测定产品中KSCN的含量:称取0.85g样品,配成100mL溶液。量取25.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴铁盐溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,滴定时发生的反应:SCN—+Ag+=AgSCN↓(白色),达到滴定终点,三次滴定平均消耗AgNO3标准溶液20.00mL。产品中KSCN的质量分数为_______ 。(写出计算过程)

已知:①CS2为不溶于水且密度比水大的非极性试剂。
②NH4HS、(NH4)2S 在热水中易分解生成NH3和H2S。
③装置B中,滴液漏斗中装有一定体积5mol/L KOH溶液。
回答下列问题:
(1)制备NH4SCN溶液:
①三颈烧瓶内盛放有76g CS2、水和难溶于水的固体做催化剂。实验开始时,打开K1,水浴加热装置B,发生反应CS2+ 3NH3
 NH4SCN + NH4HS, 则装置A中固体a的成分为
NH4SCN + NH4HS, 则装置A中固体a的成分为 ②一段时间后,当观察到三颈烧瓶内
(2)制备KSCN晶体:打开K2,
(3)测定产品中KSCN的含量:称取0.85g样品,配成100mL溶液。量取25.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴铁盐溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,滴定时发生的反应:SCN—+Ag+=AgSCN↓(白色),达到滴定终点,三次滴定平均消耗AgNO3标准溶液20.00mL。产品中KSCN的质量分数为
您最近一年使用:0次
4 . 三氯化铬(CrCl3)在工业上主要用作媒染剂和催化剂,实验室模拟工业上以BaCrO4为原料制备CrCl3。
(1)制备CrCl3
取一定质量的BaCrO4和对应量的水加入到三预瓶中,水浴加热并搅拌,一段时间后同时加入过量浓盐酸和无水乙醇(C2H5OH)充分反应,生成CrC13并放出CO2气体。
①上述反应的化学方程式为__________ 。
②上述反应中的乙醇与BaCrO4投料的物质的量比例大约为3:8,原因是__________ 。
(2)测定CrCl3的质量分数。
Ⅰ.称取样品0.3300g,加水溶解并配成250.0mL的溶液。
Ⅱ.移取25.00mL样品溶液于带塞的锥形瓶中,加热至沸后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的硫酸酸化,将Cr3+氧化为Cr2O ;再加入过量KI固体,加塞揺匀。使铬元素完全以Cr3+的形式存在。
;再加入过量KI固体,加塞揺匀。使铬元素完全以Cr3+的形式存在。
Ⅲ.加入少量淀粉溶液,用0.0500mol·L-1标准Na2S2O3溶液滴定至终点,平行测定3次。平均消耗标准Na2S2O3溶液12.00mL。
已知反应: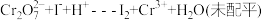 ;
;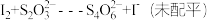
①滴定终点的现象是__________ 。
②计算CrC13的质量分数(写出计算过程,结果保留3位有效数字)__________
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有__________ (填字母)
A.碱式滴定管使用前,水洗后未用标准Na2S2O3溶液润洗
B.锥形瓶水洗后未干燥
C滴定终点读数时俯视读数
D.滴定前碱式滴定管尖嘴部分有气泡,滴定后消失
(3)CrC13样品中C1-含量测定
实验室可用AgNO3标准溶液测定CrCl3样品中C1-的含量,请补充完成相应的实验步骤:准确量取25.00mL待测样品溶液于锥形瓶中,__________ ,进行数据处理。(终点反应为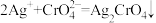 砖红色)。实验中须使用的试剂有:K2CO3溶液、AgNO3标准溶液:除常用仪器外须使用的仪器有:棕色酸式滴定管)
砖红色)。实验中须使用的试剂有:K2CO3溶液、AgNO3标准溶液:除常用仪器外须使用的仪器有:棕色酸式滴定管)
(1)制备CrCl3
取一定质量的BaCrO4和对应量的水加入到三预瓶中,水浴加热并搅拌,一段时间后同时加入过量浓盐酸和无水乙醇(C2H5OH)充分反应,生成CrC13并放出CO2气体。
①上述反应的化学方程式为
②上述反应中的乙醇与BaCrO4投料的物质的量比例大约为3:8,原因是
(2)测定CrCl3的质量分数。
Ⅰ.称取样品0.3300g,加水溶解并配成250.0mL的溶液。
Ⅱ.移取25.00mL样品溶液于带塞的锥形瓶中,加热至沸后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的硫酸酸化,将Cr3+氧化为Cr2O
 ;再加入过量KI固体,加塞揺匀。使铬元素完全以Cr3+的形式存在。
;再加入过量KI固体,加塞揺匀。使铬元素完全以Cr3+的形式存在。Ⅲ.加入少量淀粉溶液,用0.0500mol·L-1标准Na2S2O3溶液滴定至终点,平行测定3次。平均消耗标准Na2S2O3溶液12.00mL。
已知反应:
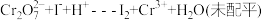 ;
;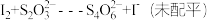
①滴定终点的现象是
②计算CrC13的质量分数(写出计算过程,结果保留3位有效数字)
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有
A.碱式滴定管使用前,水洗后未用标准Na2S2O3溶液润洗
B.锥形瓶水洗后未干燥
C滴定终点读数时俯视读数
D.滴定前碱式滴定管尖嘴部分有气泡,滴定后消失
(3)CrC13样品中C1-含量测定
实验室可用AgNO3标准溶液测定CrCl3样品中C1-的含量,请补充完成相应的实验步骤:准确量取25.00mL待测样品溶液于锥形瓶中,
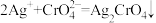 砖红色)。实验中须使用的试剂有:K2CO3溶液、AgNO3标准溶液:除常用仪器外须使用的仪器有:棕色酸式滴定管)
砖红色)。实验中须使用的试剂有:K2CO3溶液、AgNO3标准溶液:除常用仪器外须使用的仪器有:棕色酸式滴定管)
您最近一年使用:0次
22-23高三上·江苏南通·开学考试
名校
5 . ClO2是一种高效消毒灭菌剂,可用于灭活新冠病毒。ClO2稳定性差,工业上可将ClO2转化为较稳定的NaClO2保存。一种由NaClO3制取NaClO2晶体的流程如下:

已知高于60℃时,NaClO2易分解为NaClO3和NaCl。
(1)制C1O2.向用硫酸酸化的NaClO3中通入混有空气(起稀释作用)的SO2的气体,可制得C1O2气体。其他条件一定,若通入的SO2过量,所得ClO2的体积将减小,原因是_______ 。
(2)制NaClO2溶液。将一定量的ClO2通入NaOH和H2O2的混合溶液中,充分反应后可制得NaClO2溶液。由该反应可以比较反应物和产物中两种微粒的氧化性大小。碱性条件下,两种微粒的氧化性大小规律为_______>_______。_______
(3)制NaClO2晶体。已知NaClO2的溶解度曲线如图所示。设计由质量分数为10%的NaClO2溶液(含少量NaOH)制取NaClO2·3H2O晶体的实验方案:_______ 。

(4)NaClO2晶体使用时,向其中加入盐酸,即可得到ClO2气体。已知反应产物中只有一种气体和一种盐,则消耗1molNaClO2,可生成ClO2的物质的量为_______ 。
(5)ClO2还可将碱性废水中的CN-化为N2和CO ,自身转化为Cl-。经测定,某冶炼废水中CN-含量为1040mg·L-1,处理该废水10m3,理论上需要通入标准状况下ClO2的体积为多少升?(写出计算过程)
,自身转化为Cl-。经测定,某冶炼废水中CN-含量为1040mg·L-1,处理该废水10m3,理论上需要通入标准状况下ClO2的体积为多少升?(写出计算过程)__________

已知高于60℃时,NaClO2易分解为NaClO3和NaCl。
(1)制C1O2.向用硫酸酸化的NaClO3中通入混有空气(起稀释作用)的SO2的气体,可制得C1O2气体。其他条件一定,若通入的SO2过量,所得ClO2的体积将减小,原因是
(2)制NaClO2溶液。将一定量的ClO2通入NaOH和H2O2的混合溶液中,充分反应后可制得NaClO2溶液。由该反应可以比较反应物和产物中两种微粒的氧化性大小。碱性条件下,两种微粒的氧化性大小规律为_______>_______。
(3)制NaClO2晶体。已知NaClO2的溶解度曲线如图所示。设计由质量分数为10%的NaClO2溶液(含少量NaOH)制取NaClO2·3H2O晶体的实验方案:

(4)NaClO2晶体使用时,向其中加入盐酸,即可得到ClO2气体。已知反应产物中只有一种气体和一种盐,则消耗1molNaClO2,可生成ClO2的物质的量为
(5)ClO2还可将碱性废水中的CN-化为N2和CO
 ,自身转化为Cl-。经测定,某冶炼废水中CN-含量为1040mg·L-1,处理该废水10m3,理论上需要通入标准状况下ClO2的体积为多少升?(写出计算过程)
,自身转化为Cl-。经测定,某冶炼废水中CN-含量为1040mg·L-1,处理该废水10m3,理论上需要通入标准状况下ClO2的体积为多少升?(写出计算过程)
您最近一年使用:0次
名校
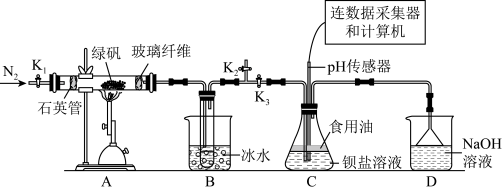
6 . 某实验小组利用如图装置模拟古法硫酸生产方法并进行SO2性质探究。
 -
-
已知A中反应的化学方程式2FeSO4•7H2O Fe2O3+SO2↑+SO3↑+14H2O。
Fe2O3+SO2↑+SO3↑+14H2O。
实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活区K3,高温加热绿矾。
完成下列填空:
(1)先通入一段时间N2的目的是____ ;D装置的作用____ 。
(2)B中所得硫酸溶液的质量分数理论值为____ (保留三位小数)。
为探究SO2与钡盐溶液的反点,在装置C中先后四次加入不同的溶液:
得到如图pH-t图:
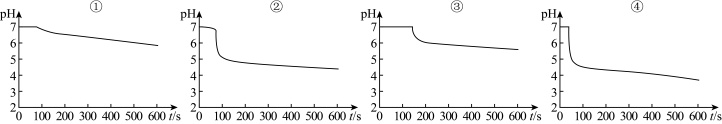
(3)曲线①显缓慢下降趋势,这是因为____ 。曲线②出现骤降,表明溶液中生成了____ (填物质名称)。
(4)对比分析上述四组数据,可得出的结论是____ (任写2条)。
(5)为对接气法收集到的SO2气体进行含量测定,将2240mL(已折算为标准状况)通入足量的Ba(NO3)2溶液中,经过滤、洗涤、烘干,最终得到沉淀20.97g,则SO2气体的体积分数为____ 。若该实验数据较实际值偏大,则可能的原因是____ (选填编号)。
a.气体通入速率过快 b.未用食用油覆盖液面
c.收集的气体中有CO2 d.沉淀未进行恒重操作
 -
-已知A中反应的化学方程式2FeSO4•7H2O
 Fe2O3+SO2↑+SO3↑+14H2O。
Fe2O3+SO2↑+SO3↑+14H2O。实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活区K3,高温加热绿矾。
完成下列填空:
(1)先通入一段时间N2的目的是
(2)B中所得硫酸溶液的质量分数理论值为
为探究SO2与钡盐溶液的反点,在装置C中先后四次加入不同的溶液:
| ① | ② | ③ | ④ |
| 已煮沸的BaCl2溶液 | 未煮沸的BaCl2溶液 | 已煮沸的Ba(NO3)2溶液 | 未煮沸的Ba(NO3)2溶液 |
| 注:锥形瓶中溶液体积相同,钡盐溶液浓度相同;油层厚度一致,通入SO2流速一致。 | |||

(3)曲线①显缓慢下降趋势,这是因为
(4)对比分析上述四组数据,可得出的结论是
(5)为对接气法收集到的SO2气体进行含量测定,将2240mL(已折算为标准状况)通入足量的Ba(NO3)2溶液中,经过滤、洗涤、烘干,最终得到沉淀20.97g,则SO2气体的体积分数为
a.气体通入速率过快 b.未用食用油覆盖液面
c.收集的气体中有CO2 d.沉淀未进行恒重操作
您最近一年使用:0次
2022-10-14更新
|
376次组卷
|
2卷引用:江苏省扬州市广陵区名校2022-2023学年高一上学期12月月考化学试题
解题方法
7 . 四氧化三铅(Pb3O4,也可写作2PbO•PbO2)俗名“铅丹”或“红丹”,可用作防锈剂。工业上以废旧铅酸电池的铅膏(主要成分是PbSO4和PbO2)为原料制备Pb3O4的流程如图:
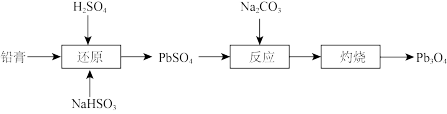
(1)CO 中碳原子杂化方式为
中碳原子杂化方式为____ 。
(2)“还原”时的化学方程式为____ 。
(3)已知:Ksp(PbCO3)=1.5×10-13。若使溶液中Pb2+的浓度小于1×10-5mol·L-1,此时溶液中的c(CO )>
)>____ mol·L-1。
(4)为测定某样品四氧化三铅含量,称取样品0.1200g,加入足量的6mol·L-1HNO3充分溶解,过滤,得到含Pb2+的滤液和PbO2固体。将固体PbO2连同滤纸一并置于另一只锥形瓶中,加入足量的醋酸和醋酸钠混合溶液,再加入过量KI,使PbO2充分氧化I-,以淀粉溶液作指示剂,用0.01000mol·L-1Na2S2O3溶液滴定,终点时用去30.00mL。已知:I2+2Na2S2O3=Na2S4O6+2NaI。
①所加KI必须过量,原因是____ 。
②计算试样中Pb3O4的质量分数____ 。(写出计算过程)

(1)CO
 中碳原子杂化方式为
中碳原子杂化方式为(2)“还原”时的化学方程式为
(3)已知:Ksp(PbCO3)=1.5×10-13。若使溶液中Pb2+的浓度小于1×10-5mol·L-1,此时溶液中的c(CO
 )>
)>(4)为测定某样品四氧化三铅含量,称取样品0.1200g,加入足量的6mol·L-1HNO3充分溶解,过滤,得到含Pb2+的滤液和PbO2固体。将固体PbO2连同滤纸一并置于另一只锥形瓶中,加入足量的醋酸和醋酸钠混合溶液,再加入过量KI,使PbO2充分氧化I-,以淀粉溶液作指示剂,用0.01000mol·L-1Na2S2O3溶液滴定,终点时用去30.00mL。已知:I2+2Na2S2O3=Na2S4O6+2NaI。
①所加KI必须过量,原因是
②计算试样中Pb3O4的质量分数
您最近一年使用:0次
名校
解题方法
8 . I.三聚氰胺最早被李比希于1834年合成,有毒,不可用于食品加工或食品添加剂。经李比希法分析得知,三聚氰胺分子中,氮元素的含量高达66.67%,氢元素的质量分数为4.76%,其余为碳元素。它的相对分子质量大于100,但小于150。试回答下列问题:
(1)分子式中原子个数比N(C)∶N(H)∶N(N)=___________ 。
(2)三聚氰胺分子中碳原子数为___________ 。
(3)三聚氰胺的分子式为___________ 。
(4)若核磁共振氢谱显示只有1个吸收峰,红外光谱表明有1个由碳、氮两种元素组成的六元杂环。则三聚氰胺的结构简式为___________ 。
II.乙酸乙酯是一种良好的工业溶剂,可通过下列转化制取(部分反应条件略去):
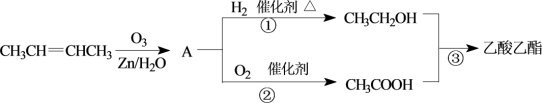
(5)CH3CH2OH中官能团的名称是___________ 。
(6)反应①是加成反应,CH3COOH的相对分子质量比A的相对分子质量大16。有机物A的结构简式是___________ ,反应②的反应类型是___________ 。
(7)CH3COOH在一定条件下反应可生成一种有机物Q。该有机物Q的摩尔质量是102 g·mol-1,其中氧的质量分数为47.06%,碳氢原子个数比为2∶3。有机物Q的分子式是___________ 。
(1)分子式中原子个数比N(C)∶N(H)∶N(N)=
(2)三聚氰胺分子中碳原子数为
(3)三聚氰胺的分子式为
(4)若核磁共振氢谱显示只有1个吸收峰,红外光谱表明有1个由碳、氮两种元素组成的六元杂环。则三聚氰胺的结构简式为
II.乙酸乙酯是一种良好的工业溶剂,可通过下列转化制取(部分反应条件略去):
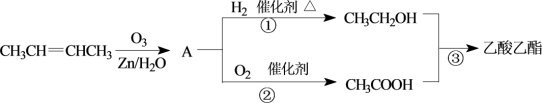
(5)CH3CH2OH中官能团的名称是
(6)反应①是加成反应,CH3COOH的相对分子质量比A的相对分子质量大16。有机物A的结构简式是
(7)CH3COOH在一定条件下反应可生成一种有机物Q。该有机物Q的摩尔质量是102 g·mol-1,其中氧的质量分数为47.06%,碳氢原子个数比为2∶3。有机物Q的分子式是
您最近一年使用:0次
名校
解题方法
9 . 某化学兴趣小组同学展开对漂白剂亚氯酸钠( )的研究。实验室制取亚氯酸钠的装置如下图所示:
)的研究。实验室制取亚氯酸钠的装置如下图所示:
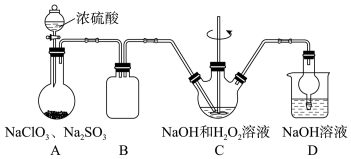
已知: 浓度过高时易发生分解;
浓度过高时易发生分解;
(1)装置 中工业上常用
中工业上常用 代替
代替 来制备
来制备 ,反应的化学方程式为
,反应的化学方程式为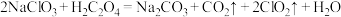 ,相比较而言,用
,相比较而言,用 制备
制备 ,其优点为
,其优点为___________ 。
(2)装置 用于制备亚氯酸钠(
用于制备亚氯酸钠( ),装置
),装置 中发生的离子方程式为
中发生的离子方程式为___________ 。装置 中反应为放热反应,在不改变反应物浓度和体积及搅拌速度的条件下,为了防止温度过高,实验中可采取的措施:缓慢滴加浓硫酸、
中反应为放热反应,在不改变反应物浓度和体积及搅拌速度的条件下,为了防止温度过高,实验中可采取的措施:缓慢滴加浓硫酸、___________ 。
(3)设计验证装置 中生成的
中生成的 (混有少量
(混有少量 )具有氧化性的实验方案:取反应后装置
)具有氧化性的实验方案:取反应后装置 中的溶液,调节溶液呈中性,
中的溶液,调节溶液呈中性,___________ 。(已知:酸性条件下 将
将 氧化为
氧化为 ,实验中须使用的试剂:
,实验中须使用的试剂: 、稀硫酸溶液、
、稀硫酸溶液、 淀粉溶液)
淀粉溶液)
(4)测定实验所得亚氯酸钠样品中的 含量(杂质不参与反应)的方法如下:准确称取
含量(杂质不参与反应)的方法如下:准确称取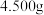 亚氯酸钠样品,加入
亚氯酸钠样品,加入 稀硫酸至完全溶解配制成
稀硫酸至完全溶解配制成 溶液,取出
溶液,取出 溶液于锥形瓶中,先加入
溶液于锥形瓶中,先加入 硫酸亚铁标准溶液
硫酸亚铁标准溶液 ,充分反应后,再用
,充分反应后,再用 酸性
酸性 溶液滴定至终点,消耗酸性
溶液滴定至终点,消耗酸性 溶液
溶液 。过程中发生的方程式为:
。过程中发生的方程式为:
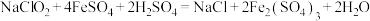
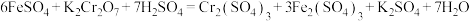
计算样品中 的质量分数,写出计算过程。
的质量分数,写出计算过程。___________
 )的研究。实验室制取亚氯酸钠的装置如下图所示:
)的研究。实验室制取亚氯酸钠的装置如下图所示:
已知:
 浓度过高时易发生分解;
浓度过高时易发生分解;(1)装置
 中工业上常用
中工业上常用 代替
代替 来制备
来制备 ,反应的化学方程式为
,反应的化学方程式为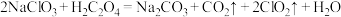 ,相比较而言,用
,相比较而言,用 制备
制备 ,其优点为
,其优点为(2)装置
 用于制备亚氯酸钠(
用于制备亚氯酸钠( ),装置
),装置 中发生的离子方程式为
中发生的离子方程式为 中反应为放热反应,在不改变反应物浓度和体积及搅拌速度的条件下,为了防止温度过高,实验中可采取的措施:缓慢滴加浓硫酸、
中反应为放热反应,在不改变反应物浓度和体积及搅拌速度的条件下,为了防止温度过高,实验中可采取的措施:缓慢滴加浓硫酸、(3)设计验证装置
 中生成的
中生成的 (混有少量
(混有少量 )具有氧化性的实验方案:取反应后装置
)具有氧化性的实验方案:取反应后装置 中的溶液,调节溶液呈中性,
中的溶液,调节溶液呈中性, 将
将 氧化为
氧化为 ,实验中须使用的试剂:
,实验中须使用的试剂: 、稀硫酸溶液、
、稀硫酸溶液、 淀粉溶液)
淀粉溶液)(4)测定实验所得亚氯酸钠样品中的
 含量(杂质不参与反应)的方法如下:准确称取
含量(杂质不参与反应)的方法如下:准确称取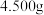 亚氯酸钠样品,加入
亚氯酸钠样品,加入 稀硫酸至完全溶解配制成
稀硫酸至完全溶解配制成 溶液,取出
溶液,取出 溶液于锥形瓶中,先加入
溶液于锥形瓶中,先加入 硫酸亚铁标准溶液
硫酸亚铁标准溶液 ,充分反应后,再用
,充分反应后,再用 酸性
酸性 溶液滴定至终点,消耗酸性
溶液滴定至终点,消耗酸性 溶液
溶液 。过程中发生的方程式为:
。过程中发生的方程式为: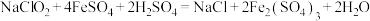
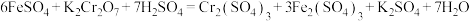
计算样品中
 的质量分数,写出计算过程。
的质量分数,写出计算过程。
您最近一年使用:0次
10 . 水合肼(N2H4·H2O)是一种精细化工原料,常用于医药、农药、染料、航天等领域。实验室模拟尿素法制备N2H4·H2O流程图如图所示。
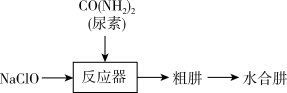
已知:①N2H4·H2O具有强还原性,易被氧化成N2。
②N2H4·H2O+H2SO4+6NaHCO3+2I2=N2↑+6CO2+Na2SO4+4NaI+7H2O
(1)CO(NH2)2(尿素)是常见的化肥,其在土壤中水解生成碳酸铵或碳酸氢铵,写出其水解生成碳酸氢铵的化学方程式_______ 。
(2)制备过程中NaClO溶液不能过量,其可能的原因是_______ 。
(3)水合肼(N2H4·H2O)产品含量测定步骤:将1.000g样品配制成100mL溶液,取5mL溶液于锥形瓶中,加入30mL水,再加入适量稀硫酸及NaHCO3固体,用0.1000mol·L-1标准碘溶液滴定至终点,消耗16.8mL,计算该产品中水合肼的质量分数_______ (写出计算过程,结果保留1位小数)。

已知:①N2H4·H2O具有强还原性,易被氧化成N2。
②N2H4·H2O+H2SO4+6NaHCO3+2I2=N2↑+6CO2+Na2SO4+4NaI+7H2O
(1)CO(NH2)2(尿素)是常见的化肥,其在土壤中水解生成碳酸铵或碳酸氢铵,写出其水解生成碳酸氢铵的化学方程式
(2)制备过程中NaClO溶液不能过量,其可能的原因是
(3)水合肼(N2H4·H2O)产品含量测定步骤:将1.000g样品配制成100mL溶液,取5mL溶液于锥形瓶中,加入30mL水,再加入适量稀硫酸及NaHCO3固体,用0.1000mol·L-1标准碘溶液滴定至终点,消耗16.8mL,计算该产品中水合肼的质量分数
您最近一年使用:0次



