解题方法
1 . 工业上将CO2通入到NH3的饱和NaCl溶液中制取NaHCO3,下列说法不正确 的是
| A.食品膨松剂的成份之一是NaHCO3 | B. 电离出H+使NaHCO3溶液显酸性 电离出H+使NaHCO3溶液显酸性 |
| C. NaHCO3不稳定,受热容易分解 | D.盐酸与NaHCO3反应放出大量气泡并吸收热量 |
您最近一年使用:0次
解题方法
2 . 下列表示不正确 的是
A. 的电子式: 的电子式:  | B. 的价层电子对互斥模型: 的价层电子对互斥模型: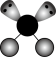 |
C. 的 的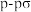 键的模型: 键的模型: | D. 的名称:1,3,4-三甲苯 的名称:1,3,4-三甲苯 |
您最近一年使用:0次
名校
3 . 丙烯酸(CH2=CHCOOH)是一种重要的化工原料。用它合成的聚丙烯酸(PAA)对水中碳酸钙和氢氧化钙有优良的分解作用。它能发生如下转化:
(1)反应①的反应类型为___________ ;物质B的官能团名称为___________ 。
(2)聚丙烯酸PPA的结构简式为___________ 。
(3)写出浓硫酸加热 条件下发生反应③的化学方程式___________ 。
(4)下列说法正确的是___________。
(5)写出B的同分异构体,要求不同化学环境氢只一种:___________ 。
(6)已知R-CN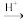 R-COOH,请设计由乙炔(CH≡CH)和HCN为原料合成D的路线图
R-COOH,请设计由乙炔(CH≡CH)和HCN为原料合成D的路线图___________ 。(参考流程图CH2=CH2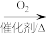 CH3CHO,表示,无机试剂任选)
CH3CHO,表示,无机试剂任选)

(1)反应①的反应类型为
(2)聚丙烯酸PPA的结构简式为
(3)写出
(4)下列说法正确的是___________。
| A.物质A能使酸性高锰酸钾溶液褪色 | B.可用NaOH溶液除去D中含有少量的A |
| C.物质A、B均能与NaOH反应 | D.反应④为取代反应 |
(5)写出B的同分异构体,要求不同化学环境氢只一种:
(6)已知R-CN
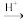 R-COOH,请设计由乙炔(CH≡CH)和HCN为原料合成D的路线图
R-COOH,请设计由乙炔(CH≡CH)和HCN为原料合成D的路线图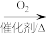 CH3CHO,表示,无机试剂任选)
CH3CHO,表示,无机试剂任选)
您最近一年使用:0次
名校
解题方法
4 . 下列事实的解释不正确的是
| 事实 | 解释 | |
| A | 晶体熔点:HF>HCl | HF分子内H-F键能大于HCl分子内H-Cl键能 |
| B | 向2.0mL浓度均为0.1mol/L的KCl、KI混合溶液中滴加1-2滴0.01mol/LAgNO3溶液,振荡,沉淀呈黄色 | Ksp:AgCl>AgI |
| C | CH 中H-C-H键角比CH 中H-C-H键角比CH 中的大 中的大 | 中心原子的孤电子对数目CH >CH >CH ,孤电子对与成键电子对之间的斥力>成键电子对之间的斥力 ,孤电子对与成键电子对之间的斥力>成键电子对之间的斥力 |
| D | 酸性:CF3COOH>CCl3COOH | 氟的电负性大于氯的电负性,F-C的极性大于Cl-C的性,使-CF3的极性大于-CCl3的极性,导致CF3COOH的羧基中的羟基的极性更大,更易电离出H+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 下列说法正确的是
| A.等质量的—OH和OH-含有的电子数目相等 | B.丁基(—C4H9)有四种结构 |
| C.C2H4和C4H8一定互为同系物 | D.异丁烷的熔沸点高于正丁烷 |
您最近一年使用:0次
名校
6 . 下列说法正确的是
A.Al2Cl6的结构式为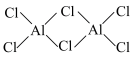 ,1mol该分子中含配位键的数目为4NA ,1mol该分子中含配位键的数目为4NA |
| B.NaClO溶液中加水,ClO-的水解程度增大,溶液碱性减弱 |
C.反应2BaO2(s) 2BaO(s)+O2(g)达到平衡后压缩体积,达到新平衡后c(O2)变大 2BaO(s)+O2(g)达到平衡后压缩体积,达到新平衡后c(O2)变大 |
| D.被保护的钢铁设备作阴极,用Zn电极作辅助阳极,该方法为外加电流法 |
您最近一年使用:0次
名校
解题方法
7 . 用NA表示阿伏加德罗常数的值。下列说法不正确 的是
| A.12g 金刚石中所C—C键数目为2NA |
| B.H2S、H2Se、H2O 分子间作用力依次增大 |
| C.标准状况下,将11.2 L Cl2通入水中,溶液中Cl-数目为0.5NA |
| D.4.4 g C2H4O中含有σ键数目最多为0.7NA |
您最近一年使用:0次
名校
解题方法
8 . 苯甲酸[M(苯甲酸)=122g/mol]是一种常用的食品防腐剂,微溶于水,易溶于乙醇等有机溶剂。苯甲酸在水中的溶解度如下:
某实验小组设计粗苯甲酸(含有少量NaCl和泥沙)的提纯方案如下:___________ 。
(2)操作Ⅱ名称是___________ 。操作Ⅱ目的是:___________ 。操作Ⅲ名称___________ 。
(3)步骤Ⅳ遵循“少量多次”的原则用冷水洗涤晶体,判断是否洗涤干净的实验方案是___________ 。
(4)测定产品的纯度
苯甲酸纯度的测定:称取1.00g苯甲酸产品,溶于烧杯中配成250mL溶液,移取25.00 mL溶液于锥形瓶中,加酚酞作指示剂,在不断摇动下用0.03mol/L NaOH标准溶液滴定至终点。平行测试3次,平均消耗 NaOH标准溶液22.50 mL。
①关于该实验的说法不正确 的是___________ 。
A.锥形瓶用蒸馏水洗净后需再用待测液润洗
B.选用干燥洁净的滴定管不用经待装液润洗即可使用
C.滴定时滴定管尖嘴内有气泡,滴定后无气泡,使得测定结果偏大
D.滴定终点时俯视读数,导致测定结果偏小
E.滴定时溶液由浅红色变无色,且30秒不复原,即可判断达到滴定终点
②计算该产品中苯甲酸的纯度是___________ %。(精确到小数点一位)
| 温度/℃ | 25 | 50 | 75 |
| 溶解度/g | 0.34 | 0.85 | 2.2 |

(2)操作Ⅱ名称是
(3)步骤Ⅳ遵循“少量多次”的原则用冷水洗涤晶体,判断是否洗涤干净的实验方案是
(4)测定产品的纯度
苯甲酸纯度的测定:称取1.00g苯甲酸产品,溶于烧杯中配成250mL溶液,移取25.00 mL溶液于锥形瓶中,加酚酞作指示剂,在不断摇动下用0.03mol/L NaOH标准溶液滴定至终点。平行测试3次,平均消耗 NaOH标准溶液22.50 mL。
①关于该实验的说法
A.锥形瓶用蒸馏水洗净后需再用待测液润洗
B.选用干燥洁净的滴定管不用经待装液润洗即可使用
C.滴定时滴定管尖嘴内有气泡,滴定后无气泡,使得测定结果偏大
D.滴定终点时俯视读数,导致测定结果偏小
E.滴定时溶液由浅红色变无色,且30秒不复原,即可判断达到滴定终点
②计算该产品中苯甲酸的纯度是
您最近一年使用:0次
名校
解题方法
9 . 下列离子方程式书写错误的是
| A.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:2Fe2++2H++H2O2=2Fe3++2H2O |
B.向AlCl3溶液中通入足量NH3:Al3+ + 4NH3 + 2H2O=AlO + 4NH + 4NH |
| C.氢氧化铜浊液中滴加氨水得到深蓝色溶液:Cu(OH)2 + 4NH3 = [Cu(NH3)4]2+ + 2OH- |
D.将铜丝插入足量浓硝酸中:Cu+4H++2NO =Cu2++2NO2↑+2H2O =Cu2++2NO2↑+2H2O |
您最近一年使用:0次
名校
解题方法
10 . 结晶水合物Fe(NO3)3·9H2O主要用作催化剂 某兴趣小组按如下流程进行实验:
某兴趣小组按如下流程进行实验:
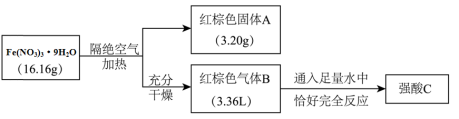
(1)混合气体B的成分为
(2)写出化合物Fe(NO3)3·9H2O隔绝空气加热分解生成A和B的化学反应方程式
(3)固体A溶于氢氰酸(弱酸,分子式为:HCN)溶液生成六配位阴离子,溶液显强酸性。写出该反应的离子方程式
(4)控制温度的条件下,加热FeCl3溶液所得固体成分为:Fe2O3或FeOCl或两者混合物(已知:FeOCl难溶于水,易溶于强酸),设计实验方案检验固体中有FeOCl:
您最近一年使用:0次



