解题方法
1 . 利用NaOH标准溶液滴定食醋中醋酸的浓度,下列操作正确的是
| A.锥形瓶洗净后需要用待测食醋润洗 |
| B.碱式滴定管用NaOH标准溶液润洗后,润洗液应从滴定管上口倒出 |
| C.滴定读数时,应双手一上一下持滴定管 |
| D.在使用前,若酸式滴定管旋塞处存在轻微漏水现象;可在旋塞处涂抹适量凡士林 |
您最近一年使用:0次
2 . 化学与生活、生产和社会息息相关,下列说法不正确的是
| A.聚合硫酸铁具有氧化性,可用于自来水杀菌消毒 |
B.将 溶液加热、蒸干、灼烧,可得到 溶液加热、蒸干、灼烧,可得到 固体 固体 |
C.牙膏中添加氟化物,可将 转化为更难溶的 转化为更难溶的 抵抗酸的侵蚀 抵抗酸的侵蚀 |
D.侯氏制碱法中将精制的饱和食盐水先氨化再碳酸化,以获得更多的 沉淀 沉淀 |
您最近一年使用:0次
3 . 杜甫诗句中“朱门酒肉臭,路有冻死骨”这里的“朱门”是指涂有_______的门。
A. | B. | C. | D. |
您最近一年使用:0次
解题方法
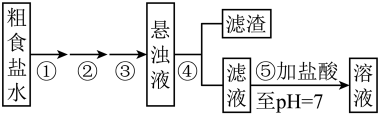
4 . 实验活动探究---食盐的精制
实验目的:从粗食盐水中除去
实验用品:
试剂:粗食盐水,稀盐酸,稀硫酸, 溶液,
溶液, 溶液,
溶液, 溶液,
溶液, 溶液
溶液
仪器:烧杯,漏斗,玻璃棒,表面皿, 试纸,滤纸,试管,胶头滴管,铁架台(带铁圈)
试纸,滤纸,试管,胶头滴管,铁架台(带铁圈)
实验操作流程: 离子,需加入过量的
离子,需加入过量的_______ ,写出①中反应的离子方程式_______ 。
(2)操作②加入过量的____ ,写出②中反应的离子方程式___ ;操作③加入过量的 溶液,除了除去
溶液,除了除去 ,还要除去操作①引入的杂质离子
,还要除去操作①引入的杂质离子______ 。
(3)操作④为_______ ,其中玻璃棒的作用是_______ 。
(4)操作⑤向滤液中滴加盐酸,用玻璃棒搅拌,直到_______ ,并用 试纸检验,使滤液呈中性或微酸性。
试纸检验,使滤液呈中性或微酸性。
(5)操作流程④与⑤可以颠倒顺序吗?_______ ,为什么?_______ 。
实验目的:从粗食盐水中除去

实验用品:
试剂:粗食盐水,稀盐酸,稀硫酸,
 溶液,
溶液, 溶液,
溶液, 溶液,
溶液, 溶液
溶液仪器:烧杯,漏斗,玻璃棒,表面皿,
 试纸,滤纸,试管,胶头滴管,铁架台(带铁圈)
试纸,滤纸,试管,胶头滴管,铁架台(带铁圈)实验操作流程:
 离子,需加入过量的
离子,需加入过量的(2)操作②加入过量的
 溶液,除了除去
溶液,除了除去 ,还要除去操作①引入的杂质离子
,还要除去操作①引入的杂质离子(3)操作④为
(4)操作⑤向滤液中滴加盐酸,用玻璃棒搅拌,直到
 试纸检验,使滤液呈中性或微酸性。
试纸检验,使滤液呈中性或微酸性。(5)操作流程④与⑤可以颠倒顺序吗?
您最近一年使用:0次
5 . 下列说法不正确的是
| A.铁元素在自然界中以化合态和游离态形式存在 |
B. 中铁的化合价有 中铁的化合价有 和 和 价,是一种混合物 价,是一种混合物 |
C.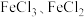 和 和 都可以通过化合反应制取 都可以通过化合反应制取 |
D. 铁与足量稀盐酸反应,转移电子数为 铁与足量稀盐酸反应,转移电子数为 |
您最近一年使用:0次
名校
6 . 硫元素代表物的价类二维图如图所示。下列说法正确的是
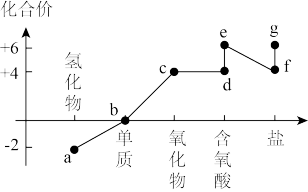

| A.物质混合可实现a+c→b,其中氧化产物与还原产物的比值为1:2 |
| B.常温下,附着在试管中的b可用CS2洗涤 |
| C.c与Cl2混合通入品红溶液,品红褪色速度更快 |
| D.浓e具有脱水性,可以用来做为部分气体的干燥剂 |
您最近一年使用:0次
7 . 下列反应图像中,符合题意的是
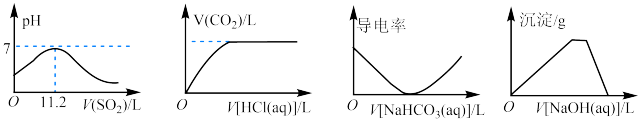

| A.向1L0.5mol·L-1H2S溶液中缓慢通入SO2(标准状况) |
| B.向纯碱溶液中缓慢滴加过量的盐酸 |
C.向 溶液中缓慢滴加NaHCO3溶液 溶液中缓慢滴加NaHCO3溶液 |
D.向 溶液中缓慢滴加NaOH溶液 溶液中缓慢滴加NaOH溶液 |
您最近一年使用:0次
8 . 卤素化合物在生产生活中应用广泛,回答下列问题
(1)研究表明 气体中存在单体和环状六聚体的平衡:
气体中存在单体和环状六聚体的平衡: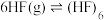 ,HF形成环状六聚体的作用力是
,HF形成环状六聚体的作用力是____________ ;在测定 相对分子质量的实验中,
相对分子质量的实验中,____________ (填“低压”或“高压”)有利于测定的准确性.
(2) 气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸
气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸 和氯酸钾
和氯酸钾 在酸性条件下制备
在酸性条件下制备 ,离子方程式为
,离子方程式为__________ ;产物中的另一种气体可以起到的作用是________________ .
(3) 与
与 以共价键形成
以共价键形成 ,其中
,其中________ 显负电性, 与水反应的方程式是
与水反应的方程式是____________ .
(4)利用 和浓磷酸制备
和浓磷酸制备 的原理是:
的原理是: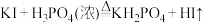 ,该反应中利用了浓磷酸的什么性质:
,该反应中利用了浓磷酸的什么性质:________ (“强酸性”“强氧化性”“高沸点”).
(1)研究表明
 气体中存在单体和环状六聚体的平衡:
气体中存在单体和环状六聚体的平衡: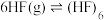 ,HF形成环状六聚体的作用力是
,HF形成环状六聚体的作用力是 相对分子质量的实验中,
相对分子质量的实验中,(2)
 气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸
气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸 和氯酸钾
和氯酸钾 在酸性条件下制备
在酸性条件下制备 ,离子方程式为
,离子方程式为(3)
 与
与 以共价键形成
以共价键形成 ,其中
,其中 与水反应的方程式是
与水反应的方程式是(4)利用
 和浓磷酸制备
和浓磷酸制备 的原理是:
的原理是: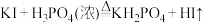 ,该反应中利用了浓磷酸的什么性质:
,该反应中利用了浓磷酸的什么性质:
您最近一年使用:0次
名校
解题方法
9 . 丙酮在HCl催化条件下发生溴化反应的化学方程式为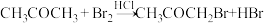 ,已知该反应的速率方程为
,已知该反应的速率方程为 ,其中k为与温度有关的常数。下列说法正确的是
,其中k为与温度有关的常数。下列说法正确的是
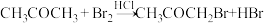 ,已知该反应的速率方程为
,已知该反应的速率方程为 ,其中k为与温度有关的常数。下列说法正确的是
,其中k为与温度有关的常数。下列说法正确的是| A.该反应为加成反应 | B.升高温度,k增大,化学反应速率加快 |
C.减小 ,化学反应速率减慢 ,化学反应速率减慢 | D.增大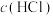 ,化学反应速率不变 ,化学反应速率不变 |
您最近一年使用:0次
2024-03-28更新
|
177次组卷
|
2卷引用:安徽省淮北市树人高级中学2023-2024学年上学期高二11月期中考试化学试题
解题方法
10 . 为了减缓温室效应,实现碳中和目标,可将 转化为甲醚、甲醇等产品.请回答问题:
转化为甲醚、甲醇等产品.请回答问题:
 与
与 制甲醚
制甲醚 的主要反应如下:
的主要反应如下:
I.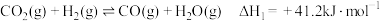
Ⅱ.
Ⅲ.
(1)总反应 的
的
__________ .
(2)若在体积恒定的密闭容器内发生上述反应,下列措施可提高总反应速率的是_________ .
a.加入催化剂 b.降低温度 c.充入惰性气体 d.同比例的增大 和
和 的投料
的投料
(3)密闭容器中充入 ,在
,在 条件下测得平衡时
条件下测得平衡时 转化率和
转化率和 选择性随温度的变化如图所示.
选择性随温度的变化如图所示. 选择性
选择性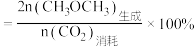
①表示 选择性的是曲线
选择性的是曲线___________ 填(“M”或“N”);
②温度高于 时,曲线N随温度升高而升高的原因是
时,曲线N随温度升高而升高的原因是_____________ ;
③为同时提高平衡时 转化率和
转化率和 选择性,应选择的反应条件为
选择性,应选择的反应条件为________ (填字母)
a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
④Q点温度下 的物质的量为
的物质的量为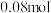 ,则该温度下反应Ⅲ的
,则该温度下反应Ⅲ的
________ .
(4)研究发现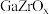 双金属氧化物对
双金属氧化物对 加氢制甲醇有良好的催化作用,反应机理如图所示,下列有关叙述正确的是
加氢制甲醇有良好的催化作用,反应机理如图所示,下列有关叙述正确的是__________ .
c.整个过程中, 元素的化合价未发生变化 d.机理图上中间体有三种
元素的化合价未发生变化 d.机理图上中间体有三种
 转化为甲醚、甲醇等产品.请回答问题:
转化为甲醚、甲醇等产品.请回答问题: 与
与 制甲醚
制甲醚 的主要反应如下:
的主要反应如下:I.
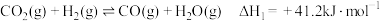
Ⅱ.

Ⅲ.

(1)总反应
 的
的
(2)若在体积恒定的密闭容器内发生上述反应,下列措施可提高总反应速率的是
a.加入催化剂 b.降低温度 c.充入惰性气体 d.同比例的增大
 和
和 的投料
的投料(3)密闭容器中充入
 ,在
,在 条件下测得平衡时
条件下测得平衡时 转化率和
转化率和 选择性随温度的变化如图所示.
选择性随温度的变化如图所示.
 选择性
选择性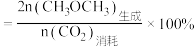
①表示
 选择性的是曲线
选择性的是曲线②温度高于
 时,曲线N随温度升高而升高的原因是
时,曲线N随温度升高而升高的原因是③为同时提高平衡时
 转化率和
转化率和 选择性,应选择的反应条件为
选择性,应选择的反应条件为a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
④Q点温度下
 的物质的量为
的物质的量为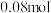 ,则该温度下反应Ⅲ的
,则该温度下反应Ⅲ的
(4)研究发现
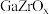 双金属氧化物对
双金属氧化物对 加氢制甲醇有良好的催化作用,反应机理如图所示,下列有关叙述正确的是
加氢制甲醇有良好的催化作用,反应机理如图所示,下列有关叙述正确的是

c.整个过程中,
 元素的化合价未发生变化 d.机理图上中间体有三种
元素的化合价未发生变化 d.机理图上中间体有三种
您最近一年使用:0次



