1 . I.有机工业中很多重要的化工原料都来源于石油化工,如图中的苯、丙烯有机物A等,其中A的产量可以用来衡量一个国家的石油化工发展水平。请回答下列问题:

(1)A的结构简式为____ ,C中官能团名称是____ 。
(2)下列说法正确的是____ 。
(3)写出B→CH3CHO反应方程式:____ 。
(4)戊烷是由石蜡油获得A的过程中的中间产物之一,它的某种同分异构体中一氯代物只有一种,写出该戊烷的结构简式:____ 。
II.分离提纯自然界矿石某些成份,然后制备有特殊性能物质是无机工业研究的一个重要方向,例如利用炼锌矿渣[主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4]可制得具有优异光电性能的氮化镓(GaN),部分工艺流程如图:

已知,金属离子在该工艺条件下的萃取率进入有机层中的金属离子百分数见表。
回答下列问题:
(5)ZnFe2O4可以写成ZnO•Fe2O3,“浸出”过程中ZnFe2O4发生反应的离子方程式为____ 。
(6)滤饼的主要成分是____ 、____ (填化学式),固体X最好选用____ (填化学式)。
(7)Ca与Al同主族,化学性质相似。“反萃取”后,溶液中镓元素的存在形式为____ (填离子符号)。

(1)A的结构简式为
(2)下列说法正确的是
| A.乙酸乙酯与丙烯酸乙酯属于同系物 |
| B.乙酸乙酯密度比水大,静置分液时沉在分液漏斗下层 |
| C.聚丙烯酸能够使酸性高锰酸钾溶液褪色 |
| D.制备硝基苯需要浓HNO3和浓H2SO4混合液,混合时应将H2SO4缓慢倒入到HNO3溶液中 |
(4)戊烷是由石蜡油获得A的过程中的中间产物之一,它的某种同分异构体中一氯代物只有一种,写出该戊烷的结构简式:
II.分离提纯自然界矿石某些成份,然后制备有特殊性能物质是无机工业研究的一个重要方向,例如利用炼锌矿渣[主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4]可制得具有优异光电性能的氮化镓(GaN),部分工艺流程如图:

已知,金属离子在该工艺条件下的萃取率进入有机层中的金属离子百分数见表。
| 金属离子 | Fe2+ | Fe3+ | Zn2+ | Ga3+ |
| 萃取率 | 0 | 99 | 0 | 97~98.5 |
(5)ZnFe2O4可以写成ZnO•Fe2O3,“浸出”过程中ZnFe2O4发生反应的离子方程式为
(6)滤饼的主要成分是
(7)Ca与Al同主族,化学性质相似。“反萃取”后,溶液中镓元素的存在形式为
您最近一年使用:0次
名校
2 . 由下列实验操作和现象得出的结论正确的是
选项 | 实验操作和现象 | 实验结论 |
A | 向久置的Na2SO3样品中加入HNO3酸化,再加入Ba(NO3)2溶液,产生白色沉淀 | Na2SO3样品已变质 |
B | 向足量KI溶液中加入几滴FeCl3溶液,充分反应,取两份反应后的溶液于试管中,分别加入几滴KSCN溶液和几滴淀粉溶液,溶液变为红色和蓝色 | Fe3+与I-的反应为可逆反应 |
C | 常温下,将Zn片和Zn粉分别加入1mol∙L-1的稀盐酸中,Zn粉反应产生气泡的速率比Zn片快 | 反应物浓度越大,反应速率越快 |
D | 向品红溶液中通入气体X后,品红溶液褪色 | 气体X一定为SO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 下列实验操作所得的实验现象及结论均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将少量Na2SO3样品溶于水,滴加足量盐酸酸化的Ba(NO3)2溶液 | 有白色沉淀产生 | 说明Na2SO3已变质 |
| B | 镁、铝为电极,氢氧化钠为电解质的原电池装置 | 铝表面有气泡 | 金属活动性:Mg>Al |
| C | 将某气体通入品红溶液中 | 溶液褪色 | 该气体一定是SO2 |
| D | 将10mL2mol/L的KI溶液与1mL1mol/LFeCl3溶液混合 | 充分反应后,滴加数滴KSCN溶液,溶液颜色变红 | 该反应为可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-21更新
|
282次组卷
|
3卷引用:江西省丰城中学2022-2023学年高一下学期期末考试化学试题
解题方法
4 . 高铁酸钾(K2FeO4)是一新型、高效、无毒的多功能水处理剂。K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定;Fe3+ 遇KSCN溶液显红色。
(1)制备K2FeO4。
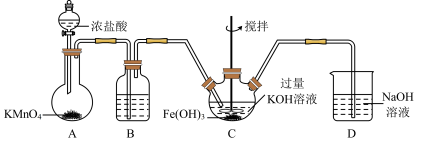
①C为制备K2FeO4装置,KOH溶液过量的原因是_______ 。
②D为尾气处理装置,发生反应的离子方程式为_______ 。
(2)探究K2FeO4的性质。取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计以下方案:
①由方案I中溶液变红可知a中含有_______ 。该离子的产生_______ (填“能”或“不能”)判断一定是由K2FeO4被Cl-还原而形成的。
②方案Ⅱ得出氧化性:Cl2_______  (填“>”或“<”)
(填“>”或“<”)
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下,配平及完成上述离子方程式_______ 。
_______ +_______H+=_______O2↑+_______ Fe3++_______
+_______H+=_______O2↑+_______ Fe3++_______
现取C中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况下)。则样品中高铁酸钾的质量分数约为_______ 。(计算结果保留到0.1%)
(1)制备K2FeO4。

①C为制备K2FeO4装置,KOH溶液过量的原因是
②D为尾气处理装置,发生反应的离子方程式为
(2)探究K2FeO4的性质。取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计以下方案:
| 方案I | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b.取少量b,滴加盐酸,有Cl2产生。 |
②方案Ⅱ得出氧化性:Cl2
 (填“>”或“<”)
(填“>”或“<”)(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下,配平及完成上述离子方程式
_______
 +_______H+=_______O2↑+_______ Fe3++_______
+_______H+=_______O2↑+_______ Fe3++_______现取C中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况下)。则样品中高铁酸钾的质量分数约为
您最近一年使用:0次
解题方法
5 . 下列操作、现象和结论都正确的是
| 选项 | 操作及现象 | 结论 |
| A | 在FeCl₂溶液中滴加KSCN溶液,溶液变红色 | FeCl₂已变质 |
| B | 在碳酸氢钠溶液中滴加澄清石灰水,产生白色沉淀 | NaHCO₃样品中含有Na₂CO₃ |
| C | 在高锰酸钾粉末中加入浓盐酸,产生黄绿色气体 | 氧化性:KMnO₄<Cl2 |
| D | 在AlCl₃溶液中滴加过量的氨水,产生白色沉淀 | Al(OH)₃不与NH₃·H₂O反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列实验操作、现象及所得实验结论均正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 铁加入到冷的浓硝酸中无明显现象,加入稀硝酸中有气泡产生 | 氧化性:稀硝酸>浓硝酸 |
| B | 将亚硫酸钠样品溶于水,加入盐酸酸化的 溶液有白色沉淀产生 溶液有白色沉淀产生 | 样品已变质 |
| C | 向某溶液中加烧碱溶液,微热,产生使湿润红色石蕊试纸变蓝的气体 | 溶液可能为铵盐溶液 |
| D | 将少量新制氯水滴到蓝色石蕊试纸上,试纸先变红后褪色 | 氯水显酸性, 有漂白性 有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-03更新
|
179次组卷
|
2卷引用:江西省南昌市第十中学2022—2023学年高一下学期第一次月考化学试题
7 . 下列有关实验的现象和结论都正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向装有1-2g过氧化钠固体的试管中加入2mL水,再滴加几滴酚酞试液 | 产生大量气泡,滴加酚酞后溶液变红 | 反应产生气体,同时生成碱性物质 |
| B | 取未知溶液少量于试管中,滴加几滴高锰酸钾溶液 | 高锰酸钾溶液紫色褪去 | 无法证明未知溶液中含有Fe2+ |
| C | 将少量硝酸亚铁样品溶于稀硫酸,再滴加几滴硫氰化钾溶液 | 溶液变成红色 | 原硝酸亚铁样品已变质 |
| D | 向装有2mL新制氯水的试管中滴加几滴紫色石蕊试液 | 溶液先变红后褪色 | 氯水既有酸性又有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-07更新
|
124次组卷
|
2卷引用:江西省宜春市铜鼓中学2022-2023学年高一下学期开学考试化学试题
8 . 下列操作、现象和结论都正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 蘸取某样品做焰色试验 | 焰色呈黄色 | 样品只含钠元素,不含钾元素 |
| B | 向盐酸中加入少量白色粉末R | 产生大量气泡 | 白色粉末R可能是碳酸盐 |
| C | 将新制的氯水滴在pH试纸上 | 试纸只变红色 | 氯水呈酸性 |
| D | 在少量烧碱粉末中滴加稀硫酸 | 产生气泡 | 烧碱已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列实验方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究反应物浓度对化学反应速率的影响 | 分别取10mL 0.1mol·Lˉ1Na2S2O3溶液和5mL 0.1mol·Lˉ1Na2S2O3溶液、5mL蒸馏水于两支试管中,然后同时加入10mL 0.1mol·Lˉ1H2SO4溶液 | 前者出现浑浊的时间更短,说明增大Na2S2O3浓度,可以加快反应速率 |
| B | 探究压强对化学反应速率的影响 | 在容积不变的密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g),向其中通入氩气,反应速率不变 2NH3(g),向其中通入氩气,反应速率不变 | 化学反应速率不受压强影响 |
| C | 检验Fe(NO3)2晶体是否氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 | 若溶液变红,则Fe(NO3)2晶体已氧化变质 |
| D | 研究淀粉的水解程度 | 取0.5g淀粉于试管中,加入适量20%的硫酸溶液后沸水浴加热5min,再滴加过量氢氧化钠溶液,再加入适量碘水 | 若溶液没有变成蓝色,则淀粉已经水解完全 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-14更新
|
417次组卷
|
3卷引用:江西省丰城拖船中学2022-2023学年高一下学期期末考试化学试题
名校
10 . 过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如图实验。
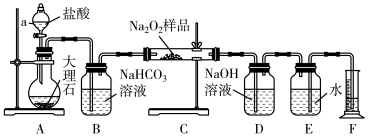
(1)探究一包Na2O2样品是否已经变质:取少量样品,将其溶解,加入_______ 溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并利用如图装置来测定过氧化钠的质量分数。
①装置中仪器a的名称是_______ ,装置D的作用是_______ 。
②将仪器连接好以后,必须进行的第一步操作是_______ 。
③写出装置C中发生主要反应的化学方程式:_______ 。
④反应结束后,在读取实验中生成气体的体积时,你认为合理的是_______ (填字母序号)。
a.读取气体体积前,需冷却到室温
b.调整量筒使E、F内液面高度相同
c.视线与凹液面的最低处相平时读取量筒中水的体积

(1)探究一包Na2O2样品是否已经变质:取少量样品,将其溶解,加入
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并利用如图装置来测定过氧化钠的质量分数。
①装置中仪器a的名称是
②将仪器连接好以后,必须进行的第一步操作是
③写出装置C中发生主要反应的化学方程式:
④反应结束后,在读取实验中生成气体的体积时,你认为合理的是
a.读取气体体积前,需冷却到室温
b.调整量筒使E、F内液面高度相同
c.视线与凹液面的最低处相平时读取量筒中水的体积
您最近一年使用:0次
2022-03-07更新
|
176次组卷
|
3卷引用:江西省上饶市铅山县第一中学2021-2022年高一上学期期中考试化学试题



