名校
1 . 工业上可以用 来生产甲醇燃料。在体积为2L的密闭容器中,充入
来生产甲醇燃料。在体积为2L的密闭容器中,充入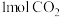 和3 mol H2,一定条件下发生反应
和3 mol H2,一定条件下发生反应 。测得
。测得 和
和 的物质的量随时间变化如图所示。下列描述正确的是
的物质的量随时间变化如图所示。下列描述正确的是
 来生产甲醇燃料。在体积为2L的密闭容器中,充入
来生产甲醇燃料。在体积为2L的密闭容器中,充入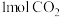 和3 mol H2,一定条件下发生反应
和3 mol H2,一定条件下发生反应 。测得
。测得 和
和 的物质的量随时间变化如图所示。下列描述正确的是
的物质的量随时间变化如图所示。下列描述正确的是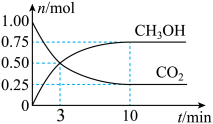
A.达到平衡时, 的转化率为75% 的转化率为75% |
| B.3 min时,达到了化学平衡状态 |
| C.反应进行到10 min时,气体的总压强是开始的0.625倍 |
D.反应开始到10 min时,用 表示的反应速率为0.0375 表示的反应速率为0.0375  |
您最近一年使用:0次
名校
2 . 与无机化合物相比,有机化合物的组成元素并不复杂,但化合物数量众多,性质各异。烃类物质是整个有机化学的基础,请根据要求完成下列问题。
(1)2023年7月12日,装配我国完全自主研发、具备自主知识产权的液氧甲烷低温发动机的朱雀二号运载火箭发射成功。甲烷的空间构型为___________ ,下列最能体现其真实结构的是___________
a.结构式 b.电子式 c.球棍模型 d.空间填充模型
(2)1 mol CH4与氯气发生取代反应,待反应完全后,测得四种产物的物质的量相等,其中俗称氯仿的产物是___________ (写化学式),消耗氯气的物质的量是___________ 。
(3)0.1 mol某烷烃完全燃烧,燃烧产物依次通过浓硫酸、浓NaOH溶液,实验结束后,称得浓硫酸增重10.8 g,浓NaOH溶液增重22 g。则该烷烃的化学式为___________ ,其中一氯代物只有一种的结构简式:___________ 。
(1)2023年7月12日,装配我国完全自主研发、具备自主知识产权的液氧甲烷低温发动机的朱雀二号运载火箭发射成功。甲烷的空间构型为
a.结构式 b.电子式 c.球棍模型 d.空间填充模型
(2)1 mol CH4与氯气发生取代反应,待反应完全后,测得四种产物的物质的量相等,其中俗称氯仿的产物是
(3)0.1 mol某烷烃完全燃烧,燃烧产物依次通过浓硫酸、浓NaOH溶液,实验结束后,称得浓硫酸增重10.8 g,浓NaOH溶液增重22 g。则该烷烃的化学式为
您最近一年使用:0次
名校
3 . 肼(N2H4)燃料电池是一种理想的电池,产物无污染,其工作原理如图所示,下列叙述正确的是
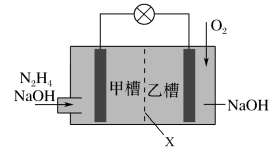
A.当消耗 时,负极生成1mol气体 时,负极生成1mol气体 | B.电池工作时,负极的pH升高 |
C.正极反应为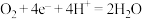 | D.X最好用阳离子交换膜 |
您最近一年使用:0次
名校
4 . 某实验小组用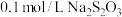 溶液和
溶液和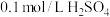 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
已知:实验结果: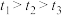 。回答下列问题:
。回答下列问题:
(1)a=___________ ml。
(2)写出Na2S2O3溶液和H2SO4溶液反应的离子方程式:___________ 。
(3)对比实验I、III可知,___________ 能加快反应速率。
(4)进行实验I、II时,依次向试管中加入Na2S2O3溶液、___________ 、___________ ,两者的顺序不可颠倒,理由是:___________ 。
(5)经查阅资料,构成原电池也能加快反应速率。某小组用一定的锌与足量的0.1 mol/L H2SO4溶液反应,下列物质即能加快反应速率,又不影响生成气体量的是:___________
a.适当升温 b.滴加几滴0.15 mol/LHCl c.滴加几滴 溶液
溶液
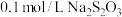 溶液和
溶液和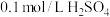 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。| 实验序号 | 温度/℃ | Na2S2O3溶液体积/mL | H2SO4溶液体积/mL | H2O体积/mL | 出现沉淀所需的时间/s |
| I | 20 | 5.0 | 5.0 | 10.0 | t1 |
| II | 20 | 5.0 | 10.0 | a | t2 |
| III | 60 | 5.0 | 5.0 | 10.0 | t3 |
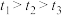 。回答下列问题:
。回答下列问题:(1)a=
(2)写出Na2S2O3溶液和H2SO4溶液反应的离子方程式:
(3)对比实验I、III可知,
(4)进行实验I、II时,依次向试管中加入Na2S2O3溶液、
(5)经查阅资料,构成原电池也能加快反应速率。某小组用一定的锌与足量的0.1 mol/L H2SO4溶液反应,下列物质即能加快反应速率,又不影响生成气体量的是:
a.适当升温 b.滴加几滴0.15 mol/LHCl c.滴加几滴
 溶液
溶液
您最近一年使用:0次
名校
5 . 向含有0.01 mol Cu,amol Cu2O、bmol CuO的混合物中滴加6 mol/L的稀硝酸溶液至10 mL时,固体恰好完全溶解,得到标准状况下224 mL气体(纯净物)。下列说法不正确的是
| A.反应过程中转移0.03 mol电子 | B.a∶b=1∶1 |
| C.等量上述稀硝酸中最多能溶解0.84 g Fe | D.被还原的硝酸为0.01 mol |
您最近一年使用:0次
6 . 下列说法正确的是
A.向NaHSO3溶液中滴加氢硫酸,产生淡黄色沉淀,证明 具有氧化性 具有氧化性 |
| B.加热浓硫酸与NaCl固体的混合物可制备HCl,说明浓硫酸酸性强于HCl |
| C.将CO2通入Ba(NO3)2,溶液无明显现象,则将SO2通入Ba(NO3)2溶液也无明显现象 |
| D.向浓HNO3中插入红热的炭,产生红棕色气体,证明炭可与浓HNO3反应生成NO2 |
您最近一年使用:0次
7 . 锰是生产各种合金的重要元素。工业上以含锰矿石(主要成分为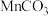 ,还含有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
,还含有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
回答下列问题:
(1)用硫酸浸取含锰矿石时,提高浸取速率的方法有_______ (写两种)。
(2)“氧化”步骤发生反应的离子方程式为_______ 。
(3)滤渣1的主要成分是___ ,实验室中为了加快固液混合物的分离,常采用的操作是___ 。
(4)当溶液中可溶组分浓度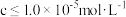 时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少为
时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少为____ (已知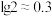 )。
)。
(5)“除杂3”步骤所得溶液中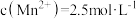 ,则其
,则其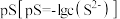 的范围是
的范围是____ 。
(6)电解废液中还含有少量 ,向其中加入饱和
,向其中加入饱和 溶液,有沉淀和气体生成,该反应的离子方程式为
溶液,有沉淀和气体生成,该反应的离子方程式为_______ 。
 ,还含有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
,还含有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下: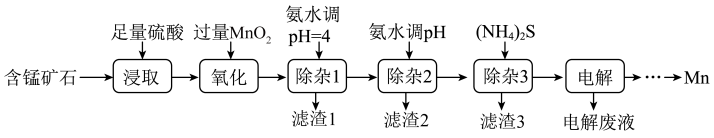
| 物质 |  |  |  | MnS | CoS |
 |  |  |  | 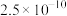 | 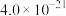 |
(1)用硫酸浸取含锰矿石时,提高浸取速率的方法有
(2)“氧化”步骤发生反应的离子方程式为
(3)滤渣1的主要成分是
(4)当溶液中可溶组分浓度
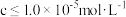 时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少为
时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少为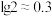 )。
)。(5)“除杂3”步骤所得溶液中
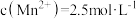 ,则其
,则其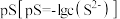 的范围是
的范围是(6)电解废液中还含有少量
 ,向其中加入饱和
,向其中加入饱和 溶液,有沉淀和气体生成,该反应的离子方程式为
溶液,有沉淀和气体生成,该反应的离子方程式为
您最近一年使用:0次
8 . 3′- (
(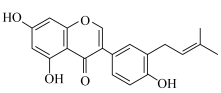 )是从大豆中分离出来的新型异戊烯基异黄酮,具有重要的生物防御活性,其合成路线如下。
)是从大豆中分离出来的新型异戊烯基异黄酮,具有重要的生物防御活性,其合成路线如下。
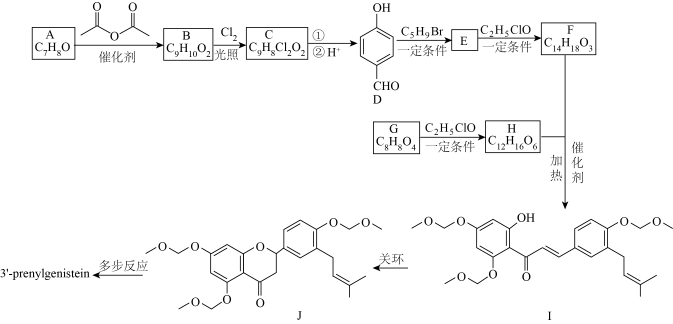
(2)C中官能团的名称为
(3)G→H的化学方程式是
(4)在B的同分异构体中,同时满足下列条件的共有
①含有苯环且只有一个侧链;②含有手性碳;③能发生银镜反应;
(5)化合物3′-
 的另一种合成路线如下:
的另一种合成路线如下: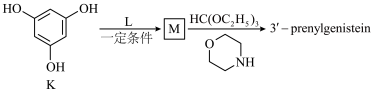
已知:①
②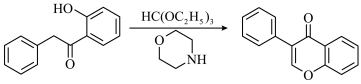
您最近一年使用:0次
名校
9 .  催化还原NO,其中一种催化机理如右图所示。下列说法错误的是
催化还原NO,其中一种催化机理如右图所示。下列说法错误的是
 催化还原NO,其中一种催化机理如右图所示。下列说法错误的是
催化还原NO,其中一种催化机理如右图所示。下列说法错误的是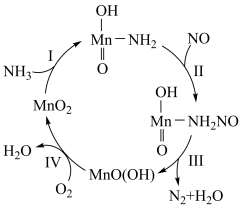
| A.反应过程中有极性键的断裂和生成 |
| B.Ⅰ、Ⅱ发生的是氧化还原反应 |
C. 是催化剂且在反应过程中化合价发生了变化 是催化剂且在反应过程中化合价发生了变化 |
D.该过程总反应为: |
您最近一年使用:0次
2024-04-29更新
|
105次组卷
|
2卷引用:山东省聊城市2023-2024学年高一下学期4月期中考试化学试题
10 . 若将铜丝插入热浓硫酸中进行如图(a-d均为没有相应试液的棉花)所示的探究实验,下列分析不正确的是

| A.Cu能与浓硫酸反应,说明浓硫酸具有强氧化性 |
| B.a处变红,说明SO2是酸性氧化物 |
| C.b或c处褪色,均说明SO2具有漂白性 |
| D.试管底部出现白色固体,体现了浓硫酸的吸水性 |
您最近一年使用:0次
2024-02-19更新
|
934次组卷
|
6卷引用:山东省聊城颐中外国语学校2023-2024学年高一下学期第一次质量检测化学试题
山东省聊城颐中外国语学校2023-2024学年高一下学期第一次质量检测化学试题福建省师范大学附属中学2023-2024学年高一上学期期末考试化学试题(已下线)专题01 硫及其化合物(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)四川省成都市简阳实验学校2023-2024学年高一下学期3月月考化学试题重点 天津市第五中学2023-2024学年高一下学期4月期中考试化学试题海南省儋州市第二中学2023-2024学年高一下学期期中考试化学试题



