解题方法
1 . 已知 是难溶于水、可溶于酸的盐。常温下用HCl调节
是难溶于水、可溶于酸的盐。常温下用HCl调节 浊液的pH,测得体系中
浊液的pH,测得体系中 (X为
(X为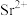 或
或 )与
)与 的关系如图。下列说法错误的是
的关系如图。下列说法错误的是
 是难溶于水、可溶于酸的盐。常温下用HCl调节
是难溶于水、可溶于酸的盐。常温下用HCl调节 浊液的pH,测得体系中
浊液的pH,测得体系中 (X为
(X为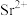 或
或 )与
)与 的关系如图。下列说法错误的是
的关系如图。下列说法错误的是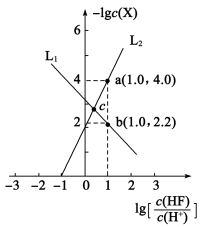
A. 代表 代表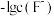 与 与 的变化曲线 的变化曲线 |
B. 的数量级为 的数量级为 |
C.a点, |
D.c点,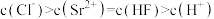 |
您最近一年使用:0次
2 . 丙烯可以在催化剂作用下由丙烷直接脱氢制备: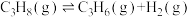
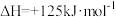 。若总压恒定为100kPa,向密闭容器中通入
。若总压恒定为100kPa,向密闭容器中通入 和
和 的混合气体(
的混合气体( 不参与反应),
不参与反应), 时,
时, 的平衡转化率与通入气体中
的平衡转化率与通入气体中 物质的量分数的关系如图。下列说法正确的是
物质的量分数的关系如图。下列说法正确的是
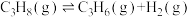
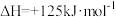 。若总压恒定为100kPa,向密闭容器中通入
。若总压恒定为100kPa,向密闭容器中通入 和
和 的混合气体(
的混合气体( 不参与反应),
不参与反应), 时,
时, 的平衡转化率与通入气体中
的平衡转化率与通入气体中 物质的量分数的关系如图。下列说法正确的是
物质的量分数的关系如图。下列说法正确的是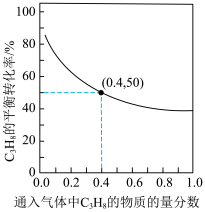
| A.当混合气体密度不随时间变化时,该反应达到化学平衡状态 |
B.平衡后,通入 可提高 可提高 的平衡转化率 的平衡转化率 |
| C.选择高效催化剂可提高丙烷的脱氢速率和丙烯的平衡产率 |
D. 时,丙烷脱氢反应的平衡常数 时,丙烷脱氢反应的平衡常数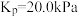 (用平衡分压代替平衡浓度,分压 (用平衡分压代替平衡浓度,分压 总压 总压 物质的量分数) 物质的量分数) |
您最近一年使用:0次
解题方法
3 . 室温下,用含少量 的
的 溶液制备
溶液制备 的过程如图。下列说法正确的是
的过程如图。下列说法正确的是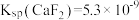 ,
,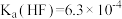 ;
;
②当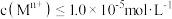 ,可认为
,可认为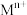 离子沉淀完全。
离子沉淀完全。
 的
的 溶液制备
溶液制备 的过程如图。下列说法正确的是
的过程如图。下列说法正确的是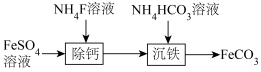
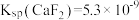 ,
,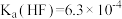 ;
;②当
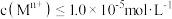 ,可认为
,可认为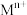 离子沉淀完全。
离子沉淀完全。A.配制 溶液时需加盐酸抑制 溶液时需加盐酸抑制 水解 水解 |
B. 溶液中: 溶液中: |
C.为确保 沉淀完全,除钙后的溶液中氟离子浓度至少为 沉淀完全,除钙后的溶液中氟离子浓度至少为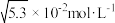 |
D.“沉铁”时发生反应的离子方程式: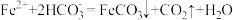 |
您最近一年使用:0次
解题方法
4 . 一定条件下
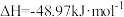 。向2L恒温恒容密闭容器中充入1mol
。向2L恒温恒容密闭容器中充入1mol 和3mol
和3mol ,在两种不同催化剂作用下建立平衡,
,在两种不同催化剂作用下建立平衡, 的转化率
的转化率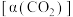 随时间
随时间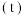 的变化曲线如图。下列说法错误的是
的变化曲线如图。下列说法错误的是

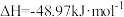 。向2L恒温恒容密闭容器中充入1mol
。向2L恒温恒容密闭容器中充入1mol 和3mol
和3mol ,在两种不同催化剂作用下建立平衡,
,在两种不同催化剂作用下建立平衡, 的转化率
的转化率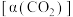 随时间
随时间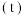 的变化曲线如图。下列说法错误的是
的变化曲线如图。下列说法错误的是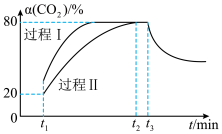
| A.该反应的活化能:过程Ⅱ>过程Ⅰ |
B.过程Ⅰ, 时刻改变的反应条件可能是升高温度 时刻改变的反应条件可能是升高温度 |
C.过程Ⅱ, 时段的化学反应速率 时段的化学反应速率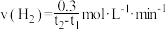 |
D.过程Ⅱ, 时刻向容器中再充入1mol 时刻向容器中再充入1mol 和3mol 和3mol ,平衡后 ,平衡后 的转化率大于80% 的转化率大于80% |
您最近一年使用:0次
名校
解题方法
5 . 某化学小组探究外界条件对化学反应速率的影响及其原因。
【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
(1)根据表中的实验数据,可以得到的结论是_______ 。
(2)利用实验1中数据计算,用KMnO4溶液的浓度变化表示的反应速率为v(KMnO4)=______ mol•L-1•min-1。
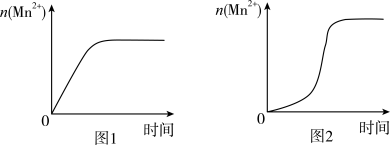
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示,但是实验过程中n(Mn2+)随时间变化的趋势应如图2所示。______ 。
②若提出的假设成立,应观察到的现象是_______ 。
(4)浓度增大反应速率加快的原因是______ (填字母,下同),催化剂使反应速率加快的原因是_______ 。
a.单位体积内活化分子数增多,单位时间内有效碰撞次数增加
b.使分子能量升高,提高了活化分子百分数,单位时间内有效碰撞次数增加
c.降低了反应的活化能,提高了活化分子百分数,单位时间内有效碰撞次数增加
【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6mol/LH2C2O4溶液 | H2O | 0.2mol/LKMnO4溶液 | 3mol/L稀硫酸 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
(1)根据表中的实验数据,可以得到的结论是
(2)利用实验1中数据计算,用KMnO4溶液的浓度变化表示的反应速率为v(KMnO4)=
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示,但是实验过程中n(Mn2+)随时间变化的趋势应如图2所示。
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6mol/LH2C2O4溶液 | H2O | 0.2mol/LKMnO4溶液 | 3mol/L稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | t | |
(4)浓度增大反应速率加快的原因是
a.单位体积内活化分子数增多,单位时间内有效碰撞次数增加
b.使分子能量升高,提高了活化分子百分数,单位时间内有效碰撞次数增加
c.降低了反应的活化能,提高了活化分子百分数,单位时间内有效碰撞次数增加
您最近一年使用:0次
6 . 短周期主族元素X、Y、Z、Q的原子序数依次增大。基态X原子最高能级有3个未成对电子;基态Y原子的最外层电子数为内层电子数的3倍;基态Z原子的第一电离能高于同周期相邻元素;基态Q原子的价电子,在不同形状的原子轨道中运动的电子数相等。下列说法错误的是
A.原子半径: | B.元素的电负性: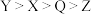 |
C.简单氢化物的熔点: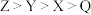 | D.X和Y的单质分子均为非极性分子 |
您最近一年使用:0次
7 . 我国某科研团队提出用多孔泡沫铁、高度膨化的纳米泡沫碳和添加 的
的 溶液构建独特的“摇椅式”全铁离子电池,电池结构如图(阴离子未标出)。
溶液构建独特的“摇椅式”全铁离子电池,电池结构如图(阴离子未标出)。
 的
的 溶液构建独特的“摇椅式”全铁离子电池,电池结构如图(阴离子未标出)。
溶液构建独特的“摇椅式”全铁离子电池,电池结构如图(阴离子未标出)。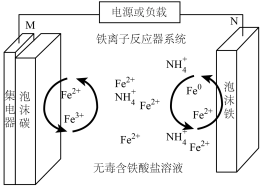
| A.放电时,N的电极电势高于M |
B.充电时,泡沫铁上发生的电极反应为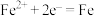 |
C.充电时,每转移 ,参与反应的物质中铁元素总质量为 ,参与反应的物质中铁元素总质量为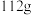 |
D.为提高电池效率,可用 代替 代替 |
您最近一年使用:0次
8 . 某 和
和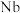 形成的金属化合物的立方晶胞结构如下。
形成的金属化合物的立方晶胞结构如下。
 和
和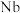 形成的金属化合物的立方晶胞结构如下。
形成的金属化合物的立方晶胞结构如下。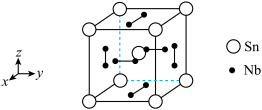
| A.该晶体属于金属晶体 |
B. 周围距离最近的 周围距离最近的 原子个数为6 原子个数为6 |
| C.该晶胞沿x轴、z轴的投影图完全相同 |
| D.该晶体在高温时导电能力更强 |
您最近一年使用:0次
9 . 邻羟基苯甲酸乙酯(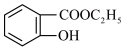 )广泛应用于有机合成,还可用作食品香料、工业溶剂等,其制备原理为
)广泛应用于有机合成,还可用作食品香料、工业溶剂等,其制备原理为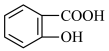 +CH3CH2OH
+CH3CH2OH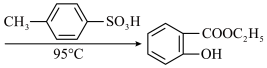 +H2O。下列说法错误的是
+H2O。下列说法错误的是
| A.加热方式可采用电加热套加热 |
B.可用饱和 溶液洗涤反应后的混合液 溶液洗涤反应后的混合液 |
| C.洗涤后所得粗品可用碱石灰干燥 |
D.酸性: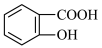 > >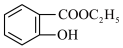 >CH3CH2OH >CH3CH2OH |
您最近一年使用:0次
解题方法
10 . 科学探究与创新意识是化学学科核心素养之一,回答下列问题:
I.某研究性学习小组欲探究原电池的形成条件,按如图所示装置进行实验并得到下表实验结果。
(1)实验①的导线中电子流向为___________ (填“A→B”或“B→A”)。
(2)实验④的导线中电流由A极流向B极,表明负极是___________ 电极(填元素名称),正极反应式为___________ 。
(3)分析上表有关信息,下列说法错误的是___________ (填标号)。
a.烧杯中的液体必须是电解质溶液
b.相对活泼的金属一定做负极
c.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
II.化学电源在日常生活中有着广泛的应用。
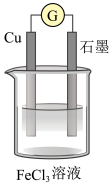
(4)将石墨和铜片用导线及电流计相连浸入500 mLFeCl3溶液中,构成如图所示的原电池装置,正极发生的电极反应式为___________ ;该电池在工作时,Cu的质量将___________ (填“增加”、“减少”或“不变”)。
(5)研究人员发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,电池的总反应方程式为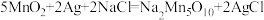 。
。___________ 。
②外电路每通过4mol电子时,生成Na2Mn5O10的物质的量是___________ mol。
I.某研究性学习小组欲探究原电池的形成条件,按如图所示装置进行实验并得到下表实验结果。
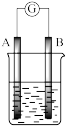
| 实验序号 | A | B | 烧杯中的液体 | 灵敏电流计指针是否偏转 |
| ① | Fe | Cu | 稀硫酸 | 有 |
| ② | Fe | Fe | 稀硫酸 | 无 |
| ③ | Fe | Cu | 苯 | 无 |
| ④ | Fe | Cu | 浓硝酸 | 有 |
| ⑤ | C | Fe | 氯化钠溶液 | 有 |
(1)实验①的导线中电子流向为
(2)实验④的导线中电流由A极流向B极,表明负极是
(3)分析上表有关信息,下列说法错误的是
a.烧杯中的液体必须是电解质溶液
b.相对活泼的金属一定做负极
c.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
II.化学电源在日常生活中有着广泛的应用。
(4)将石墨和铜片用导线及电流计相连浸入500 mLFeCl3溶液中,构成如图所示的原电池装置,正极发生的电极反应式为
(5)研究人员发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,电池的总反应方程式为
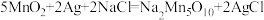 。
。
②外电路每通过4mol电子时,生成Na2Mn5O10的物质的量是
您最近一年使用:0次



