1 . 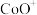 与
与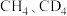 反应能高选择性地生成甲醇(氢元素有H、D、
反应能高选择性地生成甲醇(氢元素有H、D、 三种同位素,直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢),体系的能量随反应进程的变化如图所示(两者历程相似)。下列分析错误的是
三种同位素,直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢),体系的能量随反应进程的变化如图所示(两者历程相似)。下列分析错误的是
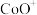 与
与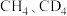 反应能高选择性地生成甲醇(氢元素有H、D、
反应能高选择性地生成甲醇(氢元素有H、D、 三种同位素,直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢),体系的能量随反应进程的变化如图所示(两者历程相似)。下列分析错误的是
三种同位素,直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢),体系的能量随反应进程的变化如图所示(两者历程相似)。下列分析错误的是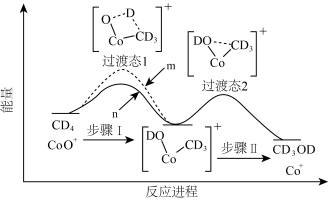
A.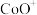 与 与 反应的能量变化应为曲线 反应的能量变化应为曲线 |
| B.步骤I既涉及碳氢键的断裂也涉及氧氢键的形成 |
C.若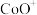 与 与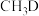 反应,可能生成 反应,可能生成 和 和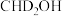 三种氚代甲醇 三种氚代甲醇 |
D.若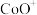 与 与 反应,相同时间内氚代甲醇的产量: 反应,相同时间内氚代甲醇的产量: |
您最近一年使用:0次
2 . 恒容密闭容器中进行反应: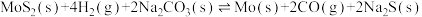
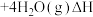 。平衡时正逆反应的平衡常数和平衡时气体浓度与温度的关系分别如图1和图2所示。下列说法正确的是
。平衡时正逆反应的平衡常数和平衡时气体浓度与温度的关系分别如图1和图2所示。下列说法正确的是
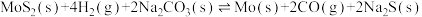
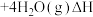 。平衡时正逆反应的平衡常数和平衡时气体浓度与温度的关系分别如图1和图2所示。下列说法正确的是
。平衡时正逆反应的平衡常数和平衡时气体浓度与温度的关系分别如图1和图2所示。下列说法正确的是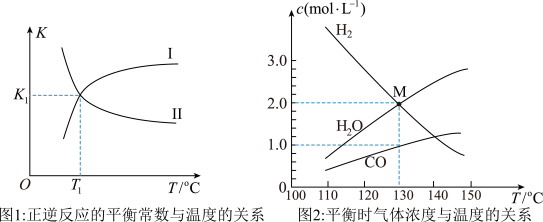
| A.曲线I代表的是K逆,曲线Ⅱ代表的是K正,T1为130 |
| B.该反应在任何温度下均可以自发进行 |
C.其他条件不变,增大 的浓度和增大压强均能提高 的浓度和增大压强均能提高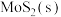 的平衡转化率 的平衡转化率 |
D.若M点对应温度下体系总压强为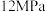 ,则该温度下 ,则该温度下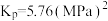 |
您最近一年使用:0次
3 . 阅读下列材料,完成下面小题。
碳酸钠俗称纯碱,是一种重要的化工原料。工业制备的碳酸钠产品中通常含有少量碳酸氢钠,某兴趣小组测定磞酸钠中碳酸氢钠含量的实验步骤如下:
步骤一:称取产品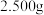 ,用蒸馏水溶解,定容于
,用蒸馏水溶解,定容于 容量瓶中;
容量瓶中;
步骤二:移取 上述溶液于锥形瓶,加入2滴指示剂
上述溶液于锥形瓶,加入2滴指示剂 ,用
,用 盐酸标准溶液滴定至终点(第一滴定终点),消耗盐酸
盐酸标准溶液滴定至终点(第一滴定终点),消耗盐酸 ;
;
步骤三:在上述锥形瓶中再加入2滴指示剂 ,继续用
,继续用 盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸
盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸 ;
;
平行测定三次, 平均值为22.45,
平均值为22.45, 平均值为23.51。
平均值为23.51。
1.下列关于滴定分析的操作,正确的是
2.下列有关上述实验或滴定管的描述错误的是
3.下列有关实验数据及误差分析错误的是
碳酸钠俗称纯碱,是一种重要的化工原料。工业制备的碳酸钠产品中通常含有少量碳酸氢钠,某兴趣小组测定磞酸钠中碳酸氢钠含量的实验步骤如下:
步骤一:称取产品
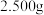 ,用蒸馏水溶解,定容于
,用蒸馏水溶解,定容于 容量瓶中;
容量瓶中;步骤二:移取
 上述溶液于锥形瓶,加入2滴指示剂
上述溶液于锥形瓶,加入2滴指示剂 ,用
,用 盐酸标准溶液滴定至终点(第一滴定终点),消耗盐酸
盐酸标准溶液滴定至终点(第一滴定终点),消耗盐酸 ;
;步骤三:在上述锥形瓶中再加入2滴指示剂
 ,继续用
,继续用 盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸
盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸 ;
;平行测定三次,
 平均值为22.45,
平均值为22.45, 平均值为23.51。
平均值为23.51。1.下列关于滴定分析的操作,正确的是
| A.滴定时应一直观察滴定管中溶液体积的变化 |
| B.平行滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以上某固定位置 |
| C.滴定时自始至终应匀速滴加 |
| D.读数时应捏住滴定管上端无刻度处,使管保持垂直 |
A.指示剂M可能为酚酞, 可能为甲基橙 可能为甲基橙 |
| B.酸性高锰酸钾溶液、碘水均需用酸式滴定管 |
| C.碱式滴定管可以通过挤压玻璃球下方的乳胶管放液 |
| D.滴定管中装液时,应由试剂瓶直接灌入,不得借用任何别的器皿 |
A.该产品中碳酸氢钠的含量约为 |
| B.第一次滴定终点时俯视读数,测得实验数据偏小 |
| C.第二次滴定终点结束后,迅速读数,测得实验数据偏大 |
| D.滴定前滴定管尖嘴处有气泡,第一次滴定结束后气泡消失,测得实验数据偏小 |
您最近一年使用:0次
解题方法
4 . 牛奶具有补充蛋白质、补钙、镇静安神等功效。回答下列问题:
(1)基态钙原子核外电子的空间运动状态有______ 种,同周期元素中基态原子成对价电子数比钙少的有______ (填元素符号)。
(2)三聚氰胺是一种重要的工业原料,曾被不法分子作为添加剂而引发毒奶粉事件。三聚氰胺在水中易发生水解和异构化,并与异构化产物形成层状的超分子,部分过程如下:______ 。乙发生“异构化”的原因为______ 。
②甲与丙能够形成层状超分子的原因为______ 。乙分子中N原子的孤对电子占据的轨道为______ 。
(3)由Ca和B两种元素形成晶体的晶胞结构如图(大球代表Ca)。______ 。
②Ca原子的配位数为______ 。
③若晶体的晶胞参数为apm,则该晶体的密度可表示为______ g∙cm-3 (设NA为阿伏加德罗常数的值)。
(1)基态钙原子核外电子的空间运动状态有
(2)三聚氰胺是一种重要的工业原料,曾被不法分子作为添加剂而引发毒奶粉事件。三聚氰胺在水中易发生水解和异构化,并与异构化产物形成层状的超分子,部分过程如下:
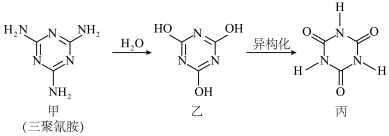
②甲与丙能够形成层状超分子的原因为
(3)由Ca和B两种元素形成晶体的晶胞结构如图(大球代表Ca)。
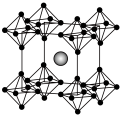
②Ca原子的配位数为
③若晶体的晶胞参数为apm,则该晶体的密度可表示为
您最近一年使用:0次
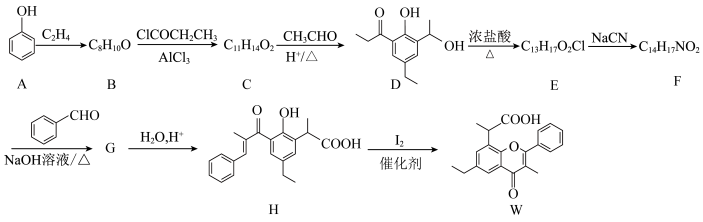
5 . 有机化合物W是一种镇痛药物的中间体,其一种合成路线如图所示:
①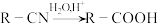 (R为烃基或H,下同);
(R为烃基或H,下同);
(1)B的名称为______ 。W中的含氧官能团名称为______ 。
(2)E的结构简式为______ 。C→D的反应类型为______ 。
(3)满足下列条件的C的同分异构体共有______ 种(不考虑立体异构)。
①含有苯环,且仅有两个侧链;
②遇 溶液显紫色;
溶液显紫色;
③与新制 悬浊液加热条件下反应,产生砖红色沉淀。
悬浊液加热条件下反应,产生砖红色沉淀。
(4)F-G反应的化学方程式为______ 。
(5)结合上述信息,以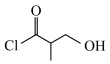 为原料三步合成
为原料三步合成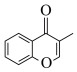 的路线为
的路线为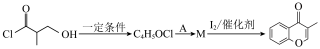 ,其中“一定条件”为
,其中“一定条件”为______ ,M的结构简式为______ 。
①
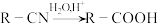 (R为烃基或H,下同);
(R为烃基或H,下同);②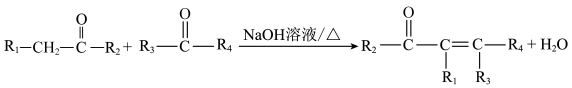
(1)B的名称为
(2)E的结构简式为
(3)满足下列条件的C的同分异构体共有
①含有苯环,且仅有两个侧链;
②遇
 溶液显紫色;
溶液显紫色;③与新制
 悬浊液加热条件下反应,产生砖红色沉淀。
悬浊液加热条件下反应,产生砖红色沉淀。(4)F-G反应的化学方程式为
(5)结合上述信息,以
 为原料三步合成
为原料三步合成 的路线为
的路线为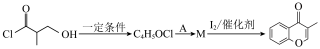 ,其中“一定条件”为
,其中“一定条件”为
您最近一年使用:0次
解题方法
6 . 氮化硅陶瓷是一种烧结时不收缩的无机材料陶瓷。以N2、H2、SiCl4气体(沸点57.6℃,极易水解,具有腐蚀性)为原料在高温下制备氮化硅的实验装置如图。
(1)仪器“A”的名称为______ 。甲中少量CuSO4的作用为______ 。
(2)乙中为NH4Cl和NaNO2的浓溶液,85℃发生反应,离子方程式为______ ,该反应的加热方式为______ 。
(3)丁装置中反应的化学方程式为______ 。戊装置的作用为______ 。
(4)实验结束时,停止加热丁装置,再通入一段时间的氮气,目的是______ 。
(5)实验结束后丁装置硬质玻璃管增重2.8g,己装置增重15.56g,该实验氮化硅的产率为______ (不考虑SiCl4在丙和戊中的损耗)。
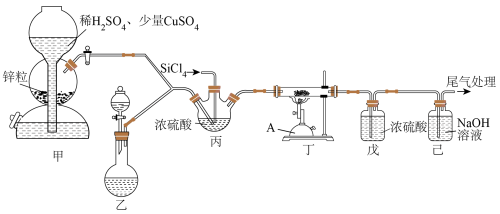
(1)仪器“A”的名称为
(2)乙中为NH4Cl和NaNO2的浓溶液,85℃发生反应,离子方程式为
(3)丁装置中反应的化学方程式为
(4)实验结束时,停止加热丁装置,再通入一段时间的氮气,目的是
(5)实验结束后丁装置硬质玻璃管增重2.8g,己装置增重15.56g,该实验氮化硅的产率为
您最近一年使用:0次
7 . 采用基于电化学的高效废铅酸电池回收技术,将废铅电极电解可重新获得铅蓄电池的两极材料,原理如图所示。下列说法正确的是

| A.a电极接电源正极 |
B.每生成1mol阳极产物,有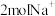 通过离子交换膜 通过离子交换膜 |
C.b的电极反应为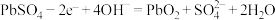 |
| D.电解一段时间后,左室pH增大 |
您最近一年使用:0次
8 . 金丝桃素具有极强的抗病毒作用,结构简式如图所示。下列关于金丝桃素的说法错误的是
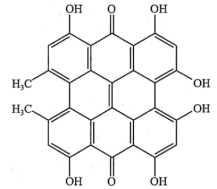
| A.能发生取代、加成反应 | B.难溶于水,易溶于NaOH溶液 |
C.1mol金丝桃素最多与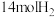 反应 反应 | D.芳环上的一氯取代物有2种 |
您最近一年使用:0次
9 . 薯类物质䤃酒含淀粉糊化、糊精水解和发酵制醇三个阶段。下列说法错误的是
| A.淀粉和麦芽糖均属于高分子化合物 |
| B.淀粉溶液能产生丁达尔效应 |
| C.发酵制醇阶段发生了分解反应 |
| D.乙醇和水的共沸物经生石灰处理、蒸馏可得无水乙醇 |
您最近一年使用:0次
解题方法
10 . 能正确表示下列反应的离子方程式为
A.用稀硝酸清洗试管内壁的银: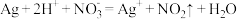 |
B.铜箔制作印刷电路板: |
C.向 溶液中加足量 溶液中加足量 溶液: 溶液: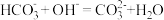 |
D. 溶液中通入足量氯气: 溶液中通入足量氯气: |
您最近一年使用:0次



