名校
1 . 寿山石是中华瑰宝,传统“四大印章石”之一。某地采掘的寿山石化学式为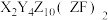 。已知F、Z、X、Y均为短周期元素且原子序数依次增大,X元素原子的最外层电子数等于其电子层数,且其单质能与强碱溶液反应生成
。已知F、Z、X、Y均为短周期元素且原子序数依次增大,X元素原子的最外层电子数等于其电子层数,且其单质能与强碱溶液反应生成 ,
,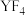 与
与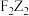 都是含有18个电子的分子。下列说法错误的是
都是含有18个电子的分子。下列说法错误的是
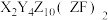 。已知F、Z、X、Y均为短周期元素且原子序数依次增大,X元素原子的最外层电子数等于其电子层数,且其单质能与强碱溶液反应生成
。已知F、Z、X、Y均为短周期元素且原子序数依次增大,X元素原子的最外层电子数等于其电子层数,且其单质能与强碱溶液反应生成 ,
,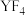 与
与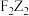 都是含有18个电子的分子。下列说法错误的是
都是含有18个电子的分子。下列说法错误的是| A.Y元素最高价氧化物对应的水化物为弱酸 |
| B.X单质的导电能力强于Y单质 |
| C.Z和F可形成不止一种化合物 |
D.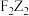 中既含有离子键,又含有共价键 中既含有离子键,又含有共价键 |
您最近一年使用:0次
名校
2 . 下列有关碱金属、卤素原子结构和性质的描述,正确的个数为
①随着核电荷数的增加,碱金属单质、卤素单质的熔、沸点依次升高,密度依次增大
②F、Cl、Br、I的最外层电子数都是7,次外层电子数都是8
③碱金属单质的金属性很强,均易与氧气发生反应,加热时生成的氧化物形式均为R2O2
④根据同主族元素性质的递变规律推测,At2与H2化合较难,砹化银难溶于水
⑤根据Cl、Br、I的非金属性依次减弱,可推出HCl、HBr、HI的酸性依次减弱
⑥碱金属都应保存在煤油中
⑦卤素按F、Cl、Br、I的顺序非金属性逐渐减弱的原因是随着核电荷数的增加,电子层数增多,原子半径增大
⑧由碳酸钠的性质可知碳酸铯易发生分解反应生成氧化铯和二氧化碳
①随着核电荷数的增加,碱金属单质、卤素单质的熔、沸点依次升高,密度依次增大
②F、Cl、Br、I的最外层电子数都是7,次外层电子数都是8
③碱金属单质的金属性很强,均易与氧气发生反应,加热时生成的氧化物形式均为R2O2
④根据同主族元素性质的递变规律推测,At2与H2化合较难,砹化银难溶于水
⑤根据Cl、Br、I的非金属性依次减弱,可推出HCl、HBr、HI的酸性依次减弱
⑥碱金属都应保存在煤油中
⑦卤素按F、Cl、Br、I的顺序非金属性逐渐减弱的原因是随着核电荷数的增加,电子层数增多,原子半径增大
⑧由碳酸钠的性质可知碳酸铯易发生分解反应生成氧化铯和二氧化碳
| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次
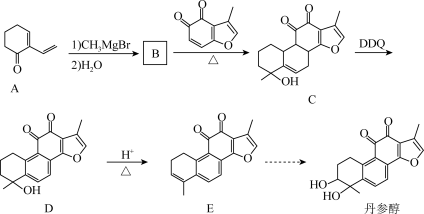
3 . 丹参醇是中药丹参中的一种天然产物。合成丹参醇的部分路线如下。_______
(2)B的结构简式为_______ ,B→C的反应类型为_______ 。
(3)E的分子式为_______
(4)写出A发生聚合反应(环参与成链)的方程式:_______ 。
(5)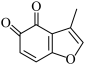 的一种同分异构体同时满足下列条件,写出该同分昇构体的结构简式
的一种同分异构体同时满足下列条件,写出该同分昇构体的结构简式_______ , 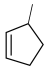 和
和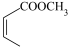 ,为原料制备
,为原料制备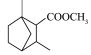 的合成路线流程图(无机试剂和乙醇任用)
的合成路线流程图(无机试剂和乙醇任用)_______ 。
已知: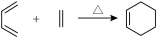
(2)B的结构简式为
(3)E的分子式为
(4)写出A发生聚合反应(环参与成链)的方程式:
(5)
 的一种同分异构体同时满足下列条件,写出该同分昇构体的结构简式
的一种同分异构体同时满足下列条件,写出该同分昇构体的结构简式①分子中含有苯环,能与FeCl₃溶液发生显色反应,不能发生银镜反应;
②碱性条件水解生成两种产物,酸化后分子中均只有2种不同化学环境的氢。
(6)写出以 和
和 ,为原料制备
,为原料制备 的合成路线流程图(无机试剂和乙醇任用)
的合成路线流程图(无机试剂和乙醇任用)
您最近一年使用:0次
4 . H₂L为某邻苯二酚类配体,其pKa1=7.46,pK2=12.4(pKa=-lgKa)。常温下构建Fe(Ⅲ)-H₂I溶液体系,其中c0(Fe3+)=2.0×10-4mol·L,c0(H2L)=5.0×10-3mol⋅L-1。体系中含Fe物种的组分分布系数δ与pH的关系如图所示,分布系数  ,已知lg 5≈0.7。下列说法正确的是
,已知lg 5≈0.7。下列说法正确的是
 ,已知lg 5≈0.7。下列说法正确的是
,已知lg 5≈0.7。下列说法正确的是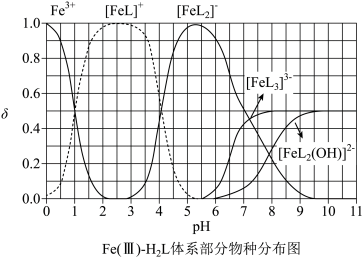
| A.当pH=0.5时,体系中c(H2L)>c([FeL]+)>c(OH-)>c(HL-) |
B.L²⁻+Fe³⁺ FeL⁺的平衡常数的lgK约为20 FeL⁺的平衡常数的lgK约为20 |
| C.pH在9.5~10.5之间,含L的物种主要为HL⁻ |
| D.当pH=10时,参与配位的c(L²⁻)≈2×10⁻⁴mol⋅L⁻¹ |
您最近一年使用:0次
解题方法
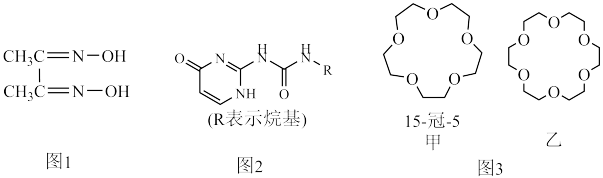
5 . 配合物和超分子广泛应用于新材料合成、物质的鉴别和分离。如丁二酮肟(如图1)可用于鉴别 Ni2+,嘧啶衍生物(如图2)是形成高韧性超分子的单体,冠醚(如图3)是皇冠状分子,可有大小不同的空穴适配不同大小的碱金属离子。
(1)基态 Ni2+核外未成对电子的数目为______ 。
(2)丁二酮肟与 Ni²⁺生成血红色配合物的结构为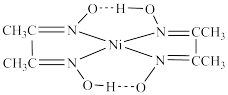 ,相同压强下,该配合物的沸点低于干二酮肟的原因为
,相同压强下,该配合物的沸点低于干二酮肟的原因为_______ 。
(3)Ni在一定条件下可与CO形成 Ni(CO)x,分子中每个Ni原子的价电子数及其周围CO提供的成键电子数之和为18,则x=_______ 。
(4)图2所示分子所含元素电负性由小到大的顺序为______ 。
(5)冠醚是状如皇冠的一类醚,分子中存在空穴,图3中甲、乙两种冠醚可分别识别 Na+、K+,其主要原因为________ ;乙的名称为______ 。
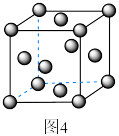
(6)金属Ni的立方晶胞结构如图4所示,则Ni的空间利用率为________ (用含π的代式表示)。
(1)基态 Ni2+核外未成对电子的数目为
(2)丁二酮肟与 Ni²⁺生成血红色配合物的结构为
 ,相同压强下,该配合物的沸点低于干二酮肟的原因为
,相同压强下,该配合物的沸点低于干二酮肟的原因为(3)Ni在一定条件下可与CO形成 Ni(CO)x,分子中每个Ni原子的价电子数及其周围CO提供的成键电子数之和为18,则x=
(4)图2所示分子所含元素电负性由小到大的顺序为
(5)冠醚是状如皇冠的一类醚,分子中存在空穴,图3中甲、乙两种冠醚可分别识别 Na+、K+,其主要原因为
(6)金属Ni的立方晶胞结构如图4所示,则Ni的空间利用率为
您最近一年使用:0次
解题方法
6 . 化合物Z2X2Y4 (YW)2,是制备X(YW)3(结构如图所示)的一种原料,其中 W、X、Y、Z为原子序数依次增大的短周期主族元素,W与X原子的电子数之和等于 Y 原子的价电子数,基态 Z原子的s能级与p能级填充的电子总数相等。下列说法正确的是

| A.第一电离能: Z> Y> X |
| B.常见单质的熔点:Z>X>Y>W |
| C.X、Z的单质均可通过电解熔融氯化物的方法冶炼 |
| D.X(YW)3中键角:∠YXY>∠WYX |
您最近一年使用:0次
名校
解题方法
7 . 絮凝剂聚合氯化铝{ ,
, }广泛用于废水处理。由偏铝酸钙
}广泛用于废水处理。由偏铝酸钙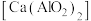 制备聚合氯化铝的一种工艺流程如下:
制备聚合氯化铝的一种工艺流程如下: 的絮凝效果可用盐基度(盐基度
的絮凝效果可用盐基度(盐基度 )衡量,当盐基度为0.60~0.85时,絮凝效果较好。
)衡量,当盐基度为0.60~0.85时,絮凝效果较好。
(1)“碱溶”时,化学反应方程式为___________ 。
(2)若滤液浓度较大,则通入过量 不利于减少
不利于减少 滤饼中的杂质,其原因是
滤饼中的杂质,其原因是___________ 。
(3)“酸化”时的装置如图所示,仪器A的名称为___________ ,若要使产品盐基度为 ,则
,则
___________ ;先将 滤饼分散在蒸馏水中,再向其中滴加一定量的盐酸,与直接向滤饼中加盐酸相比,优点是
滤饼分散在蒸馏水中,再向其中滴加一定量的盐酸,与直接向滤饼中加盐酸相比,优点是____________ 。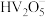 、
、 的碱性废水制取聚合氯化铝的实验方案:取适量废水,
的碱性废水制取聚合氯化铝的实验方案:取适量废水,___________ ,向其中滴加一定量的盐酸,得到聚合氯化铝。(实验中须使用的试剂有: 、5%的双氧水、蒸馏水、
、5%的双氧水、蒸馏水、 溶液)
溶液)
 ,
, }广泛用于废水处理。由偏铝酸钙
}广泛用于废水处理。由偏铝酸钙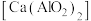 制备聚合氯化铝的一种工艺流程如下:
制备聚合氯化铝的一种工艺流程如下: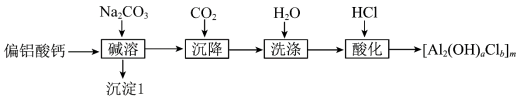
 的絮凝效果可用盐基度(盐基度
的絮凝效果可用盐基度(盐基度 )衡量,当盐基度为0.60~0.85时,絮凝效果较好。
)衡量,当盐基度为0.60~0.85时,絮凝效果较好。(1)“碱溶”时,化学反应方程式为
(2)若滤液浓度较大,则通入过量
 不利于减少
不利于减少 滤饼中的杂质,其原因是
滤饼中的杂质,其原因是(3)“酸化”时的装置如图所示,仪器A的名称为
 ,则
,则
 滤饼分散在蒸馏水中,再向其中滴加一定量的盐酸,与直接向滤饼中加盐酸相比,优点是
滤饼分散在蒸馏水中,再向其中滴加一定量的盐酸,与直接向滤饼中加盐酸相比,优点是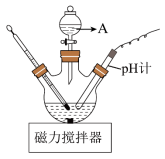
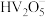 、
、 的碱性废水制取聚合氯化铝的实验方案:取适量废水,
的碱性废水制取聚合氯化铝的实验方案:取适量废水, 、5%的双氧水、蒸馏水、
、5%的双氧水、蒸馏水、 溶液)
溶液)| 化合价 |  |  |
| +4价V | 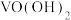 沉淀 沉淀 | 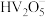 |
| +5价V |  |  |
| +3价Al |  沉淀 沉淀 |  |
您最近一年使用:0次
名校
解题方法
8 . 下列各项操作错误的有
| A.用乙醇萃取溴水中的溴单质的操作可选用分液漏斗 |
| B.进行分液时,分液漏斗中的下层液体从下口放出,上层液体则从上口倒出 |
| C.萃取、分液前需对分液漏斗检漏 |
| D.为保证分液漏斗内的液体顺利流出,需将上口的塞子拿下 |
您最近一年使用:0次
名校
9 . 下列有关物质的性质与用途均正确,且具有对应关系的是
| A.硅酸钠易溶于水,可用作木材防火剂 |
B. 与水反应生成 与水反应生成 ,故 ,故 是酸性氧化物 是酸性氧化物 |
C. 的酸性弱于 的酸性弱于 ,故非金属性C强于Si ,故非金属性C强于Si |
| D.二氧化硅做半导体材料,故“玉兔号”月球车帆板太阳能电池片的材料主要是二氧化硅 |
您最近一年使用:0次
解题方法
10 . 葛根素具有广泛的药理作用,临床上主要用于心脑血管疾病的治疗,其一种合成路线如下图:

已知:
ⅰ.BnBr为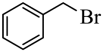
ⅱ.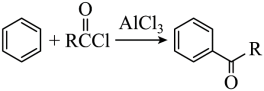
ⅲ.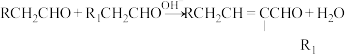
ⅳ.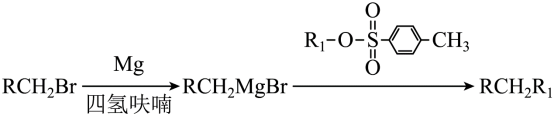
(1)化合物A的名称是_____ ,“试剂1”的结构简式_____ 。
(2)由C到D化学反应方程式_____ (写总反应)。
(3)化合物D的一种同分异构体能与 的水溶液反应生成气体,核磁共振氢谱检测到四组峰(峰面积比为2∶4∶4∶1),其结构简式为
的水溶液反应生成气体,核磁共振氢谱检测到四组峰(峰面积比为2∶4∶4∶1),其结构简式为_____ (写出一种即可)。
(4)E分子中含有3个六元环,下列描述正确的是_____ 。
a.E分子中存在手性碳原子
b.E分子中存在2种含氧官能团
c.1molE与溴水反应最多可消耗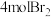
d.1个E分子中至少有9个碳原子共平面
(5)“反应5”的反应类型为_____ 。
(6)在有机合成反应时,往往需要先将要保护的基团“反应掉”,待条件适宜时,再将其“复原”,这叫做“基团保护”。上述反应中起基团保护作用的是_____ (填选项)。
a.反应1和反应3 b.反应4和反应5 c.反应2和反应6

已知:
ⅰ.BnBr为

ⅱ.
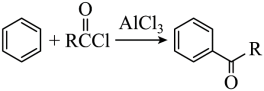
ⅲ.
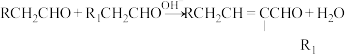
ⅳ.
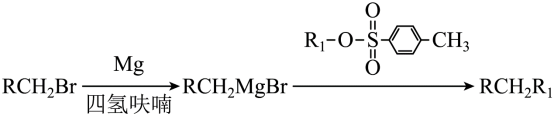
(1)化合物A的名称是
(2)由C到D化学反应方程式
(3)化合物D的一种同分异构体能与
 的水溶液反应生成气体,核磁共振氢谱检测到四组峰(峰面积比为2∶4∶4∶1),其结构简式为
的水溶液反应生成气体,核磁共振氢谱检测到四组峰(峰面积比为2∶4∶4∶1),其结构简式为(4)E分子中含有3个六元环,下列描述正确的是
a.E分子中存在手性碳原子
b.E分子中存在2种含氧官能团
c.1molE与溴水反应最多可消耗
d.1个E分子中至少有9个碳原子共平面
(5)“反应5”的反应类型为
(6)在有机合成反应时,往往需要先将要保护的基团“反应掉”,待条件适宜时,再将其“复原”,这叫做“基团保护”。上述反应中起基团保护作用的是
a.反应1和反应3 b.反应4和反应5 c.反应2和反应6
您最近一年使用:0次



