名校
解题方法
1 . 科技是第一生产力,我国科学家在诸多领域取得了重大成就。下列说法正确的是
A. 的发现开启了碳纳米材料应用的新时代, 的发现开启了碳纳米材料应用的新时代, 属于混合型晶体 属于混合型晶体 |
B.“神舟十七号”发动机的耐高温结构材料 属于分子晶体 属于分子晶体 |
C.飞船火箭使用偏二甲肼[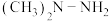 ]作燃料, ]作燃料,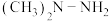 属于烃类 属于烃类 |
| D.量子计算机“悟空”即将面世,其传输信号的光纤主要成分为二氧化硅 |
您最近一年使用:0次
2024-03-25更新
|
359次组卷
|
4卷引用:广东省汕尾市陆河县河田中学2023-2024学年高二下学期4月期中考试化学试题
2 . 根据下列陈述类推得出的结论正确的是
| A.氯气能与碘化钠溶液反应置换出碘,则氟气也能与氯化钠溶液反应置换出氯气 |
| B.将CO2通入Ba(OH)2溶液中产生白色沉淀,则将CO2通入BaCl2溶液中也能产生白色沉淀 |
| C.Na常温下与水剧烈反应,则K常温下也能与水剧烈反应 |
| D.Fe能从CuSO4溶液中置换出Cu,则Na也能从CuSO4溶液中置换出 Cu |
您最近一年使用:0次
解题方法
3 . 实验室用如图所示装置制备干燥的Cl2并探究其性质。其中,a为湿润的淀粉-KI试纸,b为湿润的红纸条。下列说法正确的是
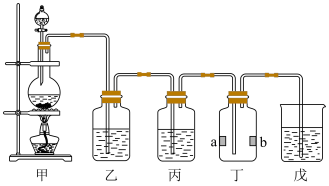
| A.上述装置用浓盐酸和MnO2反应制备Cl2,用向下排空气法收集 Cl2 |
| B.装置乙中为浓硫酸,装置丙中为NaOH溶液 |
| C.一段时间后,装置丁中a变蓝,反应的离子方程式为Cl2+2I-=I2+2Cl- |
| D.装置丁中b褪色,说明Cl2具有漂白性 |
您最近一年使用:0次
2024-01-27更新
|
94次组卷
|
2卷引用:广东省汕尾市2023-2024学年高一上学期期末教学质量监测化学试卷
4 . 下列操作中发生化学变化的是
| A.霓红灯通电后发出红光 |
| B.向饱和食盐水中滴加浓盐酸,溶液变浑浊 |
| C.无光学活性的合成酒石酸盐溶液沾染霉菌后,溶液的光学活性逐渐提高 |
| D.将装有少量碘的小烧杯盖上表面皿后放在陶土网上小火加热,烧杯中出现紫烟 |
您最近一年使用:0次
5 . “高山流水觅知音”。下列中国古乐器中,主要由硅酸盐材料制成的是
|
|
|
|
| A.九霄环佩木古琴 | B.裴李岗文化骨笛 | C.商朝后期陶埙 | D.曾侯乙青铜编钟 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-04更新
|
7292次组卷
|
18卷引用:广东省汕尾市陆河县河田中学2023-2024学年高二下学期4月期中考试化学试题
广东省汕尾市陆河县河田中学2023-2024学年高二下学期4月期中考试化学试题2023年高考广东卷化学真题(已下线)2023年广东卷高考真题变式题(选择题1-5)(已下线)第10讲 硅及其化合物青海省海南藏族自治州高级中学2022-2023学年高一下学期期末考试化学试题(已下线)考点13 硅及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)河南省南阳市第一中学校2023-2024学年高三上学期第一次月考化学试题河南省南阳市南阳一中2023-2024学年高三上学期9月月考化学试题江苏省常熟中学2023-2024学年高三上学期阶段性抽测一化学试题2024届江苏省常熟市中学高三上学期阶段性抽测一 化学试题辽宁省阜新市第二高级中学2022-2023学年高一下学期期末考试化学试卷广东省清远市阳山县南阳中学2023-2024学年高一下学期第一次月考化学(选择性)试题江西省宜春市丰城中学2023-2024学年高一下学期3月月考化学试题湖北省武汉市华中师范大学第一附属中学2023-2024学年高一下学期4月期中考试化学试题吉林省通化市辉南县第六中学2023-2024学年高一下学期3月半月考化学试卷 四川省成都市龙泉驿区东竞高级中学2023-2024学年高一下学期3月月考化学试卷北京市第二中学2023-2024学年高三下学期三模化学试题广东省广州市执信中学2023-2024学年高一下学期5月期中考试化学试题
解题方法
6 . 回答下列问题:

已知以下反应:
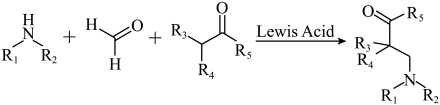
(1)请画出D、E、G、H、I、J、K、L的结构。___________
(2)有机反应类型众多,A→B属于___________ ,C→D属于___________ ,D+H→属于___________ 。
(3)化合物E进行硝化时,硝化主产物有两种,它们的名称为___________ 、___________ 。

已知以下反应:

(1)请画出D、E、G、H、I、J、K、L的结构。
(2)有机反应类型众多,A→B属于
(3)化合物E进行硝化时,硝化主产物有两种,它们的名称为
您最近一年使用:0次
7 . 碳碳键的构建一直是有机合成中重要的一环。
Ⅰ.以下是构建碳碳键 的一种反应和其机理,其中NHC指氮杂卡宾。
的一种反应和其机理,其中NHC指氮杂卡宾。
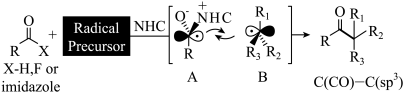
(1)该碳碳键的构建属于___________ 机理。(填字母)
a.极性 b.自由基
(2)已知两中间体A、B的构型为平面三角形,则根据杂化轨道理论,其单电子分别填在什么轨道上?_______
Ⅱ.类比该反应,广东工业大学的科研人员提出了 碳碳键的构建反应,其反应和机理如下:
碳碳键的构建反应,其反应和机理如下:
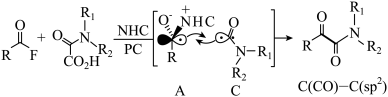
(3)已知两个中间体A、C的构型分别为平面三角形和折线型,则根据杂化轨道理论,其单电子分别填在什么轨道上?_______
Ⅲ.科研人员据此提出了以下具体反应体系:
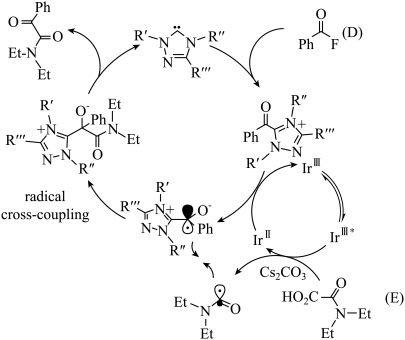
(4)写出该反应的化学方程式(无需标出反应条件)。_______
(5)该反应本质上,物质D被___________ (选填“氧化”或“还原”,下同),物质E被___________ 。
(6)其中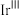 代表PC-1,可表示为
代表PC-1,可表示为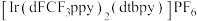 ,已知PC-1的结构如下。若以“M”代表“
,已知PC-1的结构如下。若以“M”代表“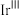 ”,“
”,“ ”代表“
”代表“ ”,“
”,“ ”代表“dtbpy”,画出PC-1的全部立体异构体。
”代表“dtbpy”,画出PC-1的全部立体异构体。_______
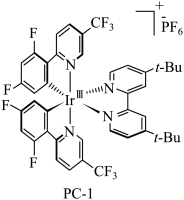
Ⅰ.以下是构建碳碳键
 的一种反应和其机理,其中NHC指氮杂卡宾。
的一种反应和其机理,其中NHC指氮杂卡宾。
(1)该碳碳键的构建属于
a.极性 b.自由基
(2)已知两中间体A、B的构型为平面三角形,则根据杂化轨道理论,其单电子分别填在什么轨道上?
Ⅱ.类比该反应,广东工业大学的科研人员提出了
 碳碳键的构建反应,其反应和机理如下:
碳碳键的构建反应,其反应和机理如下:
(3)已知两个中间体A、C的构型分别为平面三角形和折线型,则根据杂化轨道理论,其单电子分别填在什么轨道上?
Ⅲ.科研人员据此提出了以下具体反应体系:

(4)写出该反应的化学方程式(无需标出反应条件)。
(5)该反应本质上,物质D被
(6)其中
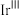 代表PC-1,可表示为
代表PC-1,可表示为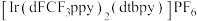 ,已知PC-1的结构如下。若以“M”代表“
,已知PC-1的结构如下。若以“M”代表“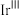 ”,“
”,“ ”代表“
”代表“ ”,“
”,“ ”代表“dtbpy”,画出PC-1的全部立体异构体。
”代表“dtbpy”,画出PC-1的全部立体异构体。
您最近一年使用:0次
8 . Ni-Cd蓄电池是一类重要的电池,其具有使用寿命长、放电电压稳定、机械性能好等优点,广泛应用于现代军事及航天事业等领域。其中,Ni-Cd蓄电池的正极活性物质为 。资料显示,目前T业上常用化学沉淀法和粉末金属法等方法来制备
。资料显示,目前T业上常用化学沉淀法和粉末金属法等方法来制备 。
。
Ⅰ.化学沉淀法的生产流程图如下所示:
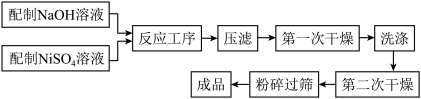
(1)写出该合成方法的化学反应方程式。_______
(2)该反应若在弱碱性条件下进行,则得到碱式硫酸盐 沉淀,请写出该化学反应方程式。
沉淀,请写出该化学反应方程式。_______
(3)在“反应工序”中, 溶液以喷淋形式加入到不断搅拌的过量的NaOH溶液中,搅拌的主要目的是什么?
溶液以喷淋形式加入到不断搅拌的过量的NaOH溶液中,搅拌的主要目的是什么?_______
(4)蒸汽干燥时,干燥温度不能超过200℃,为什么?_______
(5)“洗涤”过程的目的是洗去什么离子?可用什么溶液检验该离子是否洗净?_______
Ⅱ.粉末金属法是以粉末状金属镍为原料,通过镍粉在适当物理化学条件下的氧化水解反应来制备 。
。
(6)写出该方法的化学反应方程式。_______
(7)从动力学角度考虑,通常条件下该反应速度很小,请写出提高反应速率的方法(一条即可)。_______
 。资料显示,目前T业上常用化学沉淀法和粉末金属法等方法来制备
。资料显示,目前T业上常用化学沉淀法和粉末金属法等方法来制备 。
。Ⅰ.化学沉淀法的生产流程图如下所示:

(1)写出该合成方法的化学反应方程式。
(2)该反应若在弱碱性条件下进行,则得到碱式硫酸盐
 沉淀,请写出该化学反应方程式。
沉淀,请写出该化学反应方程式。(3)在“反应工序”中,
 溶液以喷淋形式加入到不断搅拌的过量的NaOH溶液中,搅拌的主要目的是什么?
溶液以喷淋形式加入到不断搅拌的过量的NaOH溶液中,搅拌的主要目的是什么?(4)蒸汽干燥时,干燥温度不能超过200℃,为什么?
(5)“洗涤”过程的目的是洗去什么离子?可用什么溶液检验该离子是否洗净?
Ⅱ.粉末金属法是以粉末状金属镍为原料,通过镍粉在适当物理化学条件下的氧化水解反应来制备
 。
。(6)写出该方法的化学反应方程式。
(7)从动力学角度考虑,通常条件下该反应速度很小,请写出提高反应速率的方法(一条即可)。
您最近一年使用:0次
9 . 2023年,大连理工大学的科学家们发表了一篇以亚氨基锂为介导,在电驱动下合成氨分子的报导。这些发现为开发新型电驱动合成氨开辟了新的可能性。
(1)以下是合成氨中应用到的两个反应,请根据给出的热力学数据表(“—”代表忽略不计),计算反应(Ⅰ)在298.15K下的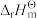 、
、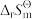 、
、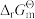 、
、 和反应(Ⅱ)的
和反应(Ⅱ)的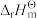 、
、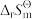 。(写出计算结果即可)
。(写出计算结果即可)_______
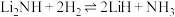 (Ⅰ)
(Ⅰ)
 (Ⅱ)
(Ⅱ)
(2)计算在1barH2、298.15K的反应条件下,NH3的平衡分压p(NH3)。(写出计算结果即可)_______
(3)经研究,反应(Ⅰ)在外加电压的条件下有热化学和电化学两种反应途径。
(ⅰ)在热化学过程中,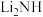 被
被 逐步取代为
逐步取代为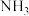 (反应Ⅲ、Ⅳ)。请写出化学反应方程式(Ⅲ)、(Ⅳ)。
(反应Ⅲ、Ⅳ)。请写出化学反应方程式(Ⅲ)、(Ⅳ)。_______
(ⅱ)在电化学过程中,反应初期,体系可以视为以LiCl-NaCl-KCl为熔融电解质溶剂,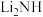 为溶质,反应物为
为溶质,反应物为 、
、 。下表是部分电对在25℃时的标准电极电势表(SHE:标准氢电极)。
。下表是部分电对在25℃时的标准电极电势表(SHE:标准氢电极)。
①试写出最有可能在阴极上发生电化学反应的反应方程式_______ ;
②上述猜测有一个小漏洞,请简述该漏洞_______ 。
(1)以下是合成氨中应用到的两个反应,请根据给出的热力学数据表(“—”代表忽略不计),计算反应(Ⅰ)在298.15K下的
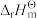 、
、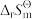 、
、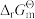 、
、 和反应(Ⅱ)的
和反应(Ⅱ)的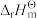 、
、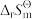 。(写出计算结果即可)
。(写出计算结果即可)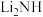 | LiH |  |  | 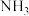 | |
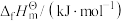 | -222 | -90.5 | 0 | 0 | -45.9 |
S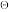 /(J /(J mol-1 mol-1 K-1) K-1) | — | — | 130.7 | 191.6 | 192.8 |
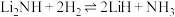 (Ⅰ)
(Ⅰ) (Ⅱ)
(Ⅱ)(2)计算在1barH2、298.15K的反应条件下,NH3的平衡分压p(NH3)。(写出计算结果即可)
(3)经研究,反应(Ⅰ)在外加电压的条件下有热化学和电化学两种反应途径。
(ⅰ)在热化学过程中,
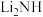 被
被 逐步取代为
逐步取代为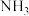 (反应Ⅲ、Ⅳ)。请写出化学反应方程式(Ⅲ)、(Ⅳ)。
(反应Ⅲ、Ⅳ)。请写出化学反应方程式(Ⅲ)、(Ⅳ)。(ⅱ)在电化学过程中,反应初期,体系可以视为以LiCl-NaCl-KCl为熔融电解质溶剂,
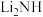 为溶质,反应物为
为溶质,反应物为 、
、 。下表是部分电对在25℃时的标准电极电势表(SHE:标准氢电极)。
。下表是部分电对在25℃时的标准电极电势表(SHE:标准氢电极)。| The electrode reaction | 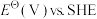 |
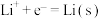 | -3.03 |
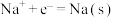 | -2.71 |
 | -2.93 |
 | -2.65 |
 | -2.30 |
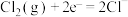 | +1.36 |
②上述猜测有一个小漏洞,请简述该漏洞
您最近一年使用:0次
10 . ⅥB族元素有着独特的性质,其中的多酸化合物可谓是引人入胜。
(1)请写出Cr、Mo、W的价电子组态。(如Fe的为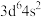 )
)_______
(2)请写出铬酸根离子在酸性水溶液的条件下聚合成重铬酸根离子的可逆反应方程式。_______
(3)当钼酸盐水溶液酸化至pH小于6时,可以得到一种带6个负电荷的七钼酸根阴离子。请写出该聚合平衡的离子反应方程式。_______
(4)当上述溶液进一步酸化到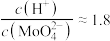 时,由电动势和超离心法研究结果推断,溶液中形成了非常大的聚阴离子X,已知X带有8个负电荷,只含两种配体,且其中一个配体为中性,
时,由电动势和超离心法研究结果推断,溶液中形成了非常大的聚阴离子X,已知X带有8个负电荷,只含两种配体,且其中一个配体为中性,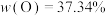 ,
,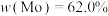 ,请写出X的化学式(书写时要表示出配体种类)和计算过程。
,请写出X的化学式(书写时要表示出配体种类)和计算过程。_______
(5)将正磷酸、钼酸铵、硝酸混合在一起,会生成一种黄色的十二钼磷酸铵,化学式为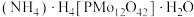 ,此反应在分析化学上被用来检验
,此反应在分析化学上被用来检验 及其盐。请写出该反应的化学方程式。
及其盐。请写出该反应的化学方程式。_______
(1)请写出Cr、Mo、W的价电子组态。(如Fe的为
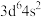 )
)(2)请写出铬酸根离子在酸性水溶液的条件下聚合成重铬酸根离子的可逆反应方程式。
(3)当钼酸盐水溶液酸化至pH小于6时,可以得到一种带6个负电荷的七钼酸根阴离子。请写出该聚合平衡的离子反应方程式。
(4)当上述溶液进一步酸化到
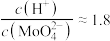 时,由电动势和超离心法研究结果推断,溶液中形成了非常大的聚阴离子X,已知X带有8个负电荷,只含两种配体,且其中一个配体为中性,
时,由电动势和超离心法研究结果推断,溶液中形成了非常大的聚阴离子X,已知X带有8个负电荷,只含两种配体,且其中一个配体为中性,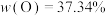 ,
,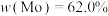 ,请写出X的化学式(书写时要表示出配体种类)和计算过程。
,请写出X的化学式(书写时要表示出配体种类)和计算过程。(5)将正磷酸、钼酸铵、硝酸混合在一起,会生成一种黄色的十二钼磷酸铵,化学式为
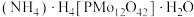 ,此反应在分析化学上被用来检验
,此反应在分析化学上被用来检验 及其盐。请写出该反应的化学方程式。
及其盐。请写出该反应的化学方程式。
您最近一年使用:0次







