解题方法
1 . 下列陈述Ⅰ和陈述Ⅱ均正确,且不具有对应关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 乙醇的沸点高于二甲醚( ) ) | 乙醇能形成分子间氢键,而二甲醚不能 |
| B | 氯化钠溶液能导电 | 氯化钠溶液中有能自由移动的离子 |
| C |  的酸性比 的酸性比 的强 的强 | F的电负性大于Cl的电负性 |
| D |  难溶于水 难溶于水 |  的相对分子质量比水大 的相对分子质量比水大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 .  、
、 (主要指
(主要指 和
和 )是大气主要污染物之一、有效去除大气中的
)是大气主要污染物之一、有效去除大气中的 、
、 是环境保护的重要课题。
是环境保护的重要课题。
已知:
反应1: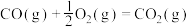
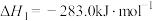
反应2:
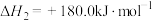
反应3:

反应4:
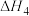
回答下列问题:
(1)计算
_____  ,已知反应3的
,已知反应3的 ,则该反应自发进行的最高温度为
,则该反应自发进行的最高温度为_____ (取整数)K。
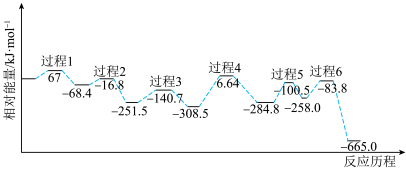
(2)已知反应4在某催化剂作用下的反应历程如图。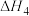
_____ (填“ ”或“
”或“ ”)0.
”)0.
②该反应历程的决速步骤为_____ 。
③可提高该反应中 平衡转化率的措施有
平衡转化率的措施有_____ (填两条)。
(3)向密闭容器中充入一定量的 和
和 ,保持总压为
,保持总压为 ,发生反应4.当
,发生反应4.当 时
时 的平衡转化率随温度
的平衡转化率随温度 以及
以及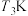 下NO的平衡转化率随投料比
下NO的平衡转化率随投料比 的变化关系如图:
的变化关系如图:_____ (填标号)。
A.气体的密度保持不变
B. 的浓度不变
的浓度不变
C.
②表示 时
时 的平衡转化率随温度
的平衡转化率随温度 的变化关系曲线是
的变化关系曲线是_____ (填“"或“II"),理由是_____ 。
③a、d两点对应的平衡常数大小比较为
_____ (填“>”“<”或“=”)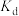 。
。
④b点对应条件下的压强平衡常数
_____  (
( 为用分压表示的平衡常数,分压=总压×物质的量分数,列出计算式即可)。
为用分压表示的平衡常数,分压=总压×物质的量分数,列出计算式即可)。
 、
、 (主要指
(主要指 和
和 )是大气主要污染物之一、有效去除大气中的
)是大气主要污染物之一、有效去除大气中的 、
、 是环境保护的重要课题。
是环境保护的重要课题。已知:
反应1:
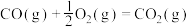
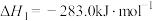
反应2:

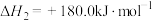
反应3:


反应4:

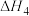
回答下列问题:
(1)计算

 ,已知反应3的
,已知反应3的 ,则该反应自发进行的最高温度为
,则该反应自发进行的最高温度为(2)已知反应4在某催化剂作用下的反应历程如图。
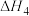
 ”或“
”或“ ”)0.
”)0.②该反应历程的决速步骤为
③可提高该反应中
 平衡转化率的措施有
平衡转化率的措施有(3)向密闭容器中充入一定量的
 和
和 ,保持总压为
,保持总压为 ,发生反应4.当
,发生反应4.当 时
时 的平衡转化率随温度
的平衡转化率随温度 以及
以及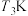 下NO的平衡转化率随投料比
下NO的平衡转化率随投料比 的变化关系如图:
的变化关系如图:
A.气体的密度保持不变
B.
 的浓度不变
的浓度不变C.

②表示
 时
时 的平衡转化率随温度
的平衡转化率随温度 的变化关系曲线是
的变化关系曲线是③a、d两点对应的平衡常数大小比较为

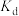 。
。④b点对应条件下的压强平衡常数

 (
( 为用分压表示的平衡常数,分压=总压×物质的量分数,列出计算式即可)。
为用分压表示的平衡常数,分压=总压×物质的量分数,列出计算式即可)。
您最近一年使用:0次
2024-05-16更新
|
551次组卷
|
4卷引用:广东省揭阳市2024届高三下学期二模考试化学试题
3 . 某同学利用如图所示的硬质玻璃管进行氯气的性质实验,已知f处为一团蘸有KOH溶液的棉花团,下列说法错误的是
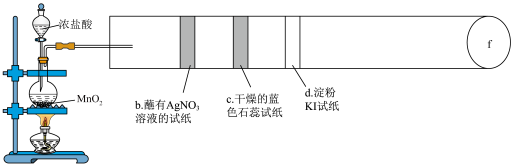
A.b处出现白色物质,说明氯气溶于水并生成 |
| B.c处现象为先变红后褪色 |
C.d处试纸变蓝,发生的反应为 |
| D.蘸有KOH溶液的棉花团的作用是处理尾气 |
您最近一年使用:0次
4 . 回答下列问题。
(1)H2S、CH4、H2O的沸点由高到低的顺序为:___________ 。
(2)HCN(H-C≡N)的一个分子中σ键和π键的个数比为:___________ 。
(3)SO 的中心原子采取
的中心原子采取___________ 杂化,空间结构是___________ 。
(4)基态硅原子最外层的电子排布图为:___________ 。
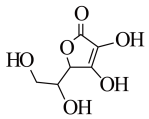
(5)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性___________ (填“难溶于水”或“易溶于水”)。
(6)LiBH4中不存在的作用力有___________。
(7)氢化锂(LiH)中负离子半径大于正离子半径,其原因是___________ 。
(1)H2S、CH4、H2O的沸点由高到低的顺序为:
(2)HCN(H-C≡N)的一个分子中σ键和π键的个数比为:
(3)SO
 的中心原子采取
的中心原子采取(4)基态硅原子最外层的电子排布图为:
(5)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性

(6)LiBH4中不存在的作用力有___________。
| A.离子键 | B.极性共价键 | C.非极性共价键 | D.分子间作用力 |
(7)氢化锂(LiH)中负离子半径大于正离子半径,其原因是
您最近一年使用:0次
5 . 回答下列问题。
(1)①比较键长大小:C-H___________ N-H___________ H-O(用“>”或“<”填空)。
②比较键能大小:C-H___________ N-H___________ H-O(用“>”或“<”填空)。
(2)乙烯分子中的碳原子均采取___________ 杂化,碳原子与氢原子形成σ键,两碳原子之间形成双键(1个___________ 键和1个___________ 键)。
(3)乙烯分子中的所有原子都位于___________ ,相邻两个键之间的夹角约为___________ 。
(4)铁原子的价层电子排布式为:___________ 。
(1)①比较键长大小:C-H
②比较键能大小:C-H
(2)乙烯分子中的碳原子均采取
(3)乙烯分子中的所有原子都位于
(4)铁原子的价层电子排布式为:
您最近一年使用:0次
名校
解题方法
6 . 二氧化铈( )是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含
)是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含 、
、 等)为原料制备
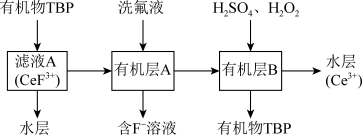
等)为原料制备 的一种工艺流程如下图所示:
的一种工艺流程如下图所示: 和
和 ;②滤液A中含:
;②滤液A中含: 、
、 等离子。
等离子。
回答下列问题:
(1)滤渣A的主要成分是________ (填化学式);“酸浸”不用盐酸的理由是________ (答一点即可)。
(2)“系列操作”包含以下几个过程:已知: 不能溶于有机物TBP;
不能溶于有机物TBP; 能溶于有机物TBP,且存在反应:
能溶于有机物TBP,且存在反应: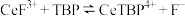 。“滤液A”中加入有机物TBP后的分离方法是
。“滤液A”中加入有机物TBP后的分离方法是________ ,“有机层B”中发生反应的离子方程式为________ 。水层中的一种溶质,理论上可以在工艺流程图中的________ 工序中循环利用,减小“调pH”工序中 的用量,节约生产成本。
的用量,节约生产成本。
(3)“调pH”中,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制pH大于
为沉淀完全),应控制pH大于________ (已知25℃时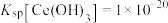 )。
)。
(4)“氧化”中,NaClO转化为NaCl,则氧化剂与还原剂的物质的量之比为________ 。
(5)二氧化铈立方晶胞如图所示,则铈原子Ce在晶胞中的位置是________ ;晶体中一个Ce周围与其最近的O的个数为________ 。
 )是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含
)是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含 、
、 等)为原料制备
等)为原料制备 的一种工艺流程如下图所示:
的一种工艺流程如下图所示: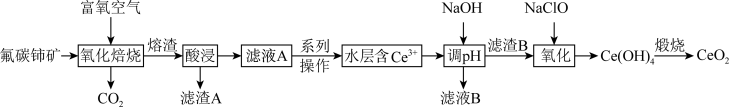
 和
和 ;②滤液A中含:
;②滤液A中含: 、
、 等离子。
等离子。回答下列问题:
(1)滤渣A的主要成分是
(2)“系列操作”包含以下几个过程:已知:
 不能溶于有机物TBP;
不能溶于有机物TBP; 能溶于有机物TBP,且存在反应:
能溶于有机物TBP,且存在反应: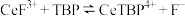 。“滤液A”中加入有机物TBP后的分离方法是
。“滤液A”中加入有机物TBP后的分离方法是 的用量,节约生产成本。
的用量,节约生产成本。
(3)“调pH”中,要使
 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制pH大于
为沉淀完全),应控制pH大于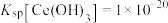 )。
)。(4)“氧化”中,NaClO转化为NaCl,则氧化剂与还原剂的物质的量之比为
(5)二氧化铈立方晶胞如图所示,则铈原子Ce在晶胞中的位置是

您最近一年使用:0次
2024-04-01更新
|
1261次组卷
|
7卷引用:广东省揭阳华侨高级中学2023-2024学年高三下学期第二次阶段(期中)考试化学试题
广东省揭阳华侨高级中学2023-2024学年高三下学期第二次阶段(期中)考试化学试题广东省韶关市2024届高三下学期综合测试(二)化学试题(已下线)题型10 工艺流程题(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)提升练07 工艺流程综合-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)压轴题11?无机化工流程综合分析(6大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)2024届云南省德宏师范高等专科学校附属天成中学高三下学期全真第三次模拟测理综试卷-高中化学(已下线)高二化学下学期期末押题卷02-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(江苏专用)
解题方法
7 . 下列说法正确的是
| A.冰融化的过程破坏了化学键 |
B. 分子中所有的原子均为8电子稳定结构 分子中所有的原子均为8电子稳定结构 |
| C.熔融状态下能导电的化合物不一定含离子键 |
D.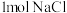 中约有 中约有 个 个 分子 分子 |
您最近一年使用:0次
8 . 下列各种说法正确的是
①合金材料可能含有非金属元素
②工业制玻璃和水泥均需要用到石灰石
③高纯度的硅广泛用于制作计算机芯片
④用锌与稀硫酸制氢气时,改用浓硫酸能加快生成氢气的速率
⑤铝用于软包装主要是利用了铝密度小的物理性质
⑥合成纤维和光导纤维都是新型无机非金属材料
⑦葡萄酒中通常含有微量SO2,既可以杀菌又可以防止营养成分被氧化
⑧在金属元素和非金属元素的分界线附近可以寻找制备半导体材料的元素
①合金材料可能含有非金属元素
②工业制玻璃和水泥均需要用到石灰石
③高纯度的硅广泛用于制作计算机芯片
④用锌与稀硫酸制氢气时,改用浓硫酸能加快生成氢气的速率
⑤铝用于软包装主要是利用了铝密度小的物理性质
⑥合成纤维和光导纤维都是新型无机非金属材料
⑦葡萄酒中通常含有微量SO2,既可以杀菌又可以防止营养成分被氧化
⑧在金属元素和非金属元素的分界线附近可以寻找制备半导体材料的元素
| A.①②③④⑦⑧ | B.①②③⑦⑧ |
| C.①③④⑤⑧ | D.①③⑤⑥⑧ |
您最近一年使用:0次
解题方法
9 . 回答下列问题。
(1)基态N原子的电子排布式为___________ 。基态P原子中,电子占据的最高能级原子轨道形状为___________ 。
(2)H2O中心原子杂化轨道类型为___________ ,说明H2O沸点大于H2S的原因___________ 。
(3)基态Ca原子价层电子由4s2状态变化为4s14p1状态所得原子光谱为___________ (填“发射”或“吸收”)光谱。
(4)下列氧原子电子排布图表示的状态中,能量最高的是___________ (填标号,下同),能量最低的是___________ 。
A.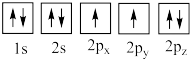 B.
B.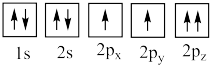
C. D.
D.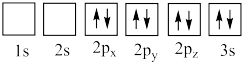
(1)基态N原子的电子排布式为
(2)H2O中心原子杂化轨道类型为
(3)基态Ca原子价层电子由4s2状态变化为4s14p1状态所得原子光谱为
(4)下列氧原子电子排布图表示的状态中,能量最高的是
A.
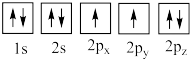 B.
B.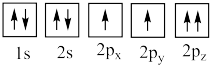
C.
 D.
D.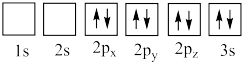
您最近一年使用:0次
2024-03-22更新
|
486次组卷
|
2卷引用:广东省普宁市勤建学校2023-2024学年高二下学期第一次月考化学试题
解题方法
10 . “五步产盐法”起源于山西运城,其生产工艺主要以集卤蒸发为主,盐池的浓卤水经过箩、调配、储卤、结晶、铲出五个步骤即可得到纯度高且颗粒大的食盐.《天工开物》中也有类似描述,“凡引水种盐,春间即为之,久则水成赤色.待夏秋之交,南风大起,则一宵结成.……但成盐时日,与不借南风则大异也”.已知:
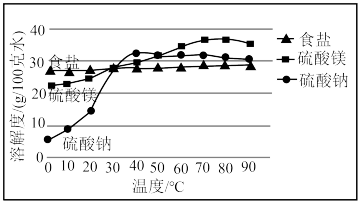
运城盐池卤水中三种主要成分溶解度随温度变化示意图
回答下列问题:
(1)为除去食盐中可能含有的少量 和
和 ,将其溶解后依次加入
,将其溶解后依次加入_________ 、 溶液后过滤,再加入适量的盐酸,蒸发结晶.
溶液后过滤,再加入适量的盐酸,蒸发结晶.
(2)运城盐池素有“夏产盐冬产硝”的说法,“夏产盐”的原理是___________________ (填操作名称,下同),“冬产硝”(主要成分为 )的原理是
)的原理是_______________ .“五步产盐法”最独特的妙处之一是在出盐前于卤水中浇洒适量淡水,由此得到的食盐晶体“质坚、粒大”且纯度较高,此法得到的食盐晶体粒大、质坚的原因是__________________________________________________ .
(3)经提纯得到的 与煤粉(主要成分为C)高温还原可制取一种重要的化工原料
与煤粉(主要成分为C)高温还原可制取一种重要的化工原料 ,同时生成无污染气体,该反应的化学方程式为
,同时生成无污染气体,该反应的化学方程式为________________________________ .
(4) 与
与 混合溶液中通入
混合溶液中通入 即可制得
即可制得 ,装置如图所示:
,装置如图所示:
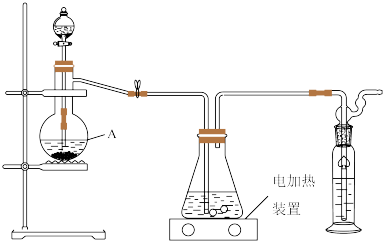
实验过程如下:打开分液漏斗活塞慢慢滴入70%的硫酸溶液,使产生的气体均匀通入 与
与 混合溶液,随着气体的通入逐渐有大量硫单质析出.继续通入气体,反应约一小时,溶液pH约等于7时(注意不要小于7),停止通气.
混合溶液,随着气体的通入逐渐有大量硫单质析出.继续通入气体,反应约一小时,溶液pH约等于7时(注意不要小于7),停止通气.
①仪器A的名称是____________ .
②锥形瓶内的反应大致可分为三步进行:
第一步:
第二步:
第三步:生成 反应的化学方程式为
反应的化学方程式为_________________ ,该实验过程中 的比例太低会导致产率过低的原因是
的比例太低会导致产率过低的原因是_________________________ .

运城盐池卤水中三种主要成分溶解度随温度变化示意图
回答下列问题:
(1)为除去食盐中可能含有的少量
 和
和 ,将其溶解后依次加入
,将其溶解后依次加入 溶液后过滤,再加入适量的盐酸,蒸发结晶.
溶液后过滤,再加入适量的盐酸,蒸发结晶.(2)运城盐池素有“夏产盐冬产硝”的说法,“夏产盐”的原理是
 )的原理是
)的原理是(3)经提纯得到的
 与煤粉(主要成分为C)高温还原可制取一种重要的化工原料
与煤粉(主要成分为C)高温还原可制取一种重要的化工原料 ,同时生成无污染气体,该反应的化学方程式为
,同时生成无污染气体,该反应的化学方程式为(4)
 与
与 混合溶液中通入
混合溶液中通入 即可制得
即可制得 ,装置如图所示:
,装置如图所示:
实验过程如下:打开分液漏斗活塞慢慢滴入70%的硫酸溶液,使产生的气体均匀通入
 与
与 混合溶液,随着气体的通入逐渐有大量硫单质析出.继续通入气体,反应约一小时,溶液pH约等于7时(注意不要小于7),停止通气.
混合溶液,随着气体的通入逐渐有大量硫单质析出.继续通入气体,反应约一小时,溶液pH约等于7时(注意不要小于7),停止通气.①仪器A的名称是
②锥形瓶内的反应大致可分为三步进行:
第一步:

第二步:

第三步:生成
 反应的化学方程式为
反应的化学方程式为 的比例太低会导致产率过低的原因是
的比例太低会导致产率过低的原因是
您最近一年使用:0次



