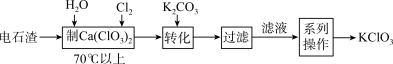
1 . 某化学兴趣小组利用如图装置制取氯气并探究其有关性质。______ 。
(2)在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是______ 。
(3)通入SO2和氯气一段时间后,甲同学在实验过程中发现品红溶液几乎不褪色,而乙同学的实验现象是品红溶液的颜色随时间的推移变得越来越浅。试根据该实验装置和两名同学的实验结果回答问题。
①试分析甲同学的实验过程中,品红溶液不褪色的原因:______ 。其涉及反应的离子方程式为______ 。
②乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅。其原因______ 。
(4)下列装置可用于尾气处理的是(夹持仪器已略去)______ (填字母)。______ 。
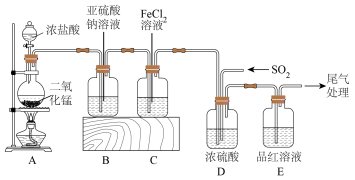
(2)在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是
(3)通入SO2和氯气一段时间后,甲同学在实验过程中发现品红溶液几乎不褪色,而乙同学的实验现象是品红溶液的颜色随时间的推移变得越来越浅。试根据该实验装置和两名同学的实验结果回答问题。
①试分析甲同学的实验过程中,品红溶液不褪色的原因:
②乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅。其原因
(4)下列装置可用于尾气处理的是(夹持仪器已略去)
a.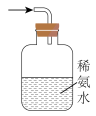 b.
b.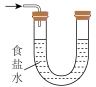 c.
c.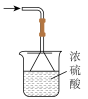 d.
d.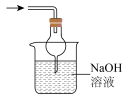
您最近一年使用:0次
解题方法
2 . 废物利用是实现绿色化学和节能减排的重要措施。电石渣[主要成分为Ca(OH)2]是氯碱工业的废料,某同学在实验室以电石渣为原料制取KClO3的流程如图所示: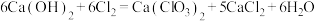 。
。
回答下列问题:
(1)KClO3中氯元素的化合价为___________ 价。
(2) KClO3可用于制备Cl2:KClO3+6HCl(浓)= +3Cl2↑+3H2O
①请补充完整反应方程式:___________ 。
②该反应的还原剂是___________ 。
(3)上述流程中,“转化”时发生反应的离子方程式为___________ 。
(4)一定量石灰乳中持续通入氯气发生反应,生成物中含氯离子仅有 、
、 、
、 ,且反应过程中不断释放热量。其中
,且反应过程中不断释放热量。其中 、
、 物质的量(n)与反应时间(t)曲线如图所示:
物质的量(n)与反应时间(t)曲线如图所示:___________ 。
②写出Ca(ClO)2的一种用途___________ 。
③若提高石灰乳中通入氯气的速度,则反应后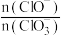
___________ 2(填“>”、“<”或“=”)。
④该石灰乳中Ca(OH)2的物质的量是___________ 。
A.1.5mol B.3mol C.5mol D.10mol
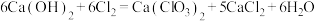 。
。回答下列问题:
(1)KClO3中氯元素的化合价为
(2) KClO3可用于制备Cl2:KClO3+6HCl(浓)= +3Cl2↑+3H2O
①请补充完整反应方程式:
②该反应的还原剂是
(3)上述流程中,“转化”时发生反应的离子方程式为
(4)一定量石灰乳中持续通入氯气发生反应,生成物中含氯离子仅有
 、
、 、
、 ,且反应过程中不断释放热量。其中
,且反应过程中不断释放热量。其中 、
、 物质的量(n)与反应时间(t)曲线如图所示:
物质的量(n)与反应时间(t)曲线如图所示: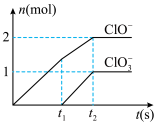
②写出Ca(ClO)2的一种用途
③若提高石灰乳中通入氯气的速度,则反应后
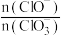
④该石灰乳中Ca(OH)2的物质的量是
A.1.5mol B.3mol C.5mol D.10mol
您最近一年使用:0次
解题方法
3 . “广东三宝”之一的新会陈皮是中国国家地理标志产品,在2009年被列入广东省非物质文化遗产。陈皮中含有的部分组成元素在周期表中的位置如下所示:
结合上述材料回答以下问题:
(1)陈皮中含有微量元素硒(Se)具有良好的抗氧化、抗肿瘤的作用。Se在元素周期表中的位置是___________ ,Se的最高价氧化物对应的水化物的化学式是___________ 。
(2)陈皮中含有的铁元素和铜元素在工业上应用广泛,如覆铜板制作印刷电路板时常用 溶液作为“腐蚀液”,写出制作原理的离子方程式
溶液作为“腐蚀液”,写出制作原理的离子方程式___________ , 的中子数是30,其电子数是
的中子数是30,其电子数是___________ 。
(3)下列由陈皮中所含元素组成的物质中,含有极性共价键的离子化合物是___________。
(4)简单氢化物的性质常被用于分析元素的性质,N和O的简单氢化物的稳定性顺序是___________ (用氢化物化学式比较)。
(5)依据上述元素在周期表中的位置,下列说法正确的有___________。
| H | |||||||||||||||||
| Li | C | N | O | ||||||||||||||
| Na | Mg | S | Cl | ||||||||||||||
| K | Ca | Fe | Cu | Se | |||||||||||||
(1)陈皮中含有微量元素硒(Se)具有良好的抗氧化、抗肿瘤的作用。Se在元素周期表中的位置是
(2)陈皮中含有的铁元素和铜元素在工业上应用广泛,如覆铜板制作印刷电路板时常用
 溶液作为“腐蚀液”,写出制作原理的离子方程式
溶液作为“腐蚀液”,写出制作原理的离子方程式 的中子数是30,其电子数是
的中子数是30,其电子数是(3)下列由陈皮中所含元素组成的物质中,含有极性共价键的离子化合物是___________。
| A.NaCl | B. | C. | D.NaOH |
(5)依据上述元素在周期表中的位置,下列说法正确的有___________。
| A.碱性:LiOH<NaOH | B.酸性: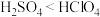 |
| C.原子半径:O<S<Cl | D.离子的还原性: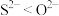 |
您最近一年使用:0次
解题方法
4 . 某硫酸厂用硫铁矿焙烧后的烧渣(成分为 、
、 、
、 )制备绿矾粗产品(
)制备绿矾粗产品(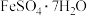 ),设计了如图流程:
),设计了如图流程: 性质稳定,不与强酸反应;
性质稳定,不与强酸反应;
②金属离子开始沉淀和沉淀完全时的pH:
回答下列问题:
(1)“试剂a”为___________。
(2)“酸浸”后溶液中存在的金属阳离子有___________ 。
(3)“还原”步骤中,溶液变为浅绿色,写出发生反应的离子方程式___________ 。
(4)滤渣的主要成分为___________ 。
(5)“调pH”是分离金属离子的重要步骤。
①欲使 完全沉淀,
完全沉淀, 未开始沉淀,此时pH为
未开始沉淀,此时pH为___________ 。
A.2.7~3.3 B.3.7~5.0 C.5.0~7.6 D.7.6~9.7
②写出生成 的离子方程式
的离子方程式___________ 。
(6)查阅资料发现, 在不同温度下结晶可得到不同的
在不同温度下结晶可得到不同的 水合物,其溶解度曲线如下图所示,制得“绿矾粗产品”应选择的最佳操作是
水合物,其溶解度曲线如下图所示,制得“绿矾粗产品”应选择的最佳操作是___________ 。
B.加热浓缩得到56℃饱和溶液,冷却结晶,过滤,洗涤,干燥
C.加热温度至略低于64℃浓缩、冷却至略高于57℃结晶,过滤,洗涤,干燥
 、
、 、
、 )制备绿矾粗产品(
)制备绿矾粗产品(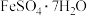 ),设计了如图流程:
),设计了如图流程: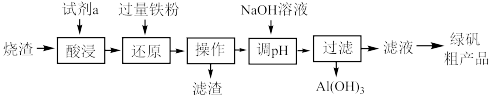
 性质稳定,不与强酸反应;
性质稳定,不与强酸反应;②金属离子开始沉淀和沉淀完全时的pH:
| 开始沉淀 | 完全沉淀 | |
 | 3.3 | 5.0 |
 | 2.7 | 3.7 |
 | 7.6 | 9.7 |
(1)“试剂a”为___________。
| A.HCl | B. | C. | D. |
(2)“酸浸”后溶液中存在的金属阳离子有
(3)“还原”步骤中,溶液变为浅绿色,写出发生反应的离子方程式
(4)滤渣的主要成分为
(5)“调pH”是分离金属离子的重要步骤。
①欲使
 完全沉淀,
完全沉淀, 未开始沉淀,此时pH为
未开始沉淀,此时pH为A.2.7~3.3 B.3.7~5.0 C.5.0~7.6 D.7.6~9.7
②写出生成
 的离子方程式
的离子方程式(6)查阅资料发现,
 在不同温度下结晶可得到不同的
在不同温度下结晶可得到不同的 水合物,其溶解度曲线如下图所示,制得“绿矾粗产品”应选择的最佳操作是
水合物,其溶解度曲线如下图所示,制得“绿矾粗产品”应选择的最佳操作是
B.加热浓缩得到56℃饱和溶液,冷却结晶,过滤,洗涤,干燥
C.加热温度至略低于64℃浓缩、冷却至略高于57℃结晶,过滤,洗涤,干燥
您最近一年使用:0次
5 . 我国是世界产盐大国,主要包括海盐、湖盐和井盐等。某同学进行粗盐提纯、溶液配制和纯度检验实验。
(一)粗盐的提纯
粗盐中含有泥沙、 、
、 、
、 等杂质,其提纯过程如下图所示:
等杂质,其提纯过程如下图所示:
(2)通HCl时溶液中有气泡产生,该反应的离子方程式为___________ 。
(3)操作X的步骤包括:___________ 、过滤、洗涤、干燥。
(二)溶液的配制
用制得的精盐配制 溶液,回答下列问题:
溶液,回答下列问题:
(4)实验中用到的玻璃仪器有:烧杯、量筒、胶头滴管、玻璃棒和___________ 。
(5)下列操作会使配得的NaCl溶液浓度偏低的有___________。
(三)纯度测定
取25.00mL所配溶液与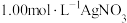 溶液反应。3次测定所消耗溶液的体积如下,回答下列问题:
溶液反应。3次测定所消耗溶液的体积如下,回答下列问题:
(6)平均消耗 溶液的体积为
溶液的体积为___________ mL。
(7)制得的NaCl的纯度是___________ 。
(一)粗盐的提纯
粗盐中含有泥沙、
 、
、 、
、 等杂质,其提纯过程如下图所示:
等杂质,其提纯过程如下图所示: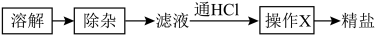
| 实验步骤 | 试剂 | 预期沉淀的离子 |
| 步骤1 |  | |
| 步骤2 | NaOH溶液 | |
| 步骤3 |
(2)通HCl时溶液中有气泡产生,该反应的离子方程式为
(3)操作X的步骤包括:
(二)溶液的配制
用制得的精盐配制
 溶液,回答下列问题:
溶液,回答下列问题:(4)实验中用到的玻璃仪器有:烧杯、量筒、胶头滴管、玻璃棒和
(5)下列操作会使配得的NaCl溶液浓度偏低的有___________。
| A.没有进行洗涤操作 |
| B.定容时俯视容量瓶的刻度线 |
| C.容量瓶中事先含有少量蒸馏水 |
| D.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线 |
(三)纯度测定
取25.00mL所配溶液与
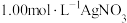 溶液反应。3次测定所消耗溶液的体积如下,回答下列问题:
溶液反应。3次测定所消耗溶液的体积如下,回答下列问题:| 测定次数 | 第1次 | 第2次 | 第3次 |
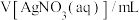 | 23.44 | 23.56 | 23.50 |
(6)平均消耗
 溶液的体积为
溶液的体积为(7)制得的NaCl的纯度是
您最近一年使用:0次
6 . 2023年诺贝尔化学奖颁发给研究量子点的三位科学家,日常生活中的电视屏幕和LED显示屏与量子点相关,一种LED器件材料的化合物为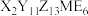 ,所含的5种元素位于主族,X、Y、M、E在同周期相邻位置且原子序数依次增大,Z单质是最轻的气体,E在地壳中含量最多。下列说法正确的是
,所含的5种元素位于主族,X、Y、M、E在同周期相邻位置且原子序数依次增大,Z单质是最轻的气体,E在地壳中含量最多。下列说法正确的是
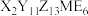 ,所含的5种元素位于主族,X、Y、M、E在同周期相邻位置且原子序数依次增大,Z单质是最轻的气体,E在地壳中含量最多。下列说法正确的是
,所含的5种元素位于主族,X、Y、M、E在同周期相邻位置且原子序数依次增大,Z单质是最轻的气体,E在地壳中含量最多。下列说法正确的是A.电负性: |
| B.Y、M、E的简单氢化物均为极性分子 |
C.第一电离能: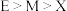 |
D.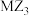 和 和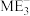 中心原子的杂化类型相同 中心原子的杂化类型相同 |
您最近一年使用:0次
2024-08-25更新
|
89次组卷
|
2卷引用:广东省江门市2024届高三上学期11月大联考化学试题
解题方法
7 . 以 为正极材料的锂电池应用广泛,一种从该种废旧锂电池中综合回收
为正极材料的锂电池应用广泛,一种从该种废旧锂电池中综合回收 和
和 并进行
并进行 再生的工艺流程如图所示:
再生的工艺流程如图所示:
(1) 中,基态
中,基态 的价电子轨道表示式为
的价电子轨道表示式为_________ , 的空间结构为
的空间结构为_________ 。
(2)“浸出”时 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(3)“调 ”时调节
”时调节 有利于提高锂的浸出率,其原因是
有利于提高锂的浸出率,其原因是______________ 。
(4)为提高产品纯度选择 作为沉锂试剂,写出“沉锂”时发生反应的离子方程式:
作为沉锂试剂,写出“沉锂”时发生反应的离子方程式:______________ 。
(5)“煅烧2”加入葡萄糖的作用是__________ ,若有 葡萄糖参与反应,理论上可制备
葡萄糖参与反应,理论上可制备__________ 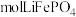 。
。
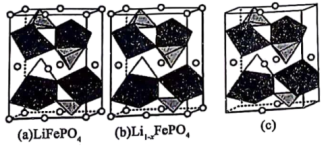
(6)图(a)为正极材料 的晶胞结构,则每个晶胞中含有的
的晶胞结构,则每个晶胞中含有的 的单元数为
的单元数为________ ;若从图(a)所示结构转化为图(b)所示结构,此过程电池_______ (填“充电”或“放电”);图(c)所示状态时,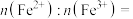
______________ 。
 为正极材料的锂电池应用广泛,一种从该种废旧锂电池中综合回收
为正极材料的锂电池应用广泛,一种从该种废旧锂电池中综合回收 和
和 并进行
并进行 再生的工艺流程如图所示:
再生的工艺流程如图所示: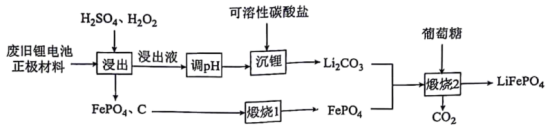
(1)
 中,基态
中,基态 的价电子轨道表示式为
的价电子轨道表示式为 的空间结构为
的空间结构为(2)“浸出”时
 发生反应的化学方程式为
发生反应的化学方程式为(3)“调
 ”时调节
”时调节 有利于提高锂的浸出率,其原因是
有利于提高锂的浸出率,其原因是(4)为提高产品纯度选择
 作为沉锂试剂,写出“沉锂”时发生反应的离子方程式:
作为沉锂试剂,写出“沉锂”时发生反应的离子方程式:(5)“煅烧2”加入葡萄糖的作用是
 葡萄糖参与反应,理论上可制备
葡萄糖参与反应,理论上可制备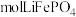 。
。(6)图(a)为正极材料
 的晶胞结构,则每个晶胞中含有的
的晶胞结构,则每个晶胞中含有的 的单元数为
的单元数为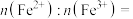
您最近一年使用:0次
解题方法
8 . 按如图所示的装置进行实验制备 并对其性质进行探究,将硫酸全部加入锥形瓶中,关闭活塞。下列说法错误的是
并对其性质进行探究,将硫酸全部加入锥形瓶中,关闭活塞。下列说法错误的是
 并对其性质进行探究,将硫酸全部加入锥形瓶中,关闭活塞。下列说法错误的是
并对其性质进行探究,将硫酸全部加入锥形瓶中,关闭活塞。下列说法错误的是 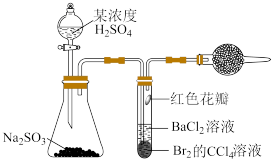
A.该制备 的原理为强酸制弱酸 的原理为强酸制弱酸 |
| B.对锥形瓶进行水浴加热,红色花瓣褪色更快 |
C.一段时间后试管内有白色沉淀 生成,说明 生成,说明 具有还原性 具有还原性 |
D.干燥管中可盛放 进行尾气处理 进行尾气处理 |
您最近一年使用:0次
9 . 化学之美,美在其外,更深藏于内。下列说法正确的是
| A.日照香炉生紫烟与胶体的丁达尔效应有关 |
| B.节日燃放五颜六色的烟花与原子吸收光谱的原理相同 |
| C.鸡蛋白遇浓硫酸加热后呈现黄色 |
| D.海上丝绸贸易用于交易的银锭中存在离子键 |
您最近一年使用:0次
10 . 人居环境优化、提升农产品产量质量、打造特色产业是乡村振兴的重要内容,下列说法正确的是
A.乡村石墙上用铁红为颜料作画,铁红的化学式为 |
| B.修建乡村道路需要用到水泥,水泥中所含的熟石膏属于碱类物质 |
| C.制作特产“企炉饼”需要用到糖,糖类均能水解 |
D.某些特产食品中适当添加 , , 可以起到防腐和抗氧化的作用 可以起到防腐和抗氧化的作用 |
您最近一年使用:0次



