解题方法
1 . 下列劳动项目与所涉及的化学知识没有关联的是
| 选项 | 劳动项目 | 化学知识 |
| A | 除去锅炉中水垢时,先用 溶液处理 溶液处理 |  在酸中溶解性比 在酸中溶解性比 大 大 |
| B | 向豆浆中加入 溶液制作豆腐 溶液制作豆腐 | 蛋白质在一些化学试剂中发生变性 |
| C | 海水晒盐得到有一定几何外形的食盐颗粒 | 晶体形成过程存在自范性 |
| D | 用高度酒浸泡药材生产药酒 | 乙醇能溶解多种有机物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 某校化学学习小组探究 与
与 溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有
溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有 固体。回答下列问题:
固体。回答下列问题:
(1)写出实验中制备 的化学方程式
的化学方程式________ 。
(2)配制100mL
 溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和
溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和________ 。
【实验探究】
向3mL
 溶液中通入
溶液中通入 ,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
猜想1: 水解产生了红棕色的
水解产生了红棕色的 胶体;
胶体;
猜想2: 与溶液中某种
与溶液中某种 价含硫微粒形成了红棕色的配合物。
价含硫微粒形成了红棕色的配合物。
(3)为验证上述猜想,甲同学用激光笔照射该红棕色溶液,________ ,证明猜想1不成立。
(4)乙同学查阅文献得知猜想2正确,并设计了下表3组实验,以确定红棕色配合物的配体是 、
、 、
、 中的哪一种(实验均在常温下进行)。
中的哪一种(实验均在常温下进行)。
已知:常温下,溶液中 价含硫微粒物质的量分数随pH变化曲线如图所示。
价含硫微粒物质的量分数随pH变化曲线如图所示。________ (填写微粒符号),依据的实验证据是________ 。
(5)丙同学查阅资料得知:
利用分光光度计可测定溶液中有色物质的吸光度,吸光度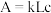 ,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
丙同学经过思考,认为乙同学的实验方案不严谨,除了pH会影响溶液红棕色的深浅,还有一个因素也可能会影响溶液红棕色的深浅。于是设计如下实验进行探究,请帮助该同学完成实验方案,填写下表中空白处。
实验结果讨论:若 ,则该因素不影响溶液红棕色的深浅;若
,则该因素不影响溶液红棕色的深浅;若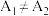 ,则该因素会影响溶液红棕色的深浅。
,则该因素会影响溶液红棕色的深浅。
(6)丁同学查阅资料得知:
配合物在溶液中存在解离平衡,如: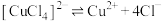 。
。
丁同学设计实验,利用分光光度计测定上述溶液中红棕色物质的吸光度,证明解离平衡的存在。请完成表中内容。
实验限选试剂为: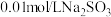 溶液,
溶液,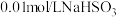 溶液,
溶液, 固体,
固体,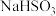 固体
固体
 与
与 溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有
溶液的反应,装置如下图所示,分液漏斗中盛有浓硫酸,锥形瓶中装有 固体。回答下列问题:
固体。回答下列问题: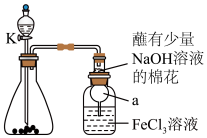
(1)写出实验中制备
 的化学方程式
的化学方程式(2)配制100mL

 溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和
溶液用到的主要玻璃仪器为烧杯、玻璃棒、胶头滴管和【实验探究】
向3mL

 溶液中通入
溶液中通入 ,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:
,观察到溶液立即由黄色变成红棕色,放置12小时后,,红棕色消失,溶液变为浅绿色。结合已有知识,针对溶液呈红棕色学习小组提出以下猜想:猜想1:
 水解产生了红棕色的
水解产生了红棕色的 胶体;
胶体;猜想2:
 与溶液中某种
与溶液中某种 价含硫微粒形成了红棕色的配合物。
价含硫微粒形成了红棕色的配合物。(3)为验证上述猜想,甲同学用激光笔照射该红棕色溶液,
(4)乙同学查阅文献得知猜想2正确,并设计了下表3组实验,以确定红棕色配合物的配体是
 、
、 、
、 中的哪一种(实验均在常温下进行)。
中的哪一种(实验均在常温下进行)。组别 | 溶液1(1mL) | 溶液2(2mL) | 现象 |
a |
|
| 溶液1和溶液2混合后,组别a、b、c所得溶液红棕色依次加深。 |
b |  的饱和溶液,用 的饱和溶液,用 固体调节. 固体调节. | ||
c |  的饱和溶液,用 的饱和溶液,用 固体调节 固体调节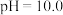 |
 价含硫微粒物质的量分数随pH变化曲线如图所示。
价含硫微粒物质的量分数随pH变化曲线如图所示。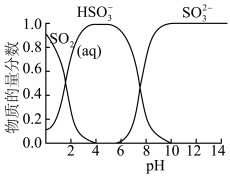
(5)丙同学查阅资料得知:
利用分光光度计可测定溶液中有色物质的吸光度,吸光度
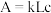 ,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。
,其中k为摩尔吸收系数;L为液层厚度即光路长度,在实验中液层厚度保持一致;c为有色物质的浓度。丙同学经过思考,认为乙同学的实验方案不严谨,除了pH会影响溶液红棕色的深浅,还有一个因素也可能会影响溶液红棕色的深浅。于是设计如下实验进行探究,请帮助该同学完成实验方案,填写下表中空白处。
实验序号 | 操作 | 吸光度 |
1 | 把1mL 0.1mol/L 溶液与2mL 溶液与2mL 饱和溶液混合均匀,溶液变成红棕色,测定溶液中红棕色物质的吸光度。 饱和溶液混合均匀,溶液变成红棕色,测定溶液中红棕色物质的吸光度。 |
|
2 |
|
 ,则该因素不影响溶液红棕色的深浅;若
,则该因素不影响溶液红棕色的深浅;若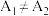 ,则该因素会影响溶液红棕色的深浅。
,则该因素会影响溶液红棕色的深浅。(6)丁同学查阅资料得知:
配合物在溶液中存在解离平衡,如:
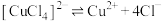 。
。丁同学设计实验,利用分光光度计测定上述溶液中红棕色物质的吸光度,证明解离平衡的存在。请完成表中内容。
实验限选试剂为:
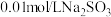 溶液,
溶液,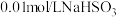 溶液,
溶液, 固体,
固体,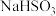 固体
固体实验序号 | 操作 | 吸光度 | 结论 |
3 | 向3mL 0.1mol/L 溶液中通入 溶液中通入 ,溶液立即由黄色变成红棕色,测定溶液中红棕色物质的吸光度 ,溶液立即由黄色变成红棕色,测定溶液中红棕色物质的吸光度 |
| |
4 |
  (填“大于”、“小于”或“等于”) (填“大于”、“小于”或“等于”) | 平衡向 |
您最近一年使用:0次
3 . “回望飞天路,逐梦新征程”。下列说法正确的是
| A.月球中的3He与地球上的3H互为同位素 |
| B.“太空快递小哥”天舟六号壳体材料主要为铝合金,其强度大于纯铝 |
C.“问天”实验舱使用砷化镓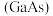 太阳能电池,其中 太阳能电池,其中 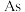 位于周期表的d区 位于周期表的d区 |
| D.长征七号遥七运载火箭采用液氧、煤油等燃料作为推进剂,液氧和煤油均属于混合物 |
您最近一年使用:0次
2024-04-16更新
|
477次组卷
|
2卷引用:广东省韶关市2023-2024学年高三上学期第一次综合检测化学试题
4 . 依据图中氮元素及其化合物的转化关系,回答下列问题:______ 。
(2)回答下列关于 的问题:
的问题:
①利用下列方法制氨气,其中合理的是______ (填字母)。
A.将浓氨水滴入氢氧化钠固体中
B.将氯化铵稀溶液滴入氧化钙固体中
C.将氯化铵固体加热分解
D.加热浓氨水
E.将浓氨水滴入碱石灰固体中
②氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:______ 。
③ 、
、 合成
合成 的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是
的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是______ 。
A. B.
B.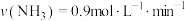
C.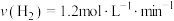 D.
D.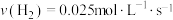
(3)下列关于NO、 的问题:
的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体C0和NO反应可转化为无害气体排放,写出相关反应的化学方程式:______ 。
②NO和 按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:______ 。
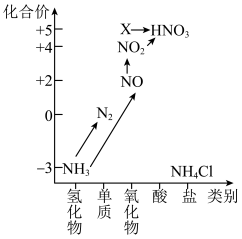
(2)回答下列关于
 的问题:
的问题:①利用下列方法制氨气,其中合理的是
A.将浓氨水滴入氢氧化钠固体中
B.将氯化铵稀溶液滴入氧化钙固体中
C.将氯化铵固体加热分解
D.加热浓氨水
E.将浓氨水滴入碱石灰固体中
②氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:
③
 、
、 合成
合成 的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是
的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是A.
 B.
B.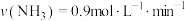
C.
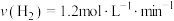 D.
D.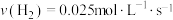
(3)下列关于NO、
 的问题:
的问题:①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体C0和NO反应可转化为无害气体排放,写出相关反应的化学方程式:
②NO和
 按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
您最近一年使用:0次
解题方法
5 . H2O2俗称双氧水,是常用的绿色氧化剂,在生产和生活中发挥重要的作用。
(1)富勒烯C60颗粒对H2O2液相氧化:SO2具有明显的促进效果,该反应机理和能量变化如下:
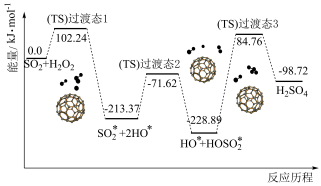
①H2O2液相氧化:SO2生成H2SO4的热化学方程式为________ 。
②图示历程包含________ 个基元反应,写出决速步骤的化学方程式________________ 。
③C60间的作用力是________ 。
(2) H2O2可用于工业源氮氧化物(NOx)的催化氧化,H2O2去除NO的反应存在平衡:
(i)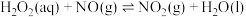
(ii)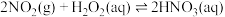
(iii)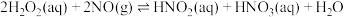
(iv)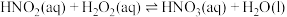
①上述反应体系在一定条件下建立平衡后,下列说法正确的有________ (填序号)。
A.其他条件不变时,温度越高,NO的转化率越大
B.加入催化剂,c(HNO3)与c(HNO2)比值保持不变
C.恒温恒压下,充入Ar,平衡(i)、(ii)向正反应方向移动
D.增大H2O2浓度,反应(i)、(ii)、(iii)、(iv)正反应速率都增加
②一定范围内,催化剂光热协同辅助H2O2降解NO的去除率变化如图甲所示,NO去除率最佳的反应条件为________ 。
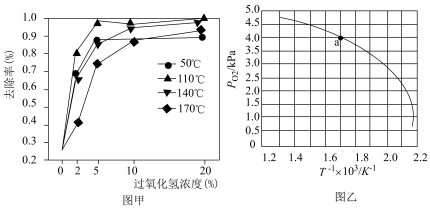
(3)过碳酸钠(2Na2CO3∙3H2O2)又称固体过氧化氢,是碳酸钠和过氧化氢的加成复合物。将2Na2CO3∙3H2O2置入真空的刚性容器中,升高温度发生分解反应:
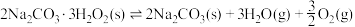 平衡时
平衡时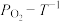 的关系如上图乙所示。a点时,该反应的平衡总压=
的关系如上图乙所示。a点时,该反应的平衡总压=________ kPa,平衡常数Kp=________ 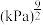 (列出算式),Kp随温度升高而
(列出算式),Kp随温度升高而________ (填“增大”、“减少”或“不变”)。
(1)富勒烯C60颗粒对H2O2液相氧化:SO2具有明显的促进效果,该反应机理和能量变化如下:

①H2O2液相氧化:SO2生成H2SO4的热化学方程式为
②图示历程包含
③C60间的作用力是
(2) H2O2可用于工业源氮氧化物(NOx)的催化氧化,H2O2去除NO的反应存在平衡:
(i)
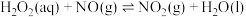
(ii)
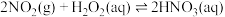
(iii)
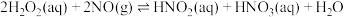
(iv)
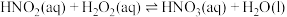
①上述反应体系在一定条件下建立平衡后,下列说法正确的有
A.其他条件不变时,温度越高,NO的转化率越大
B.加入催化剂,c(HNO3)与c(HNO2)比值保持不变
C.恒温恒压下,充入Ar,平衡(i)、(ii)向正反应方向移动
D.增大H2O2浓度,反应(i)、(ii)、(iii)、(iv)正反应速率都增加
②一定范围内,催化剂光热协同辅助H2O2降解NO的去除率变化如图甲所示,NO去除率最佳的反应条件为

(3)过碳酸钠(2Na2CO3∙3H2O2)又称固体过氧化氢,是碳酸钠和过氧化氢的加成复合物。将2Na2CO3∙3H2O2置入真空的刚性容器中,升高温度发生分解反应:
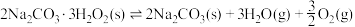 平衡时
平衡时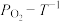 的关系如上图乙所示。a点时,该反应的平衡总压=
的关系如上图乙所示。a点时,该反应的平衡总压=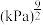 (列出算式),Kp随温度升高而
(列出算式),Kp随温度升高而
您最近一年使用:0次
解题方法
6 . 百年变局,科技创新是“关键变量”。下列说法不正确的是
| A.手机芯片的主要成分硅属于共价晶体 |
| B.C919大飞机的燃料煤油属于混合物 |
| C.新能源汽车的锂电池充电时将化学能转化为电能 |
| D.奋斗者号潜水器使用钛合金外壳利用了合金的高强度特点 |
您最近一年使用:0次
7 . 化学无处不在,下列有关说法正确的是
| A.淀粉、纤维素、油脂均属于天然高分子 |
| B.炒菜后铁锅不及时清理容易生锈,因为潮湿环境中铁锅发生析氢腐蚀 |
| C.打开汽水瓶盖有大量气泡冒出,可用勒夏特列原理解释 |
| D.向鸡蛋清溶液中加入食盐浓溶液有白色沉淀析出,因为食盐能使蛋白质变性 |
您最近一年使用:0次
8 . 劳动创造美好生活。下列生活、生产活动中,没有运用相应化学原理的是
选项 | 生活、生产活动 | 化学原理 |
A | 施肥时草木灰和铵态氮肥不能混合使用 |  溶液与铵盐发生双水解 溶液与铵盐发生双水解 |
B | 葡萄糖与银氨溶液制银镜 | 葡萄糖具有还原性 |
C | 液氨常用作制冷剂 | 液氨汽化时吸收大量的热 |
D | 漂白粉漂白有色物质放置一段时间后效果更好 |  酸性强于 酸性强于 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 牙膏中常加入含氟物质预防龋齿 | 氟磷灰石的溶解度小于羟基磷灰石 |
B | 气态氢化物稳定性: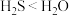 | 分子间作用力: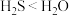 |
C | 电解食盐水制备氯气和氢氧化钠 | 氯气和氢氧化钠溶液反应制备漂白液 |
D | 饱和 溶液导电性比饱和 溶液导电性比饱和 溶液强 溶液强 |  溶液碱性强于 溶液碱性强于 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 二氧化铈( )是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含
)是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含 、
、 等)为原料制备
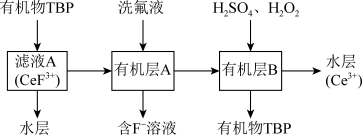
等)为原料制备 的一种工艺流程如下图所示:
的一种工艺流程如下图所示: 和
和 ;②滤液A中含:
;②滤液A中含: 、
、 等离子。
等离子。
回答下列问题:
(1)滤渣A的主要成分是________ (填化学式);“酸浸”不用盐酸的理由是________ (答一点即可)。
(2)“系列操作”包含以下几个过程:已知: 不能溶于有机物TBP;
不能溶于有机物TBP; 能溶于有机物TBP,且存在反应:
能溶于有机物TBP,且存在反应: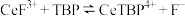 。“滤液A”中加入有机物TBP后的分离方法是
。“滤液A”中加入有机物TBP后的分离方法是________ ,“有机层B”中发生反应的离子方程式为________ 。水层中的一种溶质,理论上可以在工艺流程图中的________ 工序中循环利用,减小“调pH”工序中 的用量,节约生产成本。
的用量,节约生产成本。
(3)“调pH”中,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制pH大于
为沉淀完全),应控制pH大于________ (已知25℃时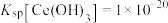 )。
)。
(4)“氧化”中,NaClO转化为NaCl,则氧化剂与还原剂的物质的量之比为________ 。
(5)二氧化铈立方晶胞如图所示,则铈原子Ce在晶胞中的位置是________ ;晶体中一个Ce周围与其最近的O的个数为________ 。
 )是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含
)是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含 、
、 等)为原料制备
等)为原料制备 的一种工艺流程如下图所示:
的一种工艺流程如下图所示: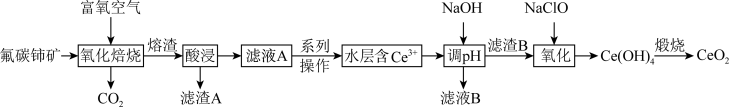
 和
和 ;②滤液A中含:
;②滤液A中含: 、
、 等离子。
等离子。回答下列问题:
(1)滤渣A的主要成分是
(2)“系列操作”包含以下几个过程:已知:
 不能溶于有机物TBP;
不能溶于有机物TBP; 能溶于有机物TBP,且存在反应:
能溶于有机物TBP,且存在反应: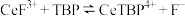 。“滤液A”中加入有机物TBP后的分离方法是
。“滤液A”中加入有机物TBP后的分离方法是 的用量,节约生产成本。
的用量,节约生产成本。
(3)“调pH”中,要使
 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制pH大于
为沉淀完全),应控制pH大于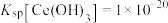 )。
)。(4)“氧化”中,NaClO转化为NaCl,则氧化剂与还原剂的物质的量之比为
(5)二氧化铈立方晶胞如图所示,则铈原子Ce在晶胞中的位置是

您最近一年使用:0次
2024-04-01更新
|
1236次组卷
|
7卷引用:广东省韶关市2024届高三下学期综合测试(二)化学试题
广东省韶关市2024届高三下学期综合测试(二)化学试题(已下线)题型10 工艺流程题(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)提升练07 工艺流程综合-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)广东省揭阳华侨高级中学2023-2024学年高三下学期第二次阶段(期中)考试化学试题(已下线)压轴题11?无机化工流程综合分析(6大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)2024届云南省德宏师范高等专科学校附属天成中学高三下学期全真第三次模拟测理综试卷-高中化学(已下线)高二化学下学期期末押题卷02-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(江苏专用)

 溶液
溶液



