名校
解题方法
1 . 有机物的种类多,在日常生活中有重要的用途。请回答下列问题:_____ 。
(2)请用系统命名法命名有机物②_____ 。
(3)⑤与⑦发生共聚反应的化学方程式_____ 。
(4)属于非极性分子的是_____ (填序号)。
(5)⑥中基态氧原子的核外电子的空间运动状态有_____ 种。
(6)硼在成键时能将一个2s电子激发进入2p能级参与形成化学键,请写出该激发态原子价电子轨道表示式:_____ ,该过程形成的原子光谱为_____ (填“吸收”或“发射”)光谱。
①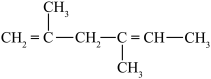 ;②
;②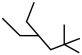 ;③
;③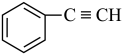 ;④
;④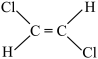 ;⑤
;⑤ ;⑥
;⑥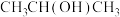 ;⑦
;⑦
(2)请用系统命名法命名有机物②
(3)⑤与⑦发生共聚反应的化学方程式
(4)属于非极性分子的是
(5)⑥中基态氧原子的核外电子的空间运动状态有
(6)硼在成键时能将一个2s电子激发进入2p能级参与形成化学键,请写出该激发态原子价电子轨道表示式:
您最近一年使用:0次
名校
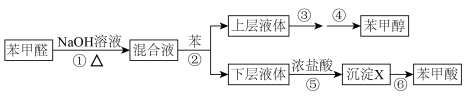
2 . Ⅰ.制备苯甲醇和苯甲酸的实验流程及涉及的主要实验装置(部分加热和固定装置已略)如图:_________________ ,仪器B的名称_____________________ 。
(2)第①步所用装置(如图),用搅拌器的目的是_____________ 。_____________ 。
(4)第⑥步的操作名称是_____________ 。
Ⅱ.铬的化合物氯化铬酰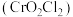 ,熔点
,熔点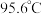 、沸点
、沸点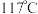 ,易溶于
,易溶于 ,可作为化工生产中的氧化剂。能通过反应
,可作为化工生产中的氧化剂。能通过反应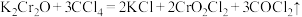 制备。
制备。
(5)固态 属于
属于_____________ 晶体。
(6)基态氯原子核外电子运动状态有_________ 种。
(7)基态钾原子核外电子排布式为_____________________________________ 。
(8)化合物 中存在的共价键类型是
中存在的共价键类型是_________________ 。(填 键或
键或 键)
键)
(9)氧族元素氢化物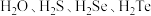 的熔沸点由高到低排列顺序为:
的熔沸点由高到低排列顺序为:_____________________ 。
(2)第①步所用装置(如图),用搅拌器的目的是

(4)第⑥步的操作名称是
Ⅱ.铬的化合物氯化铬酰
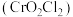 ,熔点
,熔点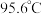 、沸点
、沸点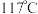 ,易溶于
,易溶于 ,可作为化工生产中的氧化剂。能通过反应
,可作为化工生产中的氧化剂。能通过反应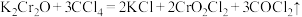 制备。
制备。(5)固态
 属于
属于(6)基态氯原子核外电子运动状态有
(7)基态钾原子核外电子排布式为
(8)化合物
 中存在的共价键类型是
中存在的共价键类型是 键或
键或 键)
键)(9)氧族元素氢化物
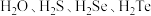 的熔沸点由高到低排列顺序为:
的熔沸点由高到低排列顺序为:
您最近一年使用:0次
名校
3 . 海水是巨大的资源宝库,工业上从海水中获取某些重要化工原料的流程如下图示。 、
、 和
和 等。回答下列问题:
等。回答下列问题:
(1)请列举除蒸馏法外海水淡化的一种方法:____________________ 。
(2)试剂1最好选用__________ (填编号)。
a. b.
b. c.
c. d.NaOH
d.NaOH
(3)提取溴单质时,往苦卤中通入氯气和酸,其酸化的目的是____________________ 。
(4)将吹出后的含 的空气按一定速率通入吸收塔,用
的空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。
和水进行吸收,吸收后的空气进行循环利用。
①流程中可用热空气吹出溴的原因为_____________________ 。
②“吸收塔”内发生反应的离子方程式:_____________________ 。
③流程中不是将酸和氯气氧化后的苦卤直接蒸馏,而是经过“空气吹出”、“二氧化硫吸收”、“氢气氧化”再蒸馏得到液溴,目的是_____________________ 。
(5)检验吸收塔里的溶液是否含 的方法是
的方法是_______________________ 。
(6)海带灰中富含以 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如图所示:
的途径如图所示:__________ (填一种仪器名称)中加热灼烧。
②向酸化的滤液中加入过氧化氢溶液,可将 氧化为
氧化为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:__________________ 。

 、
、 和
和 等。回答下列问题:
等。回答下列问题:(1)请列举除蒸馏法外海水淡化的一种方法:
(2)试剂1最好选用
a.
 b.
b. c.
c. d.NaOH
d.NaOH(3)提取溴单质时,往苦卤中通入氯气和酸,其酸化的目的是
(4)将吹出后的含
 的空气按一定速率通入吸收塔,用
的空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。
和水进行吸收,吸收后的空气进行循环利用。①流程中可用热空气吹出溴的原因为
②“吸收塔”内发生反应的离子方程式:
③流程中不是将酸和氯气氧化后的苦卤直接蒸馏,而是经过“空气吹出”、“二氧化硫吸收”、“氢气氧化”再蒸馏得到液溴,目的是
(5)检验吸收塔里的溶液是否含
 的方法是
的方法是(6)海带灰中富含以
 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如图所示:
的途径如图所示: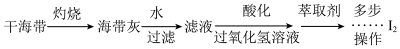
②向酸化的滤液中加入过氧化氢溶液,可将
 氧化为
氧化为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:
您最近一年使用:0次
名校
4 . 按要求回答下列问题:
(1)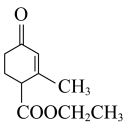 中含有的含氧官能团的名称为
中含有的含氧官能团的名称为___________ 。
(2)某有机物结构如图所示,下列说法正确的是___________ (填序号)。
③分子中C原子的杂化方式为 杂化 ④该分子是非极性分子
杂化 ④该分子是非极性分子
(3)TiO2是环境友好材料,能光催化降解有机物。纳米TiO2催化处理污水的一个实例如图所示。___________ ;化合物乙中有___________ 个手性碳原子。
(4)有A、B两种烃,已知:
( )B完全燃烧的产物
)B完全燃烧的产物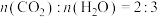 。
。
( )A是B分子中的氢原子全部被甲基取代后的产物;A遇
)A是B分子中的氢原子全部被甲基取代后的产物;A遇 的
的 溶液不褪色,其一氯代物只有一种。
溶液不褪色,其一氯代物只有一种。
①写出B与溴在光照下的反应方程式___________ (只写一取代)。
②A的结构简式为___________ ,系统命名为___________ 。
(1)
 中含有的含氧官能团的名称为
中含有的含氧官能团的名称为(2)某有机物结构如图所示,下列说法正确的是
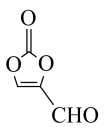
③分子中C原子的杂化方式为
 杂化 ④该分子是非极性分子
杂化 ④该分子是非极性分子(3)TiO2是环境友好材料,能光催化降解有机物。纳米TiO2催化处理污水的一个实例如图所示。

(4)有A、B两种烃,已知:
(
 )B完全燃烧的产物
)B完全燃烧的产物 。
。(
 )A是B分子中的氢原子全部被甲基取代后的产物;A遇
)A是B分子中的氢原子全部被甲基取代后的产物;A遇 的
的 溶液不褪色,其一氯代物只有一种。
溶液不褪色,其一氯代物只有一种。①写出B与溴在光照下的反应方程式
②A的结构简式为
您最近一年使用:0次
名校
解题方法
5 . 随着奥密克戎变异株致病性的减弱和疫苗接种的普及,以及防控经验的积累,我国疫情防控在不断的“放开”与“优化”。布洛芬、阿司匹林、乙酰氨基酚等解热镇痛药成为自我防疫家中常备药物。下列说法正确的是
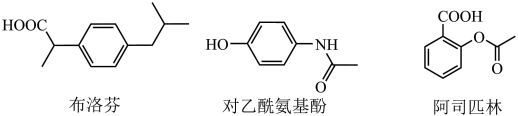
| A.阿司匹林分子中含有三种官能团 |
| B.可以通过红外光谱来区分布洛芬和对乙酰氨基酚 |
| C.布洛芬分子核磁共振氢谱图中有7个吸收峰 |
| D.对乙酰氨基酚分子的质谱中最大质荷比为137 |
您最近一年使用:0次
解题方法
6 . 二氧化硫是重要的化工原料。某实验小组欲制备SO2并探究其相关反应。
Ⅰ.SO2的制备
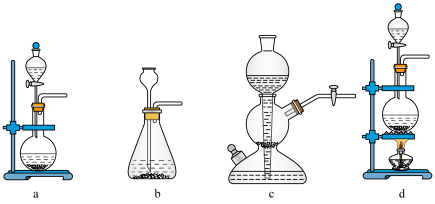
(1)实验小组以亚硫酸钠(Na2SO3)粉末和70%的硫酸为原料制取SO2,并要求能够控制反应速率,下列可选用的仪器是___________ (填标号)。
实验事实:小组同学向1mL0.5mol/LFeCl3溶液中通入SO2至饱和,溶液先变成红色,静置5min后溶液红色变浅,慢慢变为黄色,静置9h后溶液变为绿色。
提出问题:溶液变为红色与什么微粒有关?
查阅资料:①Fe3+易与阴离子形成配合物,且Fe(Ⅲ)配合物常呈现特殊颜色。
②SO2溶液中,存在的含有硫元素的微粒有SO2、H2SO3、 和
和 。
。
提出猜想:a.溶液变为红色与 有关;
有关;
b.溶液变为红色与 有关。
有关。
实验验证:为验证猜想,小组同学做了如下实验。
(2)完成表格:实验②中加入___________ 溶液。
上述两个实验中溶液都变为红色,因此无法得出实验结论。
进一步验证:为进一步验证猜想,小组同学配制系列溶液并测量其吸光度,绘制出右图曲线。
参比溶液:0.5mL1mol/LFeCl3溶液+0.5mL1mol/LNa2SO3溶液+7mL蒸馏水
图中A、B、C三点对应加入各试剂的体积如表所示。
说明:①已知吸光度大小与溶液中红色物质浓度成正比。②参比溶液的作用是空白对照,设定参比溶液的吸光度为0。
(3)补充上表中数值,其中a=___________ ,b=___________ 。
实验结论
(4)根据以上实验,可以推测:溶液变为红色与___________ (填离子符号)有关。
拓展探究
将静置9h后变为绿色的溶液分为两份,向其中一份溶液中滴加铁氰化钾溶液,有蓝色沉淀生成;向另一份溶液中滴加盐酸酸化的氯化钡溶液,有白色沉淀生成。
(5)①写出溶液变为绿色所发生氧化还原反应的离子方程式:___________ 。
②试从平衡移动的角度,分析溶液红色变浅直至消失的原因:___________ 。
(6)写出二氧化硫在生产生活中的一种应用:___________ 。
Ⅰ.SO2的制备
(1)实验小组以亚硫酸钠(Na2SO3)粉末和70%的硫酸为原料制取SO2,并要求能够控制反应速率,下列可选用的仪器是
实验事实:小组同学向1mL0.5mol/LFeCl3溶液中通入SO2至饱和,溶液先变成红色,静置5min后溶液红色变浅,慢慢变为黄色,静置9h后溶液变为绿色。
提出问题:溶液变为红色与什么微粒有关?
查阅资料:①Fe3+易与阴离子形成配合物,且Fe(Ⅲ)配合物常呈现特殊颜色。
②SO2溶液中,存在的含有硫元素的微粒有SO2、H2SO3、
 和
和 。
。提出猜想:a.溶液变为红色与
 有关;
有关;b.溶液变为红色与
 有关。
有关。实验验证:为验证猜想,小组同学做了如下实验。
| 实验 | 实验操作 | 实验现象 |
| ① | 取1mL1mol/LFeCl3溶液于试管中,加入3mL1mol/LNa2SO3溶液,观察5min内的颜色变化 | 溶液变为红色 |
| ② | 取1mL1mol/LFeCl3溶液于试管中,加入___________溶液,观察5min内的颜色变化 | 溶液变为红色 |
(2)完成表格:实验②中加入
上述两个实验中溶液都变为红色,因此无法得出实验结论。
进一步验证:为进一步验证猜想,小组同学配制系列溶液并测量其吸光度,绘制出右图曲线。
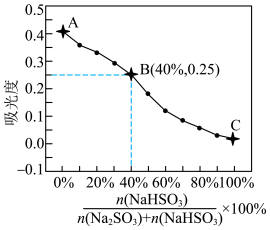
参比溶液:0.5mL1mol/LFeCl3溶液+0.5mL1mol/LNa2SO3溶液+7mL蒸馏水
图中A、B、C三点对应加入各试剂的体积如表所示。
| 点 | 1mol/LFeCl3/mL | 1mol/LNa2SO3/mL | 1mol/LNaHSO3/mL |
| A | 0.5 | 4.0 | 0.0 |
| B | a | b | |
| C | 0.0 | 4.0 |
(3)补充上表中数值,其中a=
实验结论
(4)根据以上实验,可以推测:溶液变为红色与
拓展探究
将静置9h后变为绿色的溶液分为两份,向其中一份溶液中滴加铁氰化钾溶液,有蓝色沉淀生成;向另一份溶液中滴加盐酸酸化的氯化钡溶液,有白色沉淀生成。
(5)①写出溶液变为绿色所发生氧化还原反应的离子方程式:
②试从平衡移动的角度,分析溶液红色变浅直至消失的原因:
(6)写出二氧化硫在生产生活中的一种应用:
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题:
(1)某种金属互化物具有自范性,原子在三维空间呈周期性有序排列,该金属互化物属于______ (填“晶体”或“非晶体”),可通过______ 方法鉴别。
(2) 基态核外电子排布式为
基态核外电子排布式为______
(3)苯胺(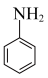 )与甲苯(
)与甲苯(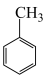 )的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是
)的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是______ 。
(4) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为______ 。
(5)某含铬化合物立方晶胞如图所示。与钙原子最近且等距离的氧原子有______ 个;钙和氧的最近距离为 ,NA为阿伏加德罗常数值,则该晶体密度为
,NA为阿伏加德罗常数值,则该晶体密度为______  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
(1)某种金属互化物具有自范性,原子在三维空间呈周期性有序排列,该金属互化物属于
(2)
 基态核外电子排布式为
基态核外电子排布式为(3)苯胺(
 )与甲苯(
)与甲苯( )的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是
)的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是(4)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为(5)某含铬化合物立方晶胞如图所示。与钙原子最近且等距离的氧原子有
 ,NA为阿伏加德罗常数值,则该晶体密度为
,NA为阿伏加德罗常数值,则该晶体密度为 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-04-29更新
|
80次组卷
|
2卷引用:广东省四会市四会中学、广信中学2023-2024学年高二下学期第二次月考化学试题
名校
8 . 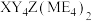 是一种分析试剂,所含的5种元素在前四周期均有分布,基态
是一种分析试剂,所含的5种元素在前四周期均有分布,基态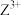 的d轨道半充满,基态M原子价层电子排布式为
的d轨道半充满,基态M原子价层电子排布式为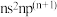 ,E和M位于同一主族,X原子比E原子少一个电子。下列说法正确的是
,E和M位于同一主族,X原子比E原子少一个电子。下列说法正确的是
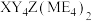 是一种分析试剂,所含的5种元素在前四周期均有分布,基态
是一种分析试剂,所含的5种元素在前四周期均有分布,基态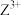 的d轨道半充满,基态M原子价层电子排布式为
的d轨道半充满,基态M原子价层电子排布式为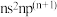 ,E和M位于同一主族,X原子比E原子少一个电子。下列说法正确的是
,E和M位于同一主族,X原子比E原子少一个电子。下列说法正确的是A.第一电离能: |
B.单质的沸点: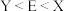 |
C.Z的单质能与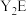 发生置换反应 发生置换反应 |
D.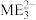 和 和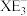 的VSEPR模型名称相同 的VSEPR模型名称相同 |
您最近一年使用:0次
2024-04-19更新
|
581次组卷
|
2卷引用:广东省四会市四会中学、广信中学2023-2024学年高二下学期第二次月考化学试题
真题
名校
9 . 下图所示化合物是制备某些药物的中间体,其中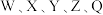 均为短周期元素,且原子序数依次增大,分子中的所有原子均满足稀有气体的稳定电子构型,Z原子的电子数是Q的一半。下列说法正确的是
均为短周期元素,且原子序数依次增大,分子中的所有原子均满足稀有气体的稳定电子构型,Z原子的电子数是Q的一半。下列说法正确的是
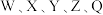 均为短周期元素,且原子序数依次增大,分子中的所有原子均满足稀有气体的稳定电子构型,Z原子的电子数是Q的一半。下列说法正确的是
均为短周期元素,且原子序数依次增大,分子中的所有原子均满足稀有气体的稳定电子构型,Z原子的电子数是Q的一半。下列说法正确的是
A.简单氢化物的稳定性: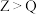 | B.第一电离能: |
C.基态原子的未成对电子数: | D.原子半径: |
您最近一年使用:0次
2024-04-07更新
|
2089次组卷
|
5卷引用:广东省肇庆市加美学校2023-2024学年高二下学期竞赛化学试题
广东省肇庆市加美学校2023-2024学年高二下学期竞赛化学试题2023年河北省高考化学试卷江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷 (已下线)通关练06 元素位-构-性推断-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)选择题6-10
10 . 近年来我国航天事业发展迅速,下列对所涉及化学知识的叙述错误的是
| A.“嫦娥五号”取回的月壤样品中含有天然玻璃物质,玻璃是晶体 |
| B.“天舟六号”壳体使用了铝合金,合金是金属材料 |
| C.“长征七号”采用了液氧煤油发动机,煤油是混合物 |
| D.“天宫”空间站新补充了一批氙推进剂,氙是稀有气体 |
您最近一年使用:0次
2024-04-07更新
|
1433次组卷
|
3卷引用:广东省肇庆市加美学校2023-2024学年高二下学期竞赛化学试题



