解题方法
1 . 化学与生产、生活密切相关,下列说法错误的是
| A.推广使用可降解塑料聚乳酸,能减少白色污染 |
| B.三星堆青铜大立人以合金为材料,其深埋于地下生锈是因为发生了析氢腐蚀 |
| C.液晶既有液体的流动性、形变性和黏度,又有类似晶体的各向异性 |
| D.汽车防冻液的主要成分为乙二醇,其沸点高的原因是易形成分子间氢键 |
您最近一年使用:0次
2024-09-18更新
|
89次组卷
|
2卷引用:甘肃省靖远县2024-2025学年高三上学期9月月考化学试题
2 . 一种回收锌电解阳极泥(主要成分为 、
、 和ZnO,还有少量锰铅复合氧化物
和ZnO,还有少量锰铅复合氧化物 和Ag)中铅和银的工艺流程如图。
和Ag)中铅和银的工艺流程如图。
(1)基态铅原子最高能级上电子云轮廓图为______ 形。
(2) 中Mn有+2价、+4价,Pb为+2价,将其写成氧化物的形式为
中Mn有+2价、+4价,Pb为+2价,将其写成氧化物的形式为____________ 。
(3)“还原”工序中主要发生反应的化学方程式为____________ 。
向“滤渣”中加入过量的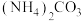 溶液可实现转化脱硫。
溶液可实现转化脱硫。
(4)结合离子方程式说明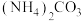 溶液显碱性的原因:
溶液显碱性的原因:____________ 。
(5)通过计算说明可用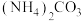 溶液将“滤渣”中的
溶液将“滤渣”中的 转化为
转化为 的原因:
的原因:____________ 。[已知:25℃时 ,
,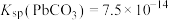 ]
]
(6)热电材料可实现热能和电能的直接相互转换,我国科学家以1%铬掺杂的硒化铅(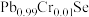 )作为研究对象,改写了室温热电优值记录。PbSe具有NaCl型的晶体结构,其晶体结构如图所示,晶胞中
)作为研究对象,改写了室温热电优值记录。PbSe具有NaCl型的晶体结构,其晶体结构如图所示,晶胞中 的配位数为
的配位数为______ ,若晶胞密度为 ,则两个
,则两个 之间的最短距离为
之间的最短距离为______ (列出计算式,设 为阿伏加德罗常数的值)nm。
为阿伏加德罗常数的值)nm。
 、
、 和ZnO,还有少量锰铅复合氧化物
和ZnO,还有少量锰铅复合氧化物 和Ag)中铅和银的工艺流程如图。
和Ag)中铅和银的工艺流程如图。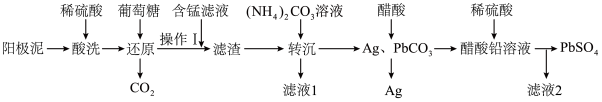
(1)基态铅原子最高能级上电子云轮廓图为
(2)
 中Mn有+2价、+4价,Pb为+2价,将其写成氧化物的形式为
中Mn有+2价、+4价,Pb为+2价,将其写成氧化物的形式为(3)“还原”工序中主要发生反应的化学方程式为
向“滤渣”中加入过量的
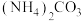 溶液可实现转化脱硫。
溶液可实现转化脱硫。(4)结合离子方程式说明
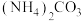 溶液显碱性的原因:
溶液显碱性的原因:(5)通过计算说明可用
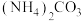 溶液将“滤渣”中的
溶液将“滤渣”中的 转化为
转化为 的原因:
的原因: ,
,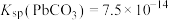 ]
](6)热电材料可实现热能和电能的直接相互转换,我国科学家以1%铬掺杂的硒化铅(
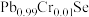 )作为研究对象,改写了室温热电优值记录。PbSe具有NaCl型的晶体结构,其晶体结构如图所示,晶胞中
)作为研究对象,改写了室温热电优值记录。PbSe具有NaCl型的晶体结构,其晶体结构如图所示,晶胞中 的配位数为
的配位数为 ,则两个
,则两个 之间的最短距离为
之间的最短距离为 为阿伏加德罗常数的值)nm。
为阿伏加德罗常数的值)nm。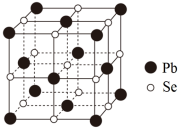
您最近一年使用:0次
解题方法
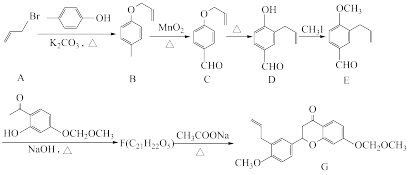
3 . 有机物G是合成某种药物的重要中间体,其合成路线如图:
(1)A的名称是______ 。
(2)C的含氧官能团的名称为______ 。
(3)F的结构简式为______ 。E→F实际上是经过两步反应,其反应类型分别是______ 、______ 。
(4)C→D为重排反应,C和D的沸点较高的是______ (填“C”或“D”),解释其原因:____________ 。检验C中含有D的试剂为______ 。
(5)有机物E有多种同分异构体,符合下列条件的E的同分异构体有______ 种(不考虑立体异构),其中核磁共振氢谱的峰面积比为1:1:2:2:2:4的是______ (填结构简式)。
①能发生银镜反应,且分子中无甲基
②仅含有一种官能团
③除苯环外,不含其他环状结构
(1)A的名称是
(2)C的含氧官能团的名称为
(3)F的结构简式为
(4)C→D为重排反应,C和D的沸点较高的是
(5)有机物E有多种同分异构体,符合下列条件的E的同分异构体有
①能发生银镜反应,且分子中无甲基
②仅含有一种官能团
③除苯环外,不含其他环状结构
您最近一年使用:0次
解题方法
4 . 乙醇是一种清洁的替代能源,催化加氢制备乙醇技术是当前的研究热点。
Ⅰ.某研究所成功研制出了单原子Bi修饰的Cu催化剂(BiCu-SAA),该催化剂能够在电催化还原 的过程中生成
的过程中生成 (多碳化合物)。
(多碳化合物)。
(1)反应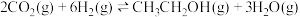 的活化能
的活化能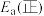
______ (填“大于”或“小于”)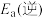 。该反应在
。该反应在______ (填“高温”“低温”或“任意温度”)条件下能自发进行。
(2)恒容绝热容器中发生反应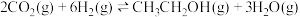 ,下列说法正确的是______。
,下列说法正确的是______。
(3)投入一定量的 和
和 发生反应,
发生反应, 的平衡转化率随温度和压强的变化如图。图中控制其他条件,只调节反应温度,反应速率最快的是
的平衡转化率随温度和压强的变化如图。图中控制其他条件,只调节反应温度,反应速率最快的是______ (填“ ”“
”“ ”或“
”或“ ”),理由是
”),理由是____________ 。
反应ⅰ: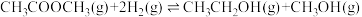
反应ⅱ: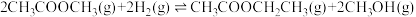
在温度为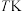 时,将
时,将 和
和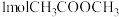 的混合气体通入体积为VL的恒容密闭容器中,反应经tmin后达到平衡,测得平衡时
的混合气体通入体积为VL的恒容密闭容器中,反应经tmin后达到平衡,测得平衡时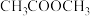 的转化率为80%,
的转化率为80%, 的选择性(
的选择性(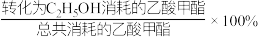 )为60%。
)为60%。
(4)0~tmin内,
______ (用含V、t的式子表示) 。
。
(5)该温度下,反应Ⅰ的平衡常数K=______ 。
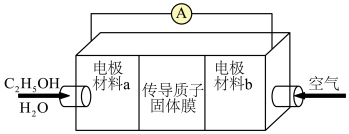
Ⅲ.乙醇燃料电池(电极材料a和b均为性电极)广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示:____________ 。当转移0.6mol电子时,正极需要通入的空气的体积约为______ L(标准状况下)。
Ⅰ.某研究所成功研制出了单原子Bi修饰的Cu催化剂(BiCu-SAA),该催化剂能够在电催化还原
 的过程中生成
的过程中生成 (多碳化合物)。
(多碳化合物)。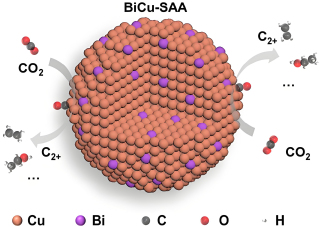
| 化学键 |  |  |  |  |  |  |
键能/( ) ) | 414 | 351 | 465 | 436 | 803 | 332 |
(1)反应
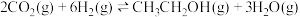 的活化能
的活化能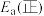
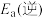 。该反应在
。该反应在(2)恒容绝热容器中发生反应
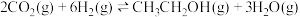 ,下列说法正确的是______。
,下列说法正确的是______。A.加入合适的催化剂可以提高 的平衡转化率 的平衡转化率 |
| B.反应达到平衡后容器内温度保持不变 |
C.反应达到平衡时 一定成立 一定成立 |
| D.容器内气体密度不变时说明达到了平衡状态 |
(3)投入一定量的
 和
和 发生反应,
发生反应, 的平衡转化率随温度和压强的变化如图。图中控制其他条件,只调节反应温度,反应速率最快的是
的平衡转化率随温度和压强的变化如图。图中控制其他条件,只调节反应温度,反应速率最快的是 ”“
”“ ”或“
”或“ ”),理由是
”),理由是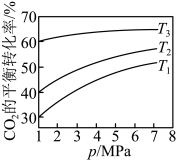
反应ⅰ:
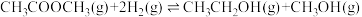
反应ⅱ:
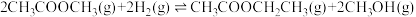
在温度为
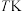 时,将
时,将 和
和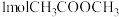 的混合气体通入体积为VL的恒容密闭容器中,反应经tmin后达到平衡,测得平衡时
的混合气体通入体积为VL的恒容密闭容器中,反应经tmin后达到平衡,测得平衡时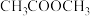 的转化率为80%,
的转化率为80%, 的选择性(
的选择性(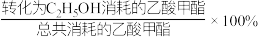 )为60%。
)为60%。(4)0~tmin内,

 。
。(5)该温度下,反应Ⅰ的平衡常数K=
Ⅲ.乙醇燃料电池(电极材料a和b均为性电极)广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示:
您最近一年使用:0次
解题方法
5 . 硫代硫酸钠晶体( )具有较强的还原性和配位能力,可用作造纸业的脱氯剂、定量分析中的还原剂。实验室可用如图所示装置制备。
)具有较强的还原性和配位能力,可用作造纸业的脱氯剂、定量分析中的还原剂。实验室可用如图所示装置制备。
Ⅱ.往烧瓶中滴加70%浓硫酸,打开开关 ,可观察到锥形瓶中有大量的浅黄色的硫逐渐析出,继续通入二氧化硫,反应进行30~40min时溶液的pH接近7,关闭
,可观察到锥形瓶中有大量的浅黄色的硫逐渐析出,继续通入二氧化硫,反应进行30~40min时溶液的pH接近7,关闭 ,打开
,打开 ,同时停止通如二氧化硫。
,同时停止通如二氧化硫。
Ⅲ.过滤,将所得硫代硫酸钠溶液转移到蒸发皿中加热,浓缩到刚有晶体析出时停止加热,冷却析出晶体,抽滤得到 晶体。
晶体。
已知:硫代硫酸钠易溶于水,难溶于乙醇,在酸性条件下极不稳定,易分解。
请回答下列问题:
(1)实验中使用的硫酸是70%的浓硫酸而不是98.3%的浓硫酸,其原因是______ 。
(2)写出实验过程中产生浅黄色的硫单质的离子方程式:____________ 。
(3)为了保证硫代硫酸钠的产量,实验中通入的 不能过量。若
不能过量。若 过量使溶液
过量使溶液 ,产率会降低,理论上
,产率会降低,理论上 和
和 的最佳物质的量之比应为
的最佳物质的量之比应为______ 。
(4)溴化银(AgBr)可用硫代硫酸钠( )溶解。写出
)溶解。写出 溶液溶解AgBr生成
溶液溶解AgBr生成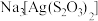 的离子方程式:
的离子方程式:__________ 。在配合物离子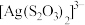 中,
中,______ (填标号)不可能作配位原子。
a. 中的中心S原子 b.
中的中心S原子 b. 中的端基S原子
中的端基S原子
测定产品的含量。
①溶液配制:
(5)称取1.2000g硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在______ 中溶解,完全溶解冷却至室温后,全部转移至100mL的______ 中,加蒸馏水至溶液的凹液面最低处与刻度线相切。
②滴定:取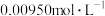 的
的 标准溶液20.00ml,硫酸酸化后加入过量KI,发生反应:
标准溶液20.00ml,硫酸酸化后加入过量KI,发生反应: 。然后用硫代硫酸钠样品溶液滴定,发生反应:
。然后用硫代硫酸钠样品溶液滴定,发生反应: 。
。
(6)加入淀粉溶液作为指示剂,继续滴定,当______ ,即为滴定终点。平行滴定3次,样品溶液的平均用量为24.80mL,则样品纯度为______ %。
 )具有较强的还原性和配位能力,可用作造纸业的脱氯剂、定量分析中的还原剂。实验室可用如图所示装置制备。
)具有较强的还原性和配位能力,可用作造纸业的脱氯剂、定量分析中的还原剂。实验室可用如图所示装置制备。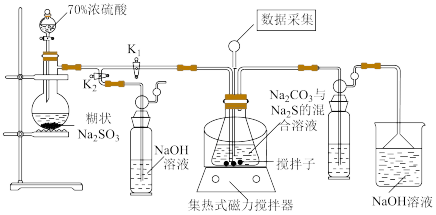
Ⅱ.往烧瓶中滴加70%浓硫酸,打开开关
 ,可观察到锥形瓶中有大量的浅黄色的硫逐渐析出,继续通入二氧化硫,反应进行30~40min时溶液的pH接近7,关闭
,可观察到锥形瓶中有大量的浅黄色的硫逐渐析出,继续通入二氧化硫,反应进行30~40min时溶液的pH接近7,关闭 ,打开
,打开 ,同时停止通如二氧化硫。
,同时停止通如二氧化硫。Ⅲ.过滤,将所得硫代硫酸钠溶液转移到蒸发皿中加热,浓缩到刚有晶体析出时停止加热,冷却析出晶体,抽滤得到
 晶体。
晶体。已知:硫代硫酸钠易溶于水,难溶于乙醇,在酸性条件下极不稳定,易分解。
请回答下列问题:
(1)实验中使用的硫酸是70%的浓硫酸而不是98.3%的浓硫酸,其原因是
(2)写出实验过程中产生浅黄色的硫单质的离子方程式:
(3)为了保证硫代硫酸钠的产量,实验中通入的
 不能过量。若
不能过量。若 过量使溶液
过量使溶液 ,产率会降低,理论上
,产率会降低,理论上 和
和 的最佳物质的量之比应为
的最佳物质的量之比应为(4)溴化银(AgBr)可用硫代硫酸钠(
 )溶解。写出
)溶解。写出 溶液溶解AgBr生成
溶液溶解AgBr生成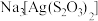 的离子方程式:
的离子方程式: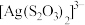 中,
中,a.
 中的中心S原子 b.
中的中心S原子 b. 中的端基S原子
中的端基S原子测定产品的含量。
①溶液配制:
(5)称取1.2000g硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在
②滴定:取
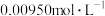 的
的 标准溶液20.00ml,硫酸酸化后加入过量KI,发生反应:
标准溶液20.00ml,硫酸酸化后加入过量KI,发生反应: 。然后用硫代硫酸钠样品溶液滴定,发生反应:
。然后用硫代硫酸钠样品溶液滴定,发生反应: 。
。(6)加入淀粉溶液作为指示剂,继续滴定,当
您最近一年使用:0次
解题方法
6 . 硫酸盐(含 、
、 )气溶胶是雾霾的成分之一。科学家发现,处于纳米液滴中的
)气溶胶是雾霾的成分之一。科学家发现,处于纳米液滴中的 通过“水分子桥”,可以将电子快速转移给周围的气相
通过“水分子桥”,可以将电子快速转移给周围的气相 分子,雾霾中硫酸盐生成的主要过程示意图如图所示。下列说法正确的是
分子,雾霾中硫酸盐生成的主要过程示意图如图所示。下列说法正确的是
 、
、 )气溶胶是雾霾的成分之一。科学家发现,处于纳米液滴中的
)气溶胶是雾霾的成分之一。科学家发现,处于纳米液滴中的 通过“水分子桥”,可以将电子快速转移给周围的气相
通过“水分子桥”,可以将电子快速转移给周围的气相 分子,雾霾中硫酸盐生成的主要过程示意图如图所示。下列说法正确的是
分子,雾霾中硫酸盐生成的主要过程示意图如图所示。下列说法正确的是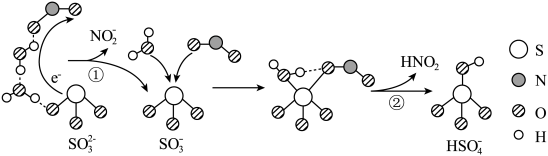
A. 、 、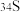 、 、 、 、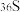 原子的中子数均相同 原子的中子数均相同 |
B.键角: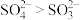 |
C. 和 和 的中心原子轨道杂化类型均为 的中心原子轨道杂化类型均为 |
D.液态水中的作用力由强到弱的顺序是氢键 范德华力 范德华力 |
您最近一年使用:0次
解题方法
7 . 下列化学用语错误的是
A.基态 的价电子轨道表示式: 的价电子轨道表示式: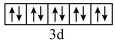 |
B.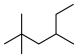 的名称:3,5,5-三甲基己烷 的名称:3,5,5-三甲基己烷 |
C. 的形成过程: 的形成过程: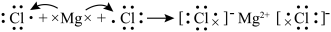 |
D. 的空间结构模型为 的空间结构模型为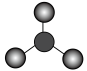 |
您最近一年使用:0次
8 . 建设人与自然和谐共生的美丽中国,人人有责。下列做法错误的是
| A.将用完的废旧电池深埋地下 | B.厨房垃圾分类收集处理后用于发电 |
| C.周末骑着共享单车去郊外游玩 | D.将燃煤与生石灰混合后再燃烧 |
您最近一年使用:0次
解题方法
9 . 科学家开发催化剂实现 催化还原制备附加值高的产品。利用
催化还原制备附加值高的产品。利用 制备甲醇的有关反应如下:
制备甲醇的有关反应如下:
I.

II.

(1)已知几种共价键的键能如下:
利用键能数据计算:
___________  。
。
(2)一定温度下,在恒容密闭容器中充入等体积的 、
、 ,仅发生反应Ⅰ,下列叙述正确的是
,仅发生反应Ⅰ,下列叙述正确的是___________ (填标号)。
A.平衡后充入氩气,正反应速率增大
B. 的体积分数不变时达到平衡状态
的体积分数不变时达到平衡状态
C.平衡后充入少量 ,
, 平衡转化率增大
平衡转化率增大
(3)在一恒容反应器中充入一定量的 、
、 ,仅发生反应Ⅱ,平衡常数(K)与温度(T)的关系如下:
,仅发生反应Ⅱ,平衡常数(K)与温度(T)的关系如下:
①
___________ (填“>”“<”或“=”)0。
②1200℃时,某时刻反应体系中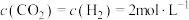 ,
,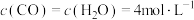 ,此时平衡
,此时平衡___________ (填“向正反应方向”“向逆反应方向”或“不”)移动。
(4)一定条件下,速率常数与活化能、温度的关系式为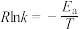 (R为常数,k为速率常数,
(R为常数,k为速率常数, 为活化能,T为温度)。一定温度下,合成甲醇的速率常数在不同催化剂(Cat1、Cat2)作用下,与温度的关系如图所示:
为活化能,T为温度)。一定温度下,合成甲醇的速率常数在不同催化剂(Cat1、Cat2)作用下,与温度的关系如图所示: 为
为___________  ;催化效果更好的是
;催化效果更好的是___________ (填“Catl”或“Cat2”)。
(5)在一定温度下,向甲、乙两密闭反应器中分别充入 和
和 ,分别在有水分子隔离膜、无水分子隔离膜作用下发生上述两个反应,测得
,分别在有水分子隔离膜、无水分子隔离膜作用下发生上述两个反应,测得 平衡转化率与压强的关系如图所示:
平衡转化率与压强的关系如图所示:___________ (填“甲”或“乙”),理由是___________ 。
②已知M点 选择性为80%,该温度下,M点反应II的平衡常数
选择性为80%,该温度下,M点反应II的平衡常数 为
为___________ (结果保留三位有效数字)。提示:分压=总压×物质的量分数, 选择性等于
选择性等于 的物质的量与
的物质的量与 转化的总物质的量之比。
转化的总物质的量之比。
 催化还原制备附加值高的产品。利用
催化还原制备附加值高的产品。利用 制备甲醇的有关反应如下:
制备甲醇的有关反应如下:I.


II.


(1)已知几种共价键的键能如下:
| 共价键 | C=O | H—H | H—C | C—O | H—O |
键能/ | 799 | 436 | 413 | 358 | 467 |

 。
。(2)一定温度下,在恒容密闭容器中充入等体积的
 、
、 ,仅发生反应Ⅰ,下列叙述正确的是
,仅发生反应Ⅰ,下列叙述正确的是A.平衡后充入氩气,正反应速率增大
B.
 的体积分数不变时达到平衡状态
的体积分数不变时达到平衡状态C.平衡后充入少量
 ,
, 平衡转化率增大
平衡转化率增大(3)在一恒容反应器中充入一定量的
 、
、 ,仅发生反应Ⅱ,平衡常数(K)与温度(T)的关系如下:
,仅发生反应Ⅱ,平衡常数(K)与温度(T)的关系如下:| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |

②1200℃时,某时刻反应体系中
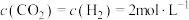 ,
,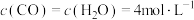 ,此时平衡
,此时平衡(4)一定条件下,速率常数与活化能、温度的关系式为
 (R为常数,k为速率常数,
(R为常数,k为速率常数, 为活化能,T为温度)。一定温度下,合成甲醇的速率常数在不同催化剂(Cat1、Cat2)作用下,与温度的关系如图所示:
为活化能,T为温度)。一定温度下,合成甲醇的速率常数在不同催化剂(Cat1、Cat2)作用下,与温度的关系如图所示: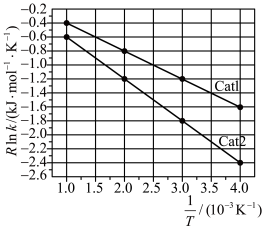
 为
为 ;催化效果更好的是
;催化效果更好的是(5)在一定温度下,向甲、乙两密闭反应器中分别充入
 和
和 ,分别在有水分子隔离膜、无水分子隔离膜作用下发生上述两个反应,测得
,分别在有水分子隔离膜、无水分子隔离膜作用下发生上述两个反应,测得 平衡转化率与压强的关系如图所示:
平衡转化率与压强的关系如图所示: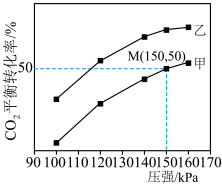
②已知M点
 选择性为80%,该温度下,M点反应II的平衡常数
选择性为80%,该温度下,M点反应II的平衡常数 为
为 选择性等于
选择性等于 的物质的量与
的物质的量与 转化的总物质的量之比。
转化的总物质的量之比。
您最近一年使用:0次
2024-08-23更新
|
99次组卷
|
2卷引用:甘肃省靖远县2023-2024学年高三上学期12月月考化学试题
10 . 氢硼烷(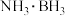 )电池可在常温下工作,装置如图所示。该电池工作时的总反应为
)电池可在常温下工作,装置如图所示。该电池工作时的总反应为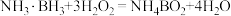 。下列说法正确的是
。下列说法正确的是
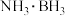 )电池可在常温下工作,装置如图所示。该电池工作时的总反应为
)电池可在常温下工作,装置如图所示。该电池工作时的总反应为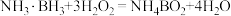 。下列说法正确的是
。下列说法正确的是 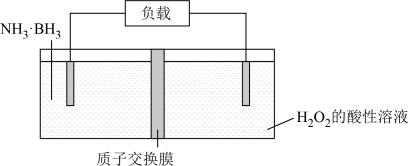
A.正极附近溶液的 减小 减小 |
| B.左侧电极发生氧化反应 |
C.消耗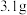 氨硼烷,理论上通过内电路的电子为 氨硼烷,理论上通过内电路的电子为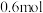 |
D.电池工作时, 通过质子交换膜向左侧电极移动 通过质子交换膜向左侧电极移动 |
您最近一年使用:0次
2024-08-19更新
|
88次组卷
|
2卷引用:甘肃省靖远县第二中学2023-2024学年高二下学期7月期末考试模拟化学试题



