21-22高一·全国·课后作业
名校
1 . 如图为实验室某浓盐酸试剂瓶标签上的部分数据,试根据标签.上的相关数据回答下列问题:.
(1)该浓盐酸中HCl的物质的量浓度为______ mol/L。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______(填字母)。
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.400mol/L的稀盐酸。
①该学生需要量取______ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面:______ ;
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水:______ 。
(4)①假设该同学成功配制了0.400mol/L的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取______ mL盐酸。
②假设该同学用新配制的盐酸中和含0.4g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是______ 。
A.浓盐酸挥发,浓度不足 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:  HCl的质量分数:36.5% |
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______(填字母)。
| A.溶液中HCl的物质的量 | B.溶液的浓度 |
C.溶液中 的数目 的数目 | D.溶液的密度 |
①该学生需要量取
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面:
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水:
(4)①假设该同学成功配制了0.400mol/L的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取
②假设该同学用新配制的盐酸中和含0.4g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是
A.浓盐酸挥发,浓度不足 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
您最近一年使用:0次
2024-02-22更新
|
76次组卷
|
6卷引用:第一章 单元检测-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)
(已下线)第一章 单元检测-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)河北省隆化存瑞中学2022-2023学年高一上学期第一次月考化学试题山东省威海市文登新一中2021-2022学年高一上学期12月月考化学试题河南省濮阳市第一高级中学2022-2023学年高一上学期期中质量检测化学试题黑龙江省齐齐哈尔市普高联谊校2022-2023学年高三上学期期中考试化学试题河南省周口市鹿邑县2023-2024学年高一上学期1月期末化学试题
2 . 已知 ;以丙烯为原料合成2-甲基-1-丙醇的过程如下,丙烯
;以丙烯为原料合成2-甲基-1-丙醇的过程如下,丙烯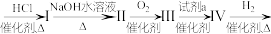 2-甲基-1-丙醇。下列说法错误的是
2-甲基-1-丙醇。下列说法错误的是
| A.丙烯→I的反应可生成两种产物 | B.II的结构简式为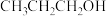 |
| C.试剂a可用作食品添加剂 | D.IV能使溴水褪色 |
您最近一年使用:0次
2023-04-23更新
|
478次组卷
|
7卷引用:烃的衍生物—进阶学习
22-23高二下·全国·课时练习
3 . 航天员的航天服采用了很多新型超高性能复合材料。其中聚酰胺纤维M就是一种新型超高性能纤维,它的防热和防火性能十分出色。聚酰胺纤维M的结构简式为
 。
。
下面是聚酰胺纤维M的一种合成路线(部分反应未注明条件):
A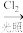 B→C
B→C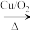 D
D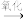

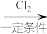 E
E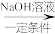 F
F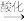 M
M
(1)写出下列反应的反应类型A→B:_______ ;G+H→M:_______ 。
(2)生成B的同时还可能生成B的一种同分异构体,其结构简式为_______ 。
(3)写出E→F的化学方程式:_______ 。
(4)聚酯纤维P是一种无毒的玩具内充物,其结构简式为 。聚酯纤维P可用A和乙烯为原料合成,请你设计并写出其合成路线
。聚酯纤维P可用A和乙烯为原料合成,请你设计并写出其合成路线_______ 。
提示:①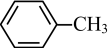

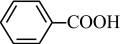 ;
;
②合成过程中无机试剂任选。
 。
。下面是聚酰胺纤维M的一种合成路线(部分反应未注明条件):
A
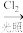 B→C
B→C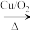 D
D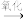

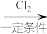 E
E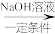 F
F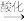 M
M(1)写出下列反应的反应类型A→B:
(2)生成B的同时还可能生成B的一种同分异构体,其结构简式为
(3)写出E→F的化学方程式:
(4)聚酯纤维P是一种无毒的玩具内充物,其结构简式为
 。聚酯纤维P可用A和乙烯为原料合成,请你设计并写出其合成路线
。聚酯纤维P可用A和乙烯为原料合成,请你设计并写出其合成路线提示:①


 ;
;②合成过程中无机试剂任选。
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
4 . 探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.

Ⅱ.

Ⅲ.

回答下列问题:
(1)
_______  。
。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为ɑ mol,CO为b mol,此时H2O(g)的浓度为_______ mol﹒L-1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为_______ 。
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2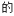 平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
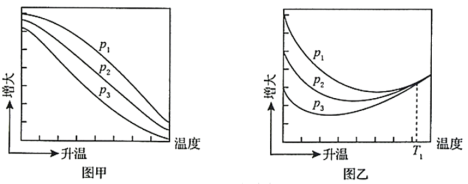
已知:CO2的平衡转化率=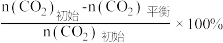
CH3OH的平衡产率=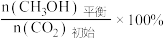
其中纵坐标表示CO2平衡转化率的是图_______ (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为_______ ;图乙中T1温度时,三条曲线几乎交于一点的原因是_______ 。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_______(填标号)。
Ⅰ.


Ⅱ.


Ⅲ.


回答下列问题:
(1)

 。
。(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为ɑ mol,CO为b mol,此时H2O(g)的浓度为
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2
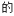 平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
已知:CO2的平衡转化率=
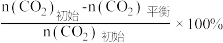
CH3OH的平衡产率=
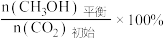
其中纵坐标表示CO2平衡转化率的是图
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_______(填标号)。
| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
您最近一年使用:0次
2023-01-31更新
|
549次组卷
|
4卷引用:化学反应速率与化学平衡——课时5影响化学平衡的因素
(已下线)化学反应速率与化学平衡——课时5影响化学平衡的因素(已下线)专题09 化学反应速率与化学平衡(测)-2023年高考化学二轮复习讲练测(新高考专用)广东北江实验学校2023—2024学年高二上学期10月月考化学试题山东省日照神州天立高级中学高复部2023-2024学年高三上学期12月份阶段性测试化学试题
5 . 三种气体 X、Y、Z 的相对分子质量关系为 Mr(X)<Mr(Y)=0.5Mr(Z),下列说法正确的是
| A.原子数相等的三种气体,质量最大是 Z |
| B.若一定条件下,三种气体体积均为2.24L,则它们的物质的量一定均为0.1 mol |
| C.同温同压下,同质量的三种气体,气体密度最小的是X |
| D.同温下,体积相同的两容器分别充agY气体和2agZ气体,则压强之比为1:2 |
您最近一年使用:0次
2022-12-25更新
|
1623次组卷
|
52卷引用:专题1 第2课时气体摩尔体积-高中化学苏教2019版必修第一册
专题1 第2课时气体摩尔体积-高中化学苏教2019版必修第一册2016届湖北省武汉市高三下学期2月调研理综化学试卷2016-2017学年江西省南昌二中高一上月考一化学试卷2017届辽宁省沈阳东北育才学校高三上期中模拟化学卷2016届辽宁省葫芦岛市第一高级中学高三上学期第二次周考理综化学试卷河北省“名校联盟”(五校联考)2018届高三上学期教学质量监测(一)化学试题湖北省武汉市部分重点中学2017-2018学年高一上学期期中考试化学试题山东省沂水县第一中学2018届高三下学期第2次模拟化学试题【全国百强校】河北省邢台市第一中学2017-2018学年高二下学期第三次月考化学试题(已下线)【备战2019年浙江新高考-考点】——考点02 物质的量【市级联考】山东省泰安市2019届高三上学期期中考试化学试题【校级联考】安徽省滁州市定远县西片区2018-2019学年高一上学期期中考试化学试题云南省新平县一中2018-2019学年高一上学期12月月考化学试题云南省元江县一中2018-2019学年高一下学期2月份考试化学试题(已下线)2019年7月2日 《每日一题》2020年高考一轮复习-阿伏加德罗定律及其推论的应用河北省秦皇岛一中2019-2020学年高一上学期第一次月考化学试题四川省广安市邻水县邻水实验学校2019-2020学年高一上学期第一次月考化学试题河北省邯郸市2019-2020学年高一上学期期中考试化学试题内蒙古第一机械制造(集团)有限公司第一中学2019-2020学年高一10月月考化学试题广西南宁市第三中学2019-2020学年高一上学期期中考试化学试题安徽省合肥十中2019-2020学年高一上学期期中考试化学试题云南省云县第一中学2019-2020学年高二12月月考化学试题1内蒙古包钢第一中学2019-2020学年高一上学期10月月考化学试题广东省江门市第一中学2019-2020学年高一上学期10月月考化学试题山西省忻州市第一中学2019-2020学年高一上学期第二次月考化学试题安徽省合肥市肥东县第二中学2020-2021学年高一上学期期末考试化学试题内蒙古呼和浩特市第十六中学2020-2021学年高一上学期第一次质量检测化学试题(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)课时11 物质的量、气体摩尔体积-2022年高考化学一轮复习小题多维练(全国通用)福建省厦门一中2019-2020学年高一上学期第一次月考(10月)化学试题(已下线)考点02 化学用语和常用化学计量-备战2022年高考化学学霸纠错(全国通用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)提升卷02-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)化学-2022年高考押题预测卷02(山东卷)(已下线)必刷卷04-2022年高考化学考前信息必刷卷(山东专用)(已下线)考点02 物质的量 气体摩尔体积-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第04讲 物质的量 气体摩尔体积 (练)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省龙西北八校联合体2022-2023学年高三上学期开学考试化学试题河南省南阳市第一中学校2023届高三上学期第二次阶段考试化学试题重庆市万州纯阳中学2022-2023学年高三上学期8月月考化学试题(已下线)专题五 化学常用计量与化学计算-实战高考·二轮复习核心突破山东莒县第一中学2022-2023学年高一上学期12月月考化学试题山东省烟台第一中学2022-2023学年高一上学期月考化学试题山东省烟台第一中学2022-2023学年高一上学期期末调研化学试题安徽省安庆市桐城中学2022-2023学年高一上学期第二次教学质量检测化学试题第二章 物质的量化学实验基本技能 第6讲 物质的量山东省枣庄市第八中学南校2022-2023学年高一1月线上测试化学试题河北省石家庄二中教育集团2022-2023学年度高一年级上学期期末考试化学试题广西浦北中学2023-2024学年高一上学期10月月考化学试题福建省泉州市安溪一中、养正中学、惠安一中、实验中学2023-2024学年高一上学期期中考化学试题
名校
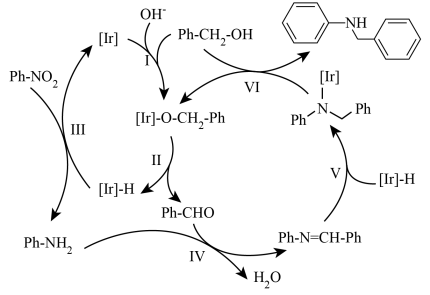
6 . 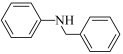 可利用酰胺型铱金属配合物通过硝基芳烃还原串联N-苄基化反应制备。反应机理如图(其中Ph-代表苯基,[Ir]代表
可利用酰胺型铱金属配合物通过硝基芳烃还原串联N-苄基化反应制备。反应机理如图(其中Ph-代表苯基,[Ir]代表 )下列说法
)下列说法不正确 的是
 可利用酰胺型铱金属配合物通过硝基芳烃还原串联N-苄基化反应制备。反应机理如图(其中Ph-代表苯基,[Ir]代表
可利用酰胺型铱金属配合物通过硝基芳烃还原串联N-苄基化反应制备。反应机理如图(其中Ph-代表苯基,[Ir]代表 )下列说法
)下列说法
| A.反应I过程中有水生成 |
| B.反应IV涉及加成反应和消去反应 |
| C.该过程反应原料为硝基苯和苯甲醇 |
D.用CH3CH2CH2OH替代上述过程中的同类物质参与反应,可以合成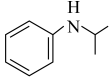 |
您最近一年使用:0次
2022-11-12更新
|
1758次组卷
|
9卷引用:【知识图鉴】单元讲练测选择性必修3第3单元03巩固练
(已下线)【知识图鉴】单元讲练测选择性必修3第3单元03巩固练浙江省宁波市2022-2023学年高三上学期选考模拟考试化学试题(已下线)热点情景汇编-专题五 简单有机物中的化学(已下线)化学(浙江B卷)-学易金卷:2023年高考第一次模拟考试卷河北省邯郸市第一中学2022-2023学年高三上学期一轮复习(四)化学试题(已下线)专题12 化学反应机理(测)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题13 反应微观机理分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)仿真卷04-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)江西省赣州市兴国平川中学2022-2023学年高二下学期4月期中考试化学试题
22-23高二上·全国·课时练习
名校
解题方法
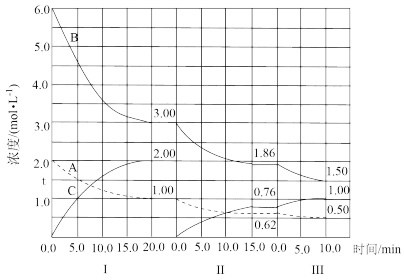
7 . 反应aA(g)+bB(g) cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:
问题:
(1)反应的化学方程式中a∶b∶c为____ 。
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小排列次序为____ 。
(3)B的平衡转化率αI(B)、αII(B)、αIII(B)中最小的是____ ,其值是____ 。
(4)由第一次平衡到第二次平衡,平衡向____ 移动,采取的措施是____ 。
(5)比较第II阶段反应温度(T2)和第III阶段反应温度(T3)的高低;T2____ T3(填“<”“>”“=”),判断的理由是____ 。
 cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:
问题:
(1)反应的化学方程式中a∶b∶c为
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小排列次序为
(3)B的平衡转化率αI(B)、αII(B)、αIII(B)中最小的是
(4)由第一次平衡到第二次平衡,平衡向
(5)比较第II阶段反应温度(T2)和第III阶段反应温度(T3)的高低;T2
您最近一年使用:0次
2022-10-18更新
|
1095次组卷
|
4卷引用:2.2.3 化学反应速率和化学平衡图像——同步学习必备知识
(已下线)2.2.3 化学反应速率和化学平衡图像——同步学习必备知识内蒙古包钢第一中学2022-2023学年高二上学期月考化学试题江西省赣州市十校协作2022-2023学年高二上学期期中联考化学试题河南省郑州中学2023-2024学年高三上学期第二次月考化学试题
22-23高二上·全国·课时练习
解题方法
8 . 在密闭容器中,对于反应N2(g)+3H2(g) 2NH3,N2和H2起始的量分别为2mol和6mol,达到平衡时H2的转化率30%。若从氨气开始进行化学反应,在相同条件下欲使平衡时各成分的含量与前者相同,则起始时NH3物质的量和NH3的转化率分别是
2NH3,N2和H2起始的量分别为2mol和6mol,达到平衡时H2的转化率30%。若从氨气开始进行化学反应,在相同条件下欲使平衡时各成分的含量与前者相同,则起始时NH3物质的量和NH3的转化率分别是
 2NH3,N2和H2起始的量分别为2mol和6mol,达到平衡时H2的转化率30%。若从氨气开始进行化学反应,在相同条件下欲使平衡时各成分的含量与前者相同,则起始时NH3物质的量和NH3的转化率分别是
2NH3,N2和H2起始的量分别为2mol和6mol,达到平衡时H2的转化率30%。若从氨气开始进行化学反应,在相同条件下欲使平衡时各成分的含量与前者相同,则起始时NH3物质的量和NH3的转化率分别是| A.3mol和70% | B.2mol和80% | C.2mol和70% | D.4mol和80% |
您最近一年使用:0次
名校
解题方法
9 . 下列说法不正确的是
| A.鸡蛋白溶液中,加入醋酸铅溶液有沉淀析出,加入水后沉淀不溶解 |
| B.用银氨溶液可以鉴别葡萄糖和乙酸溶液 |
| C.可用饱和碳酸钠溶液鉴别乙酸、乙醇、苯及氢氧化钡溶液 |
| D.取少量淀粉溶液,加入一定量稀硫酸,水浴加热几分钟后,再加入新制的氢氧化铜并加热,观察现象,判断淀粉水解的产物中是否含有葡萄糖 |
您最近一年使用:0次
2022-10-13更新
|
1354次组卷
|
5卷引用:第2课时 蛋白质、油脂
名校
解题方法
10 . 利用 合成二甲醚可以很大程度地帮助实现“碳中和”,其合成过程由两种工艺组成。
合成二甲醚可以很大程度地帮助实现“碳中和”,其合成过程由两种工艺组成。
工艺1:先在设备一加氢合成甲醇,主要涉及以下反应:
Ⅰ、甲醇的合成: ;
;
Ⅱ、逆水汽变换: ;
;
再通过设备二合成二甲醚,涉及以下反应:
Ⅲ、甲醇脱水: 。
。
工艺2:在双功能催化剂作用下,由 加氢直接得到二甲醚。
加氢直接得到二甲醚。
已知:相关物质变化的焓变示意图如下:

回答下列问题:
(1)请写出工艺2中 直接加氢合成
直接加氢合成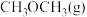 (反应Ⅳ)的热化学方程式:
(反应Ⅳ)的热化学方程式:___________ 。
(2)①工艺1需先在设备一合成甲醇。在不同压强下,按照 投料合成甲醇,实验测定
投料合成甲醇,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如图所示。
的平衡产率随温度的变化关系如图所示。


下列说法正确的是___________ (填字母)。
A.图甲纵坐标表示 的平衡产率
的平衡产率
B.压强: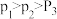
C.为了同时提高 的平衡转化率和
的平衡转化率和 的平衡产率,应选择低温、高压的反应条件
的平衡产率,应选择低温、高压的反应条件
D.一定温度、压强下,寻找活性更高的催化剂,是提高 的平衡转化率的主要研究方向
的平衡转化率的主要研究方向
②解释图乙不同压强下纵坐标代表的物理量在550℃后趋于相等的原因:___________ 。
(3)若一定量 和
和 仅发生反应Ⅰ和Ⅱ,研究表明:在其他条件相同的情况下,用新型催化剂可以显著提高甲醇的选择性。使用该催化剂,按
仅发生反应Ⅰ和Ⅱ,研究表明:在其他条件相同的情况下,用新型催化剂可以显著提高甲醇的选择性。使用该催化剂,按 (总量为a
(总量为a )投料于恒容密闭容器中进行反应,
)投料于恒容密闭容器中进行反应, 的平衡转化率和甲醇的选择性(甲醇的选择性:转化的
的平衡转化率和甲醇的选择性(甲醇的选择性:转化的 中生成甲醇的物质的量分数)随温度的变化趋势如图所示(忽略温度对催化剂的影响)。
中生成甲醇的物质的量分数)随温度的变化趋势如图所示(忽略温度对催化剂的影响)。

①根据图中数据,温度选择___________ K(填“473”“513”或“553”),达到平衡时,反应体系内甲醇的产量最高。
②随着温度的升高, 的平衡转化率增加但甲醇的选择性降低,请分析其原因:
的平衡转化率增加但甲醇的选择性降低,请分析其原因:___________ 。
 合成二甲醚可以很大程度地帮助实现“碳中和”,其合成过程由两种工艺组成。
合成二甲醚可以很大程度地帮助实现“碳中和”,其合成过程由两种工艺组成。工艺1:先在设备一加氢合成甲醇,主要涉及以下反应:
Ⅰ、甲醇的合成:
 ;
;Ⅱ、逆水汽变换:
 ;
;再通过设备二合成二甲醚,涉及以下反应:
Ⅲ、甲醇脱水:
 。
。工艺2:在双功能催化剂作用下,由
 加氢直接得到二甲醚。
加氢直接得到二甲醚。已知:相关物质变化的焓变示意图如下:

回答下列问题:
(1)请写出工艺2中
 直接加氢合成
直接加氢合成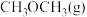 (反应Ⅳ)的热化学方程式:
(反应Ⅳ)的热化学方程式:(2)①工艺1需先在设备一合成甲醇。在不同压强下,按照
 投料合成甲醇,实验测定
投料合成甲醇,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如图所示。
的平衡产率随温度的变化关系如图所示。

下列说法正确的是
A.图甲纵坐标表示
 的平衡产率
的平衡产率B.压强:
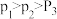
C.为了同时提高
 的平衡转化率和
的平衡转化率和 的平衡产率,应选择低温、高压的反应条件
的平衡产率,应选择低温、高压的反应条件D.一定温度、压强下,寻找活性更高的催化剂,是提高
 的平衡转化率的主要研究方向
的平衡转化率的主要研究方向②解释图乙不同压强下纵坐标代表的物理量在550℃后趋于相等的原因:
(3)若一定量
 和
和 仅发生反应Ⅰ和Ⅱ,研究表明:在其他条件相同的情况下,用新型催化剂可以显著提高甲醇的选择性。使用该催化剂,按
仅发生反应Ⅰ和Ⅱ,研究表明:在其他条件相同的情况下,用新型催化剂可以显著提高甲醇的选择性。使用该催化剂,按 (总量为a
(总量为a )投料于恒容密闭容器中进行反应,
)投料于恒容密闭容器中进行反应, 的平衡转化率和甲醇的选择性(甲醇的选择性:转化的
的平衡转化率和甲醇的选择性(甲醇的选择性:转化的 中生成甲醇的物质的量分数)随温度的变化趋势如图所示(忽略温度对催化剂的影响)。
中生成甲醇的物质的量分数)随温度的变化趋势如图所示(忽略温度对催化剂的影响)。
①根据图中数据,温度选择
②随着温度的升高,
 的平衡转化率增加但甲醇的选择性降低,请分析其原因:
的平衡转化率增加但甲醇的选择性降低,请分析其原因:
您最近一年使用:0次



