名校
1 . 重氮羰基化合物聚合可获得主链由一个碳原子作为重复结构单元的聚合物,为制备多官能团聚合物提供了新方法。利用该方法合成聚合物P的反应路线如图下列说法错误的是

| A.反应①中有氮元素的单质生成 |
| B.反应②的副产物不可能是网状结构的高分子 |
| C.在酸性或碱性的水溶液中,聚合物P的溶解程度比在水中的大 |
| D.反应②中聚合物和E的化学计量数之比为2:n |
您最近一年使用:0次
名校
2 . 橙花醇的结构简式如图,根据乙烯和乙醇的有关性质,下列有关橙花醇的说法正确的是
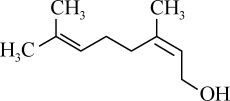
A.分子式为 |
| B.该分子中存在手性碳 |
C.与酸性高锰酸钾反应有 产生 产生 |
| D.能与溴的四氯化碳溶液发生加成反应生成三种产物 |
您最近一年使用:0次
名校
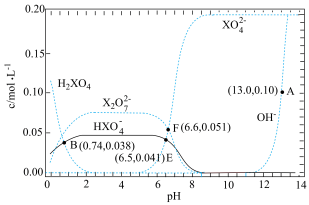
3 . 某温度下,改变 溶液的pH时,各种含X元素粒子及
溶液的pH时,各种含X元素粒子及 浓度变化如图所示。下列有关说法正确的是
浓度变化如图所示。下列有关说法正确的是
 溶液的pH时,各种含X元素粒子及
溶液的pH时,各种含X元素粒子及 浓度变化如图所示。下列有关说法正确的是
浓度变化如图所示。下列有关说法正确的是
A.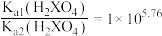 |
B.E点溶液中存在: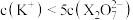 |
C.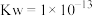 |
D.反应 的平衡常数 的平衡常数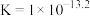 |
您最近一年使用:0次
名校
解题方法
4 . 下列离子方程式正确的是
| A.少量SO2通入Ca(ClO)2溶液:Ca2++ClO-+SO2+H2O=CaSO4↓+Cl-+2H+ |
B.FeI2溶于过量的硝酸溶液中:Fe2++4H++NO =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
C.用热NaOH溶液洗涤试管内壁的硫黄:3S+6OH- SO SO +2S2-+3H2O +2S2-+3H2O |
D.Fe与稀硝酸反应,当n(Fe)﹕n(HNO3)=1﹕3时,3Fe+8H++2NO =3Fe2++2NO↑+4H2O =3Fe2++2NO↑+4H2O |
您最近一年使用:0次
2023-04-21更新
|
1488次组卷
|
5卷引用:黑龙江省哈尔滨师范大学附属中学2022-2023学年高三下学期开学考试化学试题
名校
解题方法
5 . 罗美昔布是一种抗炎药,临床用于治疗风湿性关节炎、牙痛等,化合物W是合成罗美昔布的一种中间体,W合成路线如下:
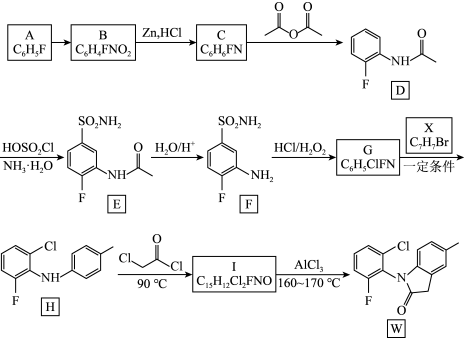
已知:(ⅰ)
(ⅱ)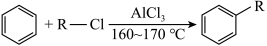
回答下列问题:
(1)A的化学名称为_______ ,B中含氧官能团的名称为_______ 。
(2)由C生成D的反应类型为_______ ;D中所含元素(H除外)第一电离能由大到小的顺序为_______ 。
(3)设置D→E和F→G两步反应的作用是_______ 。
(4)写出由G生成H的化学方程式_______ 。
(5)写出Ⅰ的结构简式_______ 。
(6)M为D的同系物,相对分子质量比D大14。M的同分异构体中同时满足下列条件的共有_______ 种(不考虑立体异构)。
①属于芳香族化合物;
②苯环上含有两个取代基,且位置相对;
③含有 ;
;
④能发生银镜反应。
满足上述条件的同分异构体中,核磁共振氢谱为3∶2∶2∶2∶1的同分异构体为_______ (写出其中两种的结构简式)。

已知:(ⅰ)

(ⅱ)
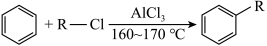
回答下列问题:
(1)A的化学名称为
(2)由C生成D的反应类型为
(3)设置D→E和F→G两步反应的作用是
(4)写出由G生成H的化学方程式
(5)写出Ⅰ的结构简式
(6)M为D的同系物,相对分子质量比D大14。M的同分异构体中同时满足下列条件的共有
①属于芳香族化合物;
②苯环上含有两个取代基,且位置相对;
③含有
 ;
;④能发生银镜反应。
满足上述条件的同分异构体中,核磁共振氢谱为3∶2∶2∶2∶1的同分异构体为
您最近一年使用:0次
2023-04-14更新
|
955次组卷
|
2卷引用:黑龙江省大庆市大庆中学2023届高三下学期模拟预测理综化学试题
名校
解题方法
6 . 已知,25℃时K2Cr2O7溶液中存在以下平衡:
①Cr2O (aq)+H2O(l)
(aq)+H2O(l) 2CrO
2CrO (aq)+2H+(aq) K1=3.27×10-15
(aq)+2H+(aq) K1=3.27×10-15
②Cr2O (aq)+H2O(l)
(aq)+H2O(l) 2HCrO
2HCrO (aq) K2=3.0×10-2
(aq) K2=3.0×10-2
③HCrO (aq)
(aq) CrO
CrO (aq)+H+(aq) K3
(aq)+H+(aq) K3
25℃时,0.1mol/LK2Cr2O7溶液中,lg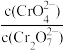 随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
①Cr2O
 (aq)+H2O(l)
(aq)+H2O(l) 2CrO
2CrO (aq)+2H+(aq) K1=3.27×10-15
(aq)+2H+(aq) K1=3.27×10-15②Cr2O
 (aq)+H2O(l)
(aq)+H2O(l) 2HCrO
2HCrO (aq) K2=3.0×10-2
(aq) K2=3.0×10-2③HCrO
 (aq)
(aq) CrO
CrO (aq)+H+(aq) K3
(aq)+H+(aq) K325℃时,0.1mol/LK2Cr2O7溶液中,lg
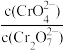 随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是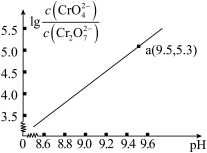
A.0.1mol/LK2Cr2O7溶液中,加入少量的HI气体,c(CrO )增大 )增大 |
| B.溶液颜色不再变化,可以判断该体系达到平衡 |
C.a点溶液中离子浓度关系:c(K+)>c(CrO )>c(Cr2O )>c(Cr2O )>c(H+) )>c(H+) |
D.反应③的化学平衡常数K3=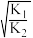 |
您最近一年使用:0次
2023-04-12更新
|
1295次组卷
|
8卷引用:黑龙江省牡丹江市第二高级中学2023-2024学年高三下学期考前热身卷化学(三)试题
黑龙江省牡丹江市第二高级中学2023-2024学年高三下学期考前热身卷化学(三)试题湘豫名校联考2022-2023学年高三上学期一轮复习诊断考试(二)化学试题(已下线)专题十二化学反应速率与平衡(已下线)专题21 电解质溶液图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)仿真卷01-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点09 盘点溶液中的“四大”平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)2023年高考山东卷化学真题变式题(不定项选择题)湖南省2024届高三下学期高考仿真模拟卷(四)化学试题
名校
解题方法
7 . 已知Na2SO3 +S= Na2S2O3,实验室用下述方法制备 固体:①铜和浓硫酸加热产生
固体:①铜和浓硫酸加热产生 ;②将
;②将 通入含
通入含 和
和 的混合溶液,溶液先变浑浊,后逐渐澄清,反应结束;③将溶液经浓缩结晶、过滤洗涤等操作得到
的混合溶液,溶液先变浑浊,后逐渐澄清,反应结束;③将溶液经浓缩结晶、过滤洗涤等操作得到 产品。下列说法错误的是
产品。下列说法错误的是
 固体:①铜和浓硫酸加热产生
固体:①铜和浓硫酸加热产生 ;②将
;②将 通入含
通入含 和
和 的混合溶液,溶液先变浑浊,后逐渐澄清,反应结束;③将溶液经浓缩结晶、过滤洗涤等操作得到
的混合溶液,溶液先变浑浊,后逐渐澄清,反应结束;③将溶液经浓缩结晶、过滤洗涤等操作得到 产品。下列说法错误的是
产品。下列说法错误的是A.①中消耗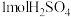 转移 转移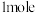 |
| B.②中溶液先变浑浊的原因:2Na2S+3SO2= 2Na2SO3+3S↓ |
C.为提高产品的纯度,混合液中 的最佳比例为1∶2 的最佳比例为1∶2 |
D.用适量 溶液吸收②中逸出的 溶液吸收②中逸出的 、 、 气体,吸收液可直接返回到步骤② 气体,吸收液可直接返回到步骤② |
您最近一年使用:0次
2023-01-14更新
|
2985次组卷
|
9卷引用:黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期第一次验收考试化学试题
名校
8 . 葡萄糖酸钙是一种有机钙盐,外观为白色结晶性或颗粒性粉末,无臭,无味,易溶于沸水,微溶于冷水,不溶于乙醇或乙醚等有机溶剂。葡萄糖酸钙临床上用于治疗骨质疏松症。实验室制备葡萄糖酸钙主要步骤如下:
I.葡萄糖酸溶液的制备
称取适量的葡萄糖[CH2OH(CHOH)4CHO],置于三颈烧瓶中,加入足量的溴水,在磁力搅拌器中沸水浴加热、搅拌得到无色透明的葡萄糖酸溶液。当氧化率达 80%以上时(60min),停止反应,把反应液冷却至 60-70℃待用。
Ⅱ.葡萄糖酸钙的制备
在搅拌下,分批加入足量的碳酸钙至葡萄糖酸溶液中。反应完全后,趁热用下图装置抽滤,得到澄清透明的葡萄糖酸钙溶液。将葡萄糖酸钙溶液转入 100ml 烧杯中冷却至室温,向烧杯中添加适量的无水乙醇,静置 10min 得到悬浊液,抽滤、洗涤、干燥得到白色的葡萄糖酸钙固体。
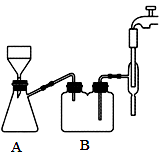
回答下列问题:
(1)步骤Ⅰ中,滴入溴水后,反应的化学方程式为_______ 。
(2)步骤 Ⅱ 中,判断碳酸钙已经足量的实验现象是_______ 。
(3)步骤Ⅱ抽滤时自来水流的作用是使瓶内与大气形成压强差,与普通过滤操作相比,抽滤的优点是_______ ;装置 B 的作用是_______ 。
(4)洗涤操作洗涤剂最合适的是_______ _(填序号),理由是_______ 。
A.冷水 B. 热水 C.乙醇
Ⅲ.葡萄糖酸钙中钙质量分数的测定
测定步骤:
(i)准确称取葡萄糖酸钙 m g,加入去离子水溶解,定容,配成 250mL 溶液。
(ii)用 c mol/L EDTA(H2Y2-)标准溶液润洗滴定管后,装入 EDTA 标准液,调至零刻度。
(iii)向 250mL 锥形瓶中加入 10mL 水、10mL NH3-NH4Cl 缓冲溶液和 5 mL 硫酸镁溶液。滴加 4 滴铬黑 T(HIn2-)指示剂,摇匀。用 EDTA 标准液滴定至终点。记录消耗的 EDTA 标准液的体积。
滴定过程中发生的反应如下:
Mg2+ + HIn2-(蓝色) MgIn-(酒红色)+ H+
MgIn-(酒红色)+ H+
Mg2+ + H2Y2- MgY2- + 2H+
MgY2- + 2H+
MgIn-(酒红色)+ H2Y2- MgY2- + H+ + HIn2-(蓝色)
MgY2- + H+ + HIn2-(蓝色)
(iv)向上述锥形瓶中加入 25.00 mL 葡萄糖酸钙溶液,摇匀,继续用 EDTA 标准液滴定至终点,记录消耗的 EDTA 标准液的总体积。平行滴定三次,测得步骤 iii 中消耗 EDTA 标准液的平均体积为 V1 L,步骤 iv 中 EDTA 标准液的平均总体积为 V2 L。
已知:配合物的稳定常数类似于化学平衡常数,如反应 Fe3+ + 3SCN- Fe(SCN)3 的平衡常数可以看做是 Fe(SCN)3 的稳定常数 K稳,一般情况下,配合物的稳定常数越大,配合物越稳定,两种离子更容易结合。已知下列化合物稳定常数的大小顺序为 CaY2- > MgY2- > MgIn- > CaIn-,其中CaIn-的稳定常数很小,CaIn-不稳定,易导致滴定终点提前。
Fe(SCN)3 的平衡常数可以看做是 Fe(SCN)3 的稳定常数 K稳,一般情况下,配合物的稳定常数越大,配合物越稳定,两种离子更容易结合。已知下列化合物稳定常数的大小顺序为 CaY2- > MgY2- > MgIn- > CaIn-,其中CaIn-的稳定常数很小,CaIn-不稳定,易导致滴定终点提前。
回答下列问题:
(5)步骤 iii 中加入硫酸镁的作用是_______ 。
(6)滴定终点的颜色变化为_______ 。
(7)步骤 iv 中,加入葡萄糖酸钙后发生反应的离子方程式为_______ ,_______ 。
(8)葡萄糖酸钙中钙的质量分数为_______ 。(用 V1、V2、m、c 的代数式表示)
I.葡萄糖酸溶液的制备
称取适量的葡萄糖[CH2OH(CHOH)4CHO],置于三颈烧瓶中,加入足量的溴水,在磁力搅拌器中沸水浴加热、搅拌得到无色透明的葡萄糖酸溶液。当氧化率达 80%以上时(60min),停止反应,把反应液冷却至 60-70℃待用。
Ⅱ.葡萄糖酸钙的制备
在搅拌下,分批加入足量的碳酸钙至葡萄糖酸溶液中。反应完全后,趁热用下图装置抽滤,得到澄清透明的葡萄糖酸钙溶液。将葡萄糖酸钙溶液转入 100ml 烧杯中冷却至室温,向烧杯中添加适量的无水乙醇,静置 10min 得到悬浊液,抽滤、洗涤、干燥得到白色的葡萄糖酸钙固体。

回答下列问题:
(1)步骤Ⅰ中,滴入溴水后,反应的化学方程式为
(2)步骤 Ⅱ 中,判断碳酸钙已经足量的实验现象是
(3)步骤Ⅱ抽滤时自来水流的作用是使瓶内与大气形成压强差,与普通过滤操作相比,抽滤的优点是
(4)洗涤操作洗涤剂最合适的是
A.冷水 B. 热水 C.乙醇
Ⅲ.葡萄糖酸钙中钙质量分数的测定
测定步骤:
(i)准确称取葡萄糖酸钙 m g,加入去离子水溶解,定容,配成 250mL 溶液。
(ii)用 c mol/L EDTA(H2Y2-)标准溶液润洗滴定管后,装入 EDTA 标准液,调至零刻度。
(iii)向 250mL 锥形瓶中加入 10mL 水、10mL NH3-NH4Cl 缓冲溶液和 5 mL 硫酸镁溶液。滴加 4 滴铬黑 T(HIn2-)指示剂,摇匀。用 EDTA 标准液滴定至终点。记录消耗的 EDTA 标准液的体积。
滴定过程中发生的反应如下:
Mg2+ + HIn2-(蓝色)
 MgIn-(酒红色)+ H+
MgIn-(酒红色)+ H+ Mg2+ + H2Y2-
 MgY2- + 2H+
MgY2- + 2H+ MgIn-(酒红色)+ H2Y2-
 MgY2- + H+ + HIn2-(蓝色)
MgY2- + H+ + HIn2-(蓝色) (iv)向上述锥形瓶中加入 25.00 mL 葡萄糖酸钙溶液,摇匀,继续用 EDTA 标准液滴定至终点,记录消耗的 EDTA 标准液的总体积。平行滴定三次,测得步骤 iii 中消耗 EDTA 标准液的平均体积为 V1 L,步骤 iv 中 EDTA 标准液的平均总体积为 V2 L。
已知:配合物的稳定常数类似于化学平衡常数,如反应 Fe3+ + 3SCN-
 Fe(SCN)3 的平衡常数可以看做是 Fe(SCN)3 的稳定常数 K稳,一般情况下,配合物的稳定常数越大,配合物越稳定,两种离子更容易结合。已知下列化合物稳定常数的大小顺序为 CaY2- > MgY2- > MgIn- > CaIn-,其中CaIn-的稳定常数很小,CaIn-不稳定,易导致滴定终点提前。
Fe(SCN)3 的平衡常数可以看做是 Fe(SCN)3 的稳定常数 K稳,一般情况下,配合物的稳定常数越大,配合物越稳定,两种离子更容易结合。已知下列化合物稳定常数的大小顺序为 CaY2- > MgY2- > MgIn- > CaIn-,其中CaIn-的稳定常数很小,CaIn-不稳定,易导致滴定终点提前。回答下列问题:
(5)步骤 iii 中加入硫酸镁的作用是
(6)滴定终点的颜色变化为
(7)步骤 iv 中,加入葡萄糖酸钙后发生反应的离子方程式为
(8)葡萄糖酸钙中钙的质量分数为
您最近一年使用:0次
9 . 羟基自由基(·OH)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 CO2 和 H2O 的原电池-电解池组合装置(如下图所示),该装置能实现发电、环保二位一体。下列说法错误的是
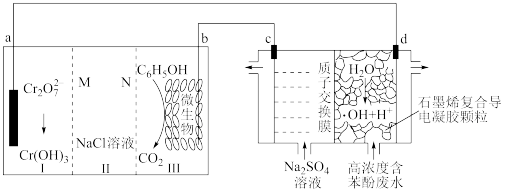

| A.系统工作时,电流由 b 极经 III、II、I 室流向 a 极 |
| B.d 极区苯酚被氧化的化学方程式为 C6H5OH+28·OH = 6 CO2↑+17 H2O |
| C.系统工作时,每转移 28mol e-消耗 1mol 苯酚 |
D.a 电极的电极反应式:7H2O + Cr2O + 6 e-=2 Cr(OH)3 + 8 OH- + 6 e-=2 Cr(OH)3 + 8 OH- |
您最近一年使用:0次
名校
解题方法
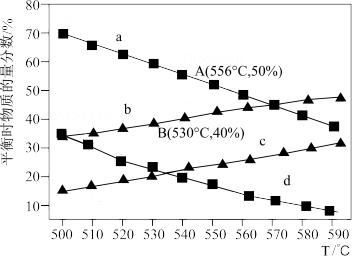
10 . 利用丙烷(C3H8)在无氧条件下制备丙烯(C3H6)的反应方程式为:C3H8(g) C3H6(g)+H2(g) △H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是
C3H6(g)+H2(g) △H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是
 C3H6(g)+H2(g) △H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是
C3H6(g)+H2(g) △H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是
| A.c曲线表示的是0.01MPa压强下丙烯随温度变化的物质的量分数 |
| B.A点对应的该反应平衡常数Kp=1.25MPa(Kp为以分压表示的平衡常数) |
| C.B点丙烷的平衡转化率为33.3% |
| D.实际生产过程中需通入一定量水蒸气,其目的是稀释原料气,增大丙烯的平衡产率 |
您最近一年使用:0次
2022-09-04更新
|
1510次组卷
|
5卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高二10月月考化学试题
黑龙江省牡丹江市第一高级中学2022-2023学年高二10月月考化学试题重庆市南开中学校2022-2023学年高三上学期第一次质量检测联考化学试题(已下线)2022年北京高考真题变式题1-14重庆市南开中学2022-2023学年高三上学期第一次质检化学试题(已下线)2022年北京高考真题化学试题变式题(选择题11-14)



