名校
解题方法
1 . 溶液X中含有下表离子中的某5种,且其浓度均为 (不考虑水的电离与离子水解)。向X溶液中加入足量稀盐酸,有无色气体生成,经分析,反应前后阴离子种类没有变化。下列叙述不正确的是
(不考虑水的电离与离子水解)。向X溶液中加入足量稀盐酸,有无色气体生成,经分析,反应前后阴离子种类没有变化。下列叙述不正确的是
 (不考虑水的电离与离子水解)。向X溶液中加入足量稀盐酸,有无色气体生成,经分析,反应前后阴离子种类没有变化。下列叙述不正确的是
(不考虑水的电离与离子水解)。向X溶液中加入足量稀盐酸,有无色气体生成,经分析,反应前后阴离子种类没有变化。下列叙述不正确的是阳离子 | 阴离子 |
|
|
| A.X溶液中可能含3种阳离子、2种阴离子 | B.X溶液中不可能含有 或 或 |
C.生成的无色气体是 | D.根据电荷守恒,原溶液中一定含 |
您最近一年使用:0次
2023-04-20更新
|
1309次组卷
|
9卷引用:辽宁省大连市金普新区省示范性高中2022届高三上学期第一次联合考试化学试题
辽宁省大连市金普新区省示范性高中2022届高三上学期第一次联合考试化学试题黑龙江省鹤岗市绥滨县第一中学2021-2022学年高三上学期期中考试化学试题辽宁省沈阳市铁路实验中学2022-2023学年高一下学期第一次月考化学试题(已下线)上海市华东师范大学第二附属中学2021-2022学年高一下学期3月阶段反馈化学试题上海市育才中学2022-2023学年高三上学期10月月考化学试题黑龙江省哈尔滨师范大学附属中学2022-2023学年高三下学期开学考试化学试题黑龙江省哈尔滨师范大学附属中学2024届高三上学期开学考试化学试题河北省秦皇岛市昌黎第一中学2023届高三第一次调研考试化学试题河北省石家庄市第二中学2023-2024高一上学期第一次诊断测评化学试题
名校
解题方法
2 . 研究表明:丰富的CO2可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)枯竭危机,同时又可缓解由CO2累积所产生的温室效应,实现CO2的良性循环。
(1)目前工业上有一种方法是用CO2加氢合成低碳烯烃。现以合成乙烯(C2H4)为例,该过程分两步进行:
第一步:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41.3kJ·mol-1
第二步:2CO(g)+4H2(g)=C2H4(g)+2H2O(g) ΔH=-210.5kJ·mol-1
①CO2加氢合成乙烯的热化学方程式为___ 。
②一定条件下的密闭容器中,上述反应达到平衡后,要加快反应速率并提高CO2的转化率,可以采取的措施是___ (填字母)。
A.减小压强 B.增大H2浓度 C.加入适当催化剂 D.分离出水蒸气
(2)另一种方法是将CO2和H2在催化剂条件下生成甲醇蒸气和水蒸气。现在10L恒容密闭容器中投入1molCO2和2.75molH2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。在不同条件下测得平衡时甲醇的物质的量随温度、压强的变化如图所示:
CH3OH(g)+H2O(g)。在不同条件下测得平衡时甲醇的物质的量随温度、压强的变化如图所示:
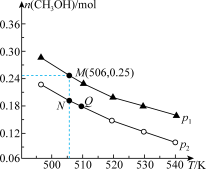
①能判断该反应达到化学平衡状态的是___  填字母
填字母 。
。
a.c(H2):c(CH3OH)=3:1 b.容器内氢气的体积分数不再改变
c.容器内气体的密度不再改变 d.容器内压强不再改变
②上述反应的ΔH___ 0(填“>”或“<”),图中压强P1___ P2(填“>”或“<”)。
③经测定知Q点时容器的压强是反应前压强的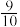 ,则Q点H2的转化率为
,则Q点H2的转化率为___ 。
④N点时,该反应的平衡常数K=___ (计算结果保留两位小数)。
(3)工业生产中应用:COS的水解反应为COS(g)+H2O(g) CO2(g)+H2S(g) ΔH<0。某温度时,用活性α—Al2O3作催化剂,在恒容密闭容器中COS(g)的平衡转化率随不同投料比[
CO2(g)+H2S(g) ΔH<0。某温度时,用活性α—Al2O3作催化剂,在恒容密闭容器中COS(g)的平衡转化率随不同投料比[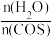 ]的转化关系如图甲所示。其他条件相同时,改变反应温度,测得一定时间内COS的水解转化率如图乙所示:
]的转化关系如图甲所示。其他条件相同时,改变反应温度,测得一定时间内COS的水解转化率如图乙所示:
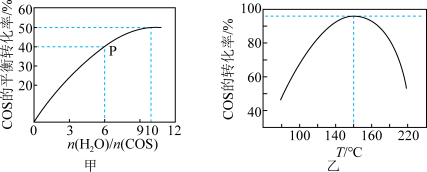
①该反应的最佳条件为:投料比[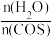 ]=
]=___ ,温度___ 。
②P点对应的平衡常数为___ 。(保留小数点后2位)
③当温度升高到一定值后,发现一定时间内COS(g)的水解转化率降低;猜测可能的原因是___ 。
(1)目前工业上有一种方法是用CO2加氢合成低碳烯烃。现以合成乙烯(C2H4)为例,该过程分两步进行:
第一步:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41.3kJ·mol-1
第二步:2CO(g)+4H2(g)=C2H4(g)+2H2O(g) ΔH=-210.5kJ·mol-1
①CO2加氢合成乙烯的热化学方程式为
②一定条件下的密闭容器中,上述反应达到平衡后,要加快反应速率并提高CO2的转化率,可以采取的措施是
A.减小压强 B.增大H2浓度 C.加入适当催化剂 D.分离出水蒸气
(2)另一种方法是将CO2和H2在催化剂条件下生成甲醇蒸气和水蒸气。现在10L恒容密闭容器中投入1molCO2和2.75molH2,发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。在不同条件下测得平衡时甲醇的物质的量随温度、压强的变化如图所示:
CH3OH(g)+H2O(g)。在不同条件下测得平衡时甲醇的物质的量随温度、压强的变化如图所示:
①能判断该反应达到化学平衡状态的是
 填字母
填字母 。
。a.c(H2):c(CH3OH)=3:1 b.容器内氢气的体积分数不再改变
c.容器内气体的密度不再改变 d.容器内压强不再改变
②上述反应的ΔH
③经测定知Q点时容器的压强是反应前压强的
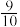 ,则Q点H2的转化率为
,则Q点H2的转化率为④N点时,该反应的平衡常数K=
(3)工业生产中应用:COS的水解反应为COS(g)+H2O(g)
 CO2(g)+H2S(g) ΔH<0。某温度时,用活性α—Al2O3作催化剂,在恒容密闭容器中COS(g)的平衡转化率随不同投料比[
CO2(g)+H2S(g) ΔH<0。某温度时,用活性α—Al2O3作催化剂,在恒容密闭容器中COS(g)的平衡转化率随不同投料比[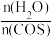 ]的转化关系如图甲所示。其他条件相同时,改变反应温度,测得一定时间内COS的水解转化率如图乙所示:
]的转化关系如图甲所示。其他条件相同时,改变反应温度,测得一定时间内COS的水解转化率如图乙所示:
①该反应的最佳条件为:投料比[
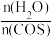 ]=
]=②P点对应的平衡常数为
③当温度升高到一定值后,发现一定时间内COS(g)的水解转化率降低;猜测可能的原因是
您最近一年使用:0次
解题方法
3 . 青蒿素是烃的含氧衍生物,为无色针状晶体,在乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素60℃以上易分解,青蒿素是高效的抗疟药。已知:乙醚沸点为35℃。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的。
(1)青蒿素在超临界CO2中有很强的溶解性,萃取青蒿素________ (填”能”或“不能”)用超临界CO2作萃取剂;中医古籍《肘后备急方》中“青蒿一握,以水二升渍,绞取汁,尽服之”______ (填“是”或“不是”)为了提取纤维素。现有四氯化碳(沸点76.5℃)和乙醚两种溶剂,应选用__________ 作为萃取剂;青蒿素组成元素中电负性较大的两种元素第一电离能由大到小排序为__________ (填元素符号)。
(2)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与_________ (填字母)具有相似的性质。说明青蒿素的结构中含有_______ (填官能团名称)。
A.乙醇B.乙酸乙酯C.乙酸D.酰胺E.葡萄糖
(3)青蒿素的质谱数据中有一个峰值与另一种抗疟药鹰爪素相同,而鹰爪素的该质谱峰对应过氧基团,于是推测青蒿素中含有_____ (填粒子的电子式)。青蒿素所属晶体类型为_________ 。1974年中科院上海有机所和生物物理研究所在研究青蒿素功能基团的过程中,屠呦呦团队发明了双氢青蒿素。从青蒿素到生成双氢青蒿素发生了_____ 反应。
(4)科学家对H2O2分子结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:甲: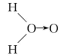 、乙: H—O—O—H,甲式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的分子结构,设计并完成了下列实验:
、乙: H—O—O—H,甲式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的分子结构,设计并完成了下列实验:
a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂)。
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)________ 。
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:_______________________ 。
(1)青蒿素在超临界CO2中有很强的溶解性,萃取青蒿素
(2)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与
A.乙醇B.乙酸乙酯C.乙酸D.酰胺E.葡萄糖
(3)青蒿素的质谱数据中有一个峰值与另一种抗疟药鹰爪素相同,而鹰爪素的该质谱峰对应过氧基团,于是推测青蒿素中含有
(4)科学家对H2O2分子结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:甲:
 、乙: H—O—O—H,甲式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的分子结构,设计并完成了下列实验:
、乙: H—O—O—H,甲式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的分子结构,设计并完成了下列实验:a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂)。
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:
您最近一年使用:0次
名校
解题方法
4 . 某小组同学设计实验探究镁与铵盐溶液的反应,记录如下:
根据上述实验所得结论正确的是
| 实验编号 | ① | ② | ③ | ④ |
| 溶液种类 | 1  | 0.5  | 0.1  |  |
 | 0.48 | 0.48 | 0.48 | 0.48 |
V(溶液) | 100 | 100 | 100 | 100 |
| 实验现象 | 有气体产生,并产生白色沉淀 | 有气体产生,并产生白色沉淀 | 有气体产生,并产生白色沉淀 | 几乎看不到现象 |
6h时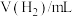 | 433 | 255 | 347 | 12 |
A.实验②中发生的反应为 |
B.由实验①、③可得,溶液中 越大,反应速率越快 越大,反应速率越快 |
C.由实验①、②可得,溶液中阴离子的种类对产生 的速率有影响 的速率有影响 |
D.由实验①~④可得,溶液的 越小,产生 越小,产生 的速率越快 的速率越快 |
您最近一年使用:0次
2021-04-09更新
|
3310次组卷
|
8卷引用:2021年辽宁高考化学试题变式题11-19
2021年辽宁高考化学试题变式题11-19河北省石家庄市2021届高三一模考试化学试题(已下线)押山东卷第11题 关于表格实验题的考查-备战2021年高考化学临考题号押题(山东卷)(已下线)2021年秋季高三化学开学摸底考试卷01(广东专用)辽宁省东北育才学校高中部高三2021-2022下学期开学初第六次模拟考试化学试题湖南省长沙市雅礼中学2022-2023学年高三上学期第五次月考化学试题湖北省荆州市沙市区湖北省沙市中学等5校2022-2023学年高二下学期4月期中考试化学试题广东省广州市广外、铁一、广附三校2022-2023学年高一下学期期末联考化学试题
5 . 某温度下,分别向10 mL浓度均为0.1mol·L-1的CuCl2和ZnCl2溶液中滴加0.1 mol·L-1的Na2S溶液,滴加过程中溶液中-lg c(Cu2+)和-lg c(Zn2+)与Na2S溶液体积(V)的关系如图所示。[已知:Ksp(ZnS)>Ksp(CuS),lg 3≈0.5],下列说法错误的是


| A.溶液pH:a<b<e |
| B.a点的ZnCl2溶液中:c(Cl-)<2[c(Zn2+)+c(H+)] |
| C.a-b-e为滴定CuCl2溶液的曲线 |
| D.d点纵坐标约为33.9 |
您最近一年使用:0次
2021-01-15更新
|
1942次组卷
|
2卷引用:辽宁省实验中学、大连八中、大连二十四中、鞍山一中、东北育才学校五校协作体2020-2021学年高二上学期期末化学试题
名校
解题方法
6 . 丙烷与溴原子能发生以下两种反应:
① CH3CH2CH3(g) + Br·(g) → CH3CH2CH2·(g) + HBr(g)
② CH3CH2CH3(g) + Br·(g) → CH3CH·CH3 (g) + HBr(g)
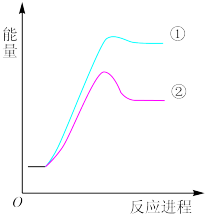
反应过程的能量变化如图所示。下列说法正确的是
① CH3CH2CH3(g) + Br·(g) → CH3CH2CH2·(g) + HBr(g)
② CH3CH2CH3(g) + Br·(g) → CH3CH·CH3 (g) + HBr(g)
反应过程的能量变化如图所示。下列说法正确的是

| A.反应①是放热反应 |
| B.反应②使用了催化剂 |
| C.产物中 CH3CH2CH2·(g)含量比 CH3CH·CH3(g)低 |
| D.CH3CH2CH2·(g)转变为 CH3CH·CH3(g)时需要吸热 |
您最近一年使用:0次
2020-12-23更新
|
2372次组卷
|
9卷引用:2021年辽宁高考化学试题变式题11-19
2021年辽宁高考化学试题变式题11-19上海市闵行区2021届高三一模化学试题(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)黑龙江省大庆市实验中学2021-2022学年高三上学期开学考试化学试题上海市徐汇区2023届高三一模化学试题(已下线)专题12 反应机理和能量变化
名校
解题方法
7 . 有一化合物X,其水溶液为浅绿色,有如图所示的转化关系(部分反应物、生成物已略)。其中B、D、E、F均为无色气体,M、L为常见的金属单质,C为难溶于水的红褐色固体。在混合液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀 ,H和M反应可放出大量的热。(电解装置中用石墨做电极)下列说法正确的是( )
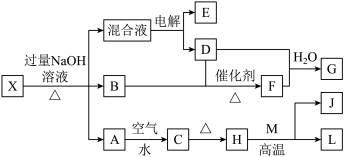

| A.生成G的反应中,生成1molG转移1mol电子 |
| B.此转化关系中只有一个置换反应 |
| C.“混合液”电解一段时间后pH不变 |
| D.检验X中是否存在Cl-,所用试剂为HNO3酸化的AgNO3 |
您最近一年使用:0次
2020-12-02更新
|
1933次组卷
|
3卷引用:辽宁省沈阳市东北育才学校2021-2022学年高三上学期学段考试化学试题
名校
解题方法
8 . 已知还原性:SO >I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
>I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
 >I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
>I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )A.当a=b时,发生的离子反应为SO +Cl2+H2O=SO +Cl2+H2O=SO +2H++2Cl- +2H++2Cl- |
B.当5a=4b时,发生的离子反应为4SO +2I-+5Cl2+4H2O=4SO +2I-+5Cl2+4H2O=4SO +I2+8H++10Cl- +I2+8H++10Cl- |
C.当a≤b≤ a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol |
D.当a<b< a时,溶液中SO a时,溶液中SO 、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b 、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b |
您最近一年使用:0次
2020-08-18更新
|
3399次组卷
|
7卷引用:辽宁省实验中学2021-2022学年高一上学期11月期中阶段测试化学试题
辽宁省实验中学2021-2022学年高一上学期11月期中阶段测试化学试题(已下线)解密04 离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密04 离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练黑龙江省哈尔滨师范大学附属中学2020-2021学年高二下学期期末考试化学试题(已下线)课时06 与量有关的离子方程式书写-2022年高考化学一轮复习小题多维练(全国通用)浙江省瑞安市上海新纪元高级中学2019-2020学年高一下学期期末考试化学试题(2)福建省泉州市永春第一中学2022-2023学年高一上学期期末考试化学试题
名校
9 . 足量的铜与一定量的浓硝酸充分反应,得到4.48L(标准状况)NO2与NO的混合气体,这些气体与一定体积的O2混合后通入水中,恰好被完全吸收生成硝酸。向所得硝酸铜溶液中加入100mL4mol·L-1NaOH溶液,Cu2+恰好沉淀完全。下列说法正确的是
| A.此反应过程中转移了0.5mol的电子 |
| B.消耗氧气的体积为1.12L(标准状况) |
| C.参加反应的HNO3是0.45mol |
| D.混合气体中含2.24L(标准状况)NO |
您最近一年使用:0次
2020-07-22更新
|
3026次组卷
|
11卷引用:辽宁省大连市一0三中学2020-2021学年高一4月月考化学试题
辽宁省大连市一0三中学2020-2021学年高一4月月考化学试题辽宁省大连市旅顺口区2019-2020学年高一下学期期末考试化学试题辽宁省大连市2019-2020学年高一下学期期末考试化学试题山西省实验中学2020-2021学年高一下学期第一次月考化学试题辽宁省部分中学2019-2020高一下学期期末考试化学试题重庆市缙云教育联盟2020-2021学年高一9月月考化学试题黑龙江省鹤岗市第一中学2021-2022学年高一下学期4月月考化学试题云南省曲靖市第一中学2022-2023学年高一下学期期末考试化学试题安徽省铜陵市第一中学2022-2023 学年高一下学期期中教学质量检测化学试题云南省开远市第一中学校2022-2023学年高一下学期期末考试化学试题重庆市万州第二高级中学2023-2024学年高一下学期3月月考试题 化学试题
名校
解题方法
10 . 有关 反应的叙述正确的为
反应的叙述正确的为
 反应的叙述正确的为
反应的叙述正确的为| A.还原剂与氧化剂物质的量之比为5:3 |
| B.生成lmolO2,反应共转移4mol电子 |
C.若有5mol水做还原剂时,被BrF3还原的BrF3为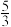 mol mol |
| D.若有5mol水参与反应时,被水还原的BrF3为2mol |
您最近一年使用:0次
2019-11-24更新
|
2665次组卷
|
7卷引用:辽宁省实验中学2021-2022学年高一上学期11月期中阶段测试化学试题

 、
、 、
、 、
、 、
、
 、
、 、
、 、
、


