1 .  NaOH溶液滴定20.00mL
NaOH溶液滴定20.00mL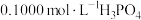 溶液时,
溶液时,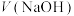 、各含磷元素微粒的
、各含磷元素微粒的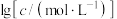 和pH的关系如图。下列说法错误的是
和pH的关系如图。下列说法错误的是
 NaOH溶液滴定20.00mL
NaOH溶液滴定20.00mL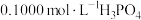 溶液时,
溶液时,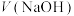 、各含磷元素微粒的
、各含磷元素微粒的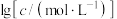 和pH的关系如图。下列说法错误的是
和pH的关系如图。下列说法错误的是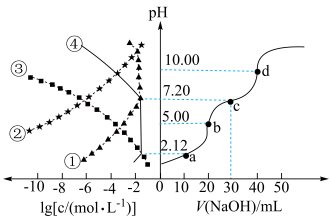
A. 的 的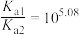 |
| B.水的电离程度:d>c>b>a |
C.③为 的 的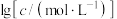 与pH的关系 与pH的关系 |
D.c点时,溶液中存在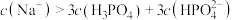 |
您最近一年使用:0次
2024-06-08更新
|
175次组卷
|
4卷引用:辽宁省凌源市2024届高三下学期第三次模拟考试化学试卷
名校
2 . Ⅰ、CO2催化加氢制CH3OH的反应体系中,发生的主要反应有:
①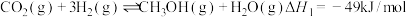
②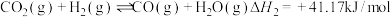
③
(1)③___________ (填“高温自发”“低温自发”或“任何温度下都自发”),该反应中活化能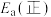
___________ 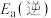 。(填“>”或“<”)
。(填“>”或“<”)
(2)反应①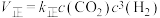 ,
, ,(
,( 、
、 只是温度的函数)。若该温度下的平衡常数K=10,则
只是温度的函数)。若该温度下的平衡常数K=10,则
___________  。升高温度,
。升高温度, 增大的倍数
增大的倍数___________ (填“大于”“小于”或“等于”) 增大的倍数。
增大的倍数。
(3)一定压强下,往某密闭容器中按投料比 充入H2和CO2,反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
充入H2和CO2,反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。___________ 。
A.恒温恒压时充入氦气,反应①、③的平衡均逆向移动,反应②不移动
B.增大 的比值,H2的平衡转化率增大
的比值,H2的平衡转化率增大
C.图中X、Y分别代表CO、H2O
D.体系中的CO2的物质的量分数随温度变化不大,原因是温度变化,反应①、②的平衡移动方向相反
②在一定温度下,向恒容密闭容器中充入lnolCO2和3molH2,仅发生反应①。实验测得CH3OH的平衡分压与起始投料比[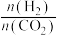 ]的关系如图。起始时容器内气体的总压强为8pkPa,则b点时反应的平衡常数Kp=
]的关系如图。起始时容器内气体的总压强为8pkPa,则b点时反应的平衡常数Kp=___________  (用含p的表达式表示)。(已知:用气体分压计算的平衡常数为Kp,分压=总压×物质的量分数)。
(用含p的表达式表示)。(已知:用气体分压计算的平衡常数为Kp,分压=总压×物质的量分数)。
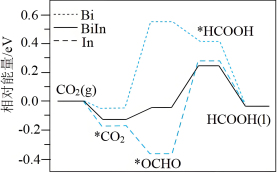
(4)我国学者探究了BiIn合金催化剂电化学还原CO2生产HCOOH的催化性能及机理,并通过DFT计算催化剂表面该还原过程的物质的相对能量,如图所示(带“*”表示物质处于吸附态),试从图分析,采用BiIn合金催化剂优于中金属Bi和单金属In催化剂的原因分别是___________ 。
①
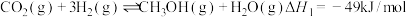
②
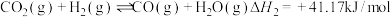
③

(1)③
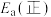
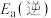 。(填“>”或“<”)
。(填“>”或“<”)(2)反应①
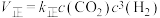 ,
, ,(
,( 、
、 只是温度的函数)。若该温度下的平衡常数K=10,则
只是温度的函数)。若该温度下的平衡常数K=10,则
 。升高温度,
。升高温度, 增大的倍数
增大的倍数 增大的倍数。
增大的倍数。(3)一定压强下,往某密闭容器中按投料比
 充入H2和CO2,反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
充入H2和CO2,反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。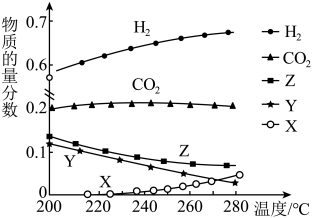
A.恒温恒压时充入氦气,反应①、③的平衡均逆向移动,反应②不移动
B.增大
 的比值,H2的平衡转化率增大
的比值,H2的平衡转化率增大C.图中X、Y分别代表CO、H2O
D.体系中的CO2的物质的量分数随温度变化不大,原因是温度变化,反应①、②的平衡移动方向相反
②在一定温度下,向恒容密闭容器中充入lnolCO2和3molH2,仅发生反应①。实验测得CH3OH的平衡分压与起始投料比[
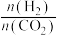 ]的关系如图。起始时容器内气体的总压强为8pkPa,则b点时反应的平衡常数Kp=
]的关系如图。起始时容器内气体的总压强为8pkPa,则b点时反应的平衡常数Kp= (用含p的表达式表示)。(已知:用气体分压计算的平衡常数为Kp,分压=总压×物质的量分数)。
(用含p的表达式表示)。(已知:用气体分压计算的平衡常数为Kp,分压=总压×物质的量分数)。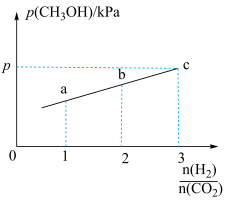
(4)我国学者探究了BiIn合金催化剂电化学还原CO2生产HCOOH的催化性能及机理,并通过DFT计算催化剂表面该还原过程的物质的相对能量,如图所示(带“*”表示物质处于吸附态),试从图分析,采用BiIn合金催化剂优于中金属Bi和单金属In催化剂的原因分别是
您最近一年使用:0次
2024-06-06更新
|
336次组卷
|
3卷引用:2024届辽宁省实验中学高三下学期考前模拟训练(五模)化学试卷
2024·黑龙江吉林·模拟预测
解题方法
3 . 乙苯是生产苯乙烯的一种重要工业原料,工业上一般采用苯烷基化法制取乙苯。回答下列问题:
I.目前工业上生产乙苯主要采用乙烷裂解和苯与乙烯催化烷基化法,发生的反应如下:
①C2H6(g)=C2H4(g)+H2(g)______ (填字母),反应③在热力学上能实现的温度范围为_______ 。______ eV,该步基元反应的化学方程式为______ 。
②能提高反应①平衡转化率的适宜条件为_______ (填字母)。
A.升温 B.加压 C.使用高效的催化剂 D.分离出H2
II.工业上还可以在催化条件下用氯乙烷和苯反应制取乙苯,发生的反应如下:
乙苯的选择性=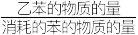 ×100%
×100%
Ka为为物质的量分数平衡常数_______ 。
(4)反应最适宜的时间为_______ (填字母)。
A.10min B.20min C.30min
(5)该温度下,反应④的平衡常数Kx=______ 。
I.目前工业上生产乙苯主要采用乙烷裂解和苯与乙烯催化烷基化法,发生的反应如下:
①C2H6(g)=C2H4(g)+H2(g)
②C2H4(g)+ (g)=
(g)=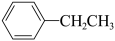 (g)
(g)
③C2H6(g)+ (g)=
(g)= (g)+H2(g)
(g)+H2(g)


②能提高反应①平衡转化率的适宜条件为
A.升温 B.加压 C.使用高效的催化剂 D.分离出H2
II.工业上还可以在催化条件下用氯乙烷和苯反应制取乙苯,发生的反应如下:
④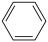 (g)+CH3CH2Cl(g)=
(g)+CH3CH2Cl(g)= (g)+HCl(g)
(g)+HCl(g)
⑤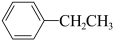 (g)+CH3CH2Cl(g)=
(g)+CH3CH2Cl(g)=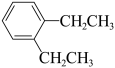 (g)+HCl(g)
(g)+HCl(g)
乙苯的选择性=
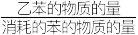 ×100%
×100%Ka为为物质的量分数平衡常数

(4)反应最适宜的时间为
A.10min B.20min C.30min
(5)该温度下,反应④的平衡常数Kx=
您最近一年使用:0次
4 . 已知SrF2为难溶于水、可溶于酸的盐。常温下,向SrF2浊液中滴加稀盐酸,溶液中-lgc(X)(X为Sr2+)变化关系如图。下列说法正确的是

A.L1表示-lgc(Sr2+)与lg 的变化关系 的变化关系 |
| B.Ksp(SrF2)的数量级为10-8 |
| C.c点溶液的pH=3.2 |
| D.b点溶液中存在:2c(Sr2+)+c(H+)=c(OH-)+c(F-) |
您最近一年使用:0次
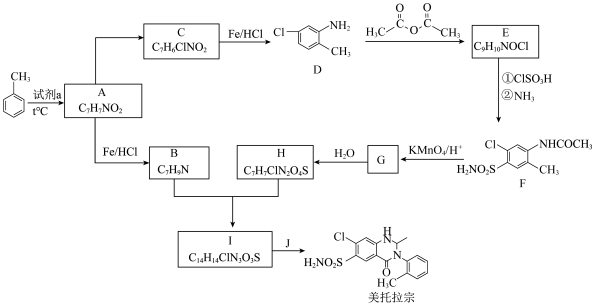
5 . 某研究小组以甲苯为起始原料,按下列路线合成利尿药美托拉宗。
(1)试剂a是_______ 。
(2)C→D的反应类型是_______ 。
(3)E分子中的官能团有_______ 。
(4)属于芳香族化合物的B的同分异构体有_______ 个(提示:不包括B)。
(5)写出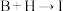 的化学方程式
的化学方程式_______ 。
(6)从D→H的流程看,D→E的主要目的是_______ 。
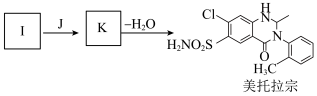
(7)有人认为由I合成美托拉宗的过程如下:_______ ,K的结构简式_______ 。
已知:ⅰ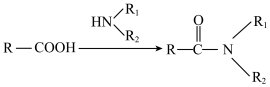 。
。
ⅱ.
(1)试剂a是
(2)C→D的反应类型是
(3)E分子中的官能团有
(4)属于芳香族化合物的B的同分异构体有
(5)写出
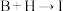 的化学方程式
的化学方程式(6)从D→H的流程看,D→E的主要目的是
(7)有人认为由I合成美托拉宗的过程如下:
您最近一年使用:0次
名校
6 . 将一定量的锌、镁合金与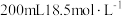 浓硫酸充分反应后,固体完全溶解,同时生成气体
浓硫酸充分反应后,固体完全溶解,同时生成气体 (生成气体全部逸出,测定条件为标准状况)。将反应后的溶液稀释到
(生成气体全部逸出,测定条件为标准状况)。将反应后的溶液稀释到 ,测得稀释后溶液中的
,测得稀释后溶液中的 浓度为
浓度为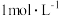 。向反应后的溶液中加入
。向反应后的溶液中加入 溶液
溶液 时,所得沉淀质量最大,其质量为
时,所得沉淀质量最大,其质量为 。下列叙述中错误的是
。下列叙述中错误的是
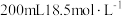 浓硫酸充分反应后,固体完全溶解,同时生成气体
浓硫酸充分反应后,固体完全溶解,同时生成气体 (生成气体全部逸出,测定条件为标准状况)。将反应后的溶液稀释到
(生成气体全部逸出,测定条件为标准状况)。将反应后的溶液稀释到 ,测得稀释后溶液中的
,测得稀释后溶液中的 浓度为
浓度为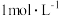 。向反应后的溶液中加入
。向反应后的溶液中加入 溶液
溶液 时,所得沉淀质量最大,其质量为
时,所得沉淀质量最大,其质量为 。下列叙述中错误的是
。下列叙述中错误的是A.气体A中 和 和 的体积比为 的体积比为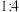 | B.该合金中锌、镁的物质的量之比为 |
C.该实验所有 的浓度是 的浓度是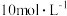 | D.沉淀质量最大时,溶液中所含溶质的质量为 |
您最近一年使用:0次
7 . 常温下,向 饱和溶液[有足量
饱和溶液[有足量 固体]中滴加氨水,发生反应:
固体]中滴加氨水,发生反应: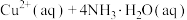

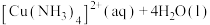 ,溶液中
,溶液中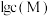 与
与 的关系如图所示,其中
的关系如图所示,其中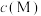 表示
表示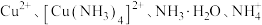 的浓度,单位为
的浓度,单位为 。下列说法正确的是
。下列说法正确的是
 饱和溶液[有足量
饱和溶液[有足量 固体]中滴加氨水,发生反应:
固体]中滴加氨水,发生反应: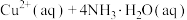

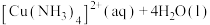 ,溶液中
,溶液中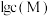 与
与 的关系如图所示,其中
的关系如图所示,其中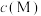 表示
表示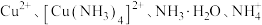 的浓度,单位为
的浓度,单位为 。下列说法正确的是
。下列说法正确的是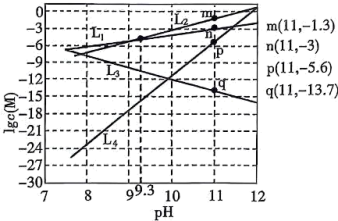
A. 表示溶液中 表示溶液中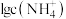 与 与 的关系 的关系 |
B. 的溶度积常数 的溶度积常数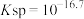 |
C. 时,溶液中: 时,溶液中: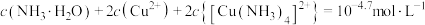 |
D.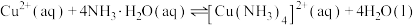 的平衡常数 的平衡常数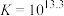 |
您最近一年使用:0次
解题方法
8 . 甲醇和乙醇都是清洁能源,也是重要的化工原料。回答下列问题:
(1)工业上利用合成气合成甲醇: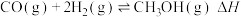
已知:① ;
;
②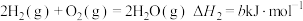 ;
;
③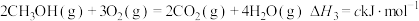
上述反应中的
___________  。
。
(2)一定温度下,在恒容密闭容器中充入1molCO和1molH2,在固体催化剂作用下合成甲醇: ,下列叙述错误的是___________(填字母)。
,下列叙述错误的是___________(填字母)。
(3)甲醇是一种潜在储氢材料。我国学者研究甲醇在钯基催化剂表面上分解制氢: ,其反应历程如图a所示(吸附在催化剂表面的物种用“*”表示)。
,其反应历程如图a所示(吸附在催化剂表面的物种用“*”表示)。___________ 下(高温、低温、任意温度)自发进行;图示历程包括___________ 个基元反应;其中决速反应是反应___________ (填序号),写出该步反应式:___________ 。
(4)工业上,可以采用CO2催化还原制备CH3OH、CH3CH2OH.发生反应如下:
① (主反应);
(主反应);
② (主反应);
(主反应);
③ (副反应)。
(副反应)。
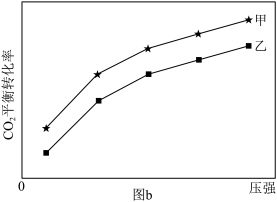
一定温度下,在甲、乙体积相同的反应容器中分别充入1molCO2和3molH2,发生上述反应,其中一个容器使用水分子膜分离技术,另一个容器不使用水分子膜分离技术。实验测得CO2平衡转化率与压强关系如图b所示。其他条件相同,增大压强,CO2平衡转化率增大,其原因是___________ ;采用水分子膜分离技术的容器是___________ (填“甲”或“乙”)。 为
为___________  。(写出数字表达式即可,分压=总压×物质的量分数)
。(写出数字表达式即可,分压=总压×物质的量分数)
(1)工业上利用合成气合成甲醇:
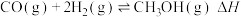
已知:①
 ;
;②
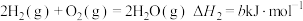 ;
;③
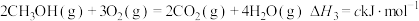
上述反应中的

 。
。(2)一定温度下,在恒容密闭容器中充入1molCO和1molH2,在固体催化剂作用下合成甲醇:
 ,下列叙述错误的是___________(填字母)。
,下列叙述错误的是___________(填字母)。| A.当CO体积分数不变时达到平衡状态 |
| B.平衡后充入少量氩气,平衡不移动 |
| C.平衡后再充入0.1molCO和0.1molH2,CO平衡转化率增大 |
| D.增大催化剂质量,正、逆反应速率同倍数增大 |
(3)甲醇是一种潜在储氢材料。我国学者研究甲醇在钯基催化剂表面上分解制氢:
 ,其反应历程如图a所示(吸附在催化剂表面的物种用“*”表示)。
,其反应历程如图a所示(吸附在催化剂表面的物种用“*”表示)。
(4)工业上,可以采用CO2催化还原制备CH3OH、CH3CH2OH.发生反应如下:
①
 (主反应);
(主反应);②
 (主反应);
(主反应);③
 (副反应)。
(副反应)。一定温度下,在甲、乙体积相同的反应容器中分别充入1molCO2和3molH2,发生上述反应,其中一个容器使用水分子膜分离技术,另一个容器不使用水分子膜分离技术。实验测得CO2平衡转化率与压强关系如图b所示。其他条件相同,增大压强,CO2平衡转化率增大,其原因是
 为
为 。(写出数字表达式即可,分压=总压×物质的量分数)
。(写出数字表达式即可,分压=总压×物质的量分数)
您最近一年使用:0次
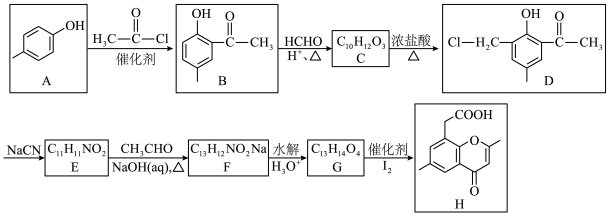
9 . 有机化合物H为某药物中间体,一种合成化合物H的路线如图。
已知:Ⅰ. (R为烃基或H原子,X为卤素原子,下同)
(R为烃基或H原子,X为卤素原子,下同)
Ⅱ.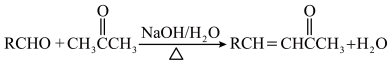
Ⅲ.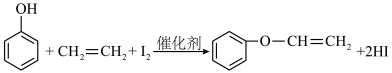
回答下列问题:
(1)A的名称为______ ,H中含氧官能团的名称为醚键、______ 。
(2)C的结构简式为______ 。
(3)E→F的化学方程式为______ 。
(4)B有多种同分异构体,其中能发生银镜反应和水解反应的芳香族化合物的同分异构体有______ 种(不考虑立体异构),核磁共振氢谱有4组峰的同分异构体的结构简式为______ 。(任写一个)
(5)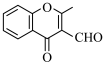 的合成路线如图(部分反应条件已略去),其中M和N的结构简式分别为
的合成路线如图(部分反应条件已略去),其中M和N的结构简式分别为______ 和______ 。
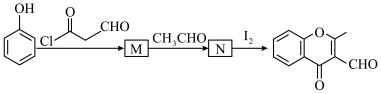

已知:Ⅰ.
 (R为烃基或H原子,X为卤素原子,下同)
(R为烃基或H原子,X为卤素原子,下同)Ⅱ.

Ⅲ.

回答下列问题:
(1)A的名称为
(2)C的结构简式为
(3)E→F的化学方程式为
(4)B有多种同分异构体,其中能发生银镜反应和水解反应的芳香族化合物的同分异构体有
(5)
 的合成路线如图(部分反应条件已略去),其中M和N的结构简式分别为
的合成路线如图(部分反应条件已略去),其中M和N的结构简式分别为
您最近一年使用:0次
10 . 从含钴余液(含 、
、 、
、 、
、 等杂质)中提取氧化钴的流程如下:
等杂质)中提取氧化钴的流程如下:
(1)在去除钙、镁时,选择适当加热条件的理由是___________ ;该步骤控制pH是影响除钙镁效果的重要因素,下图是不同pH条件下硫化钴含量和钴收率图,根据图中信息选择最适宜的pH为___________ ;___________ ;
(3)已知P507萃取剂 和
和 发生如下反应:
发生如下反应:
萃取时适当增加溶液的pH,能增大 的萃取率,原因是
的萃取率,原因是___________ ;
(4)反萃取时加入的试剂a应为___________(填代号);
(5)沉钴的离子方程式为___________ ;
(6)系列操作中如何检验 是否洗涤干净
是否洗涤干净___________ ;
(7)空气中煅烧 生成钴的某种氧化物和
生成钴的某种氧化物和 ,测得充分煅烧后剩余固体质量为24.1 g,同时获得标准状况下
,测得充分煅烧后剩余固体质量为24.1 g,同时获得标准状况下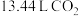 ,则钴的氧化物的化学式为
,则钴的氧化物的化学式为___________ 。
 、
、 、
、 、
、 等杂质)中提取氧化钴的流程如下:
等杂质)中提取氧化钴的流程如下: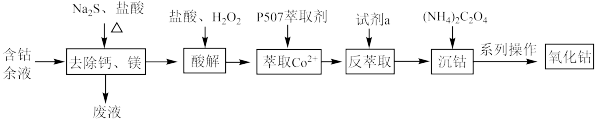
(1)在去除钙、镁时,选择适当加热条件的理由是

(3)已知P507萃取剂
 和
和 发生如下反应:
发生如下反应:
萃取时适当增加溶液的pH,能增大
 的萃取率,原因是
的萃取率,原因是(4)反萃取时加入的试剂a应为___________(填代号);
A. | B.HCl | C.NaOH | D. |
(5)沉钴的离子方程式为
(6)系列操作中如何检验
 是否洗涤干净
是否洗涤干净(7)空气中煅烧
 生成钴的某种氧化物和
生成钴的某种氧化物和 ,测得充分煅烧后剩余固体质量为24.1 g,同时获得标准状况下
,测得充分煅烧后剩余固体质量为24.1 g,同时获得标准状况下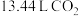 ,则钴的氧化物的化学式为
,则钴的氧化物的化学式为
您最近一年使用:0次



