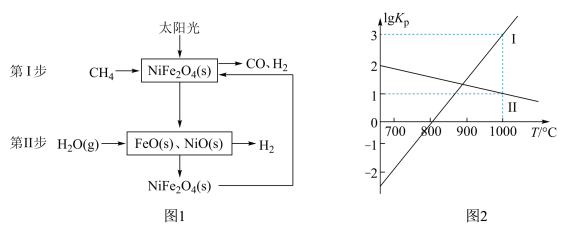
1 . 一种利用太阳能催化甲烷、水蒸气重整制氢反应原理及各步反应步骤如图1,以气体分压(单位为kPa)表示的平衡常数与温度T的变化关系如图2所示: )中铁的化合价为
)中铁的化合价为___________ 。
(2)若第Ⅰ步反应生成1mol ,吸收Q kJ热量,则第Ⅰ步反应的热化学方程式为
,吸收Q kJ热量,则第Ⅰ步反应的热化学方程式为___________ 。
(3)根据图2可知 (Ⅰ)斜率更大,受温度影响更大。则甲烷、水蒸气重整制氢反应:
(Ⅰ)斜率更大,受温度影响更大。则甲烷、水蒸气重整制氢反应: 的ΔH
的ΔH___________ 0(填“>”、“<”或“=”)。
(4)已知上述制氢过程中存在副反应: 。将
。将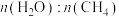
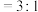 的混合气体投入温度为T的恒温恒容密闭容器中,初始压强为100kPa,若只发生甲烷、水蒸气重整反应和上述副反应,达平衡时容器内的压强为140kPa,
的混合气体投入温度为T的恒温恒容密闭容器中,初始压强为100kPa,若只发生甲烷、水蒸气重整反应和上述副反应,达平衡时容器内的压强为140kPa, 分压为10kPa,则
分压为10kPa,则 的平衡转化率为
的平衡转化率为___________ ,则甲烷、水蒸气重整反应的
___________ (列出计算式)。
(5)一定条件下,向密闭容器中加入一定量的CO、 和催化剂,发生反应:
和催化剂,发生反应: 。
。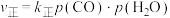 ,
,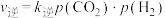 。其中
。其中 、
、 为正、逆反应速率,
为正、逆反应速率, 、
、 为正、逆速率常数,p为气体分压。已知降低温度时,
为正、逆速率常数,p为气体分压。已知降低温度时, 增大。调整CO和
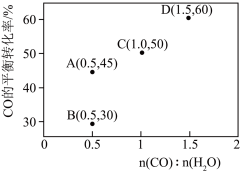
增大。调整CO和 初始投料比,测得CO的平衡转化率如下图所示,A、B、C、D四点温度由高到低的顺序是
初始投料比,测得CO的平衡转化率如下图所示,A、B、C、D四点温度由高到低的顺序是___________ ,在C点所示投料比下,当CO转化率达到40%时,
___________ 。
 )中铁的化合价为
)中铁的化合价为(2)若第Ⅰ步反应生成1mol
 ,吸收Q kJ热量,则第Ⅰ步反应的热化学方程式为
,吸收Q kJ热量,则第Ⅰ步反应的热化学方程式为(3)根据图2可知
 (Ⅰ)斜率更大,受温度影响更大。则甲烷、水蒸气重整制氢反应:
(Ⅰ)斜率更大,受温度影响更大。则甲烷、水蒸气重整制氢反应: 的ΔH
的ΔH(4)已知上述制氢过程中存在副反应:
 。将
。将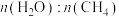
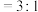 的混合气体投入温度为T的恒温恒容密闭容器中,初始压强为100kPa,若只发生甲烷、水蒸气重整反应和上述副反应,达平衡时容器内的压强为140kPa,
的混合气体投入温度为T的恒温恒容密闭容器中,初始压强为100kPa,若只发生甲烷、水蒸气重整反应和上述副反应,达平衡时容器内的压强为140kPa, 分压为10kPa,则
分压为10kPa,则 的平衡转化率为
的平衡转化率为
(5)一定条件下,向密闭容器中加入一定量的CO、
 和催化剂,发生反应:
和催化剂,发生反应: 。
。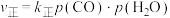 ,
,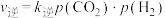 。其中
。其中 、
、 为正、逆反应速率,
为正、逆反应速率, 、
、 为正、逆速率常数,p为气体分压。已知降低温度时,
为正、逆速率常数,p为气体分压。已知降低温度时, 增大。调整CO和
增大。调整CO和 初始投料比,测得CO的平衡转化率如下图所示,A、B、C、D四点温度由高到低的顺序是
初始投料比,测得CO的平衡转化率如下图所示,A、B、C、D四点温度由高到低的顺序是
您最近一年使用:0次
名校
2 . 已知常温下水溶液中 、
、 、
、 、
、 、
、 的分布分数
的分布分数 如[如
如[如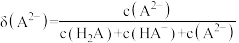 ]随
]随 变化曲线如图1所示,溶液中
变化曲线如图1所示,溶液中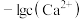 和
和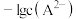 关系如图2所示,用
关系如图2所示,用 的
的 溶液滴定
溶液滴定
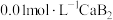 溶液,下列说法错误的是
溶液,下列说法错误的是
 、
、 、
、 、
、 、
、 的分布分数
的分布分数 如[如
如[如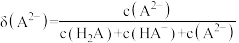 ]随
]随 变化曲线如图1所示,溶液中
变化曲线如图1所示,溶液中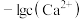 和
和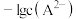 关系如图2所示,用
关系如图2所示,用 的
的 溶液滴定
溶液滴定
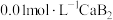 溶液,下列说法错误的是
溶液,下列说法错误的是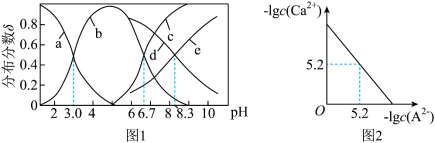
A.曲线b表示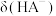 |
B. 溶液中存在: 溶液中存在: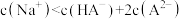 |
C.反应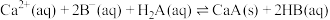 的平衡常数 的平衡常数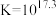 |
D.滴定过程中始终存在: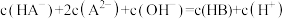 |
您最近一年使用:0次
7日内更新
|
128次组卷
|
2卷引用:2024届河南省信阳市高三下学期高考考前押题理科综合试卷-高中化学
解题方法
3 . 高分子材料PET聚酯树脂和PMMA的合成路线如下: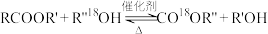 (R、R′、R″代表烃基)
(R、R′、R″代表烃基)___________ ,B的名称是___________ 。
(2)PMMA单体的官能团名称是___________ 。
(3)步骤②发生反应的化学方程式为___________ 。
(4)E的核磁共振氢谱图显示只有一组峰,步骤⑤的化学方程式为___________ 。
(5)F的结构简式为___________ 。
(6)下列说法正确的是___________(填标号)。
(7)写出符合下列条件的PMAA单体的同分异构体的结构简式:___________ 。
A.具有PMAA单体的所有官能团
B.能与新制银氨溶液反应产生银镜
C.含有3种不同化学环境的氢原子
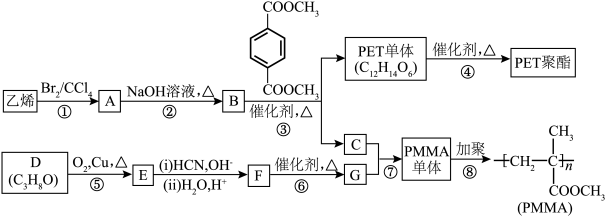
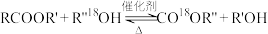 (R、R′、R″代表烃基)
(R、R′、R″代表烃基)Ⅱ、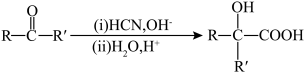 (R、R′代表烃基)
(R、R′代表烃基)
(2)PMMA单体的官能团名称是
(3)步骤②发生反应的化学方程式为
(4)E的核磁共振氢谱图显示只有一组峰,步骤⑤的化学方程式为
(5)F的结构简式为
(6)下列说法正确的是___________(填标号)。
| A.⑦为酯化反应 | B.B和C互为同系物 |
| C.D的沸点比同碳原子数的烷烃高 | D.步骤⑥的反应条件为浓硫酸、加热到140℃ |
(7)写出符合下列条件的PMAA单体的同分异构体的结构简式:
A.具有PMAA单体的所有官能团
B.能与新制银氨溶液反应产生银镜
C.含有3种不同化学环境的氢原子
您最近一年使用:0次
名校
4 . 向含有0.01 mol Cu,amol Cu2O、bmol CuO的混合物中滴加6 mol/L的稀硝酸溶液至10 mL时,固体恰好完全溶解,得到标准状况下224 mL气体(纯净物)。下列说法不正确的是
| A.反应过程中转移0.03 mol电子 | B.a∶b=1∶1 |
| C.等量上述稀硝酸中最多能溶解0.84 g Fe | D.被还原的硝酸为0.01 mol |
您最近一年使用:0次
解题方法
5 . 常温下 与
与 的反应为
的反应为 ,当加入
,当加入 时生成更难溶的Ca5(PO4)3F,氟磷比
时生成更难溶的Ca5(PO4)3F,氟磷比 为1∶10、10∶1的两种水溶液中加入过量
为1∶10、10∶1的两种水溶液中加入过量 ,平衡时
,平衡时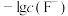 、
、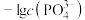 与
与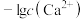 的关系如图。下列说法错误的是
的关系如图。下列说法错误的是
 与
与 的反应为
的反应为 ,当加入
,当加入 时生成更难溶的Ca5(PO4)3F,氟磷比
时生成更难溶的Ca5(PO4)3F,氟磷比 为1∶10、10∶1的两种水溶液中加入过量
为1∶10、10∶1的两种水溶液中加入过量 ,平衡时
,平衡时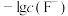 、
、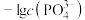 与
与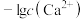 的关系如图。下列说法错误的是
的关系如图。下列说法错误的是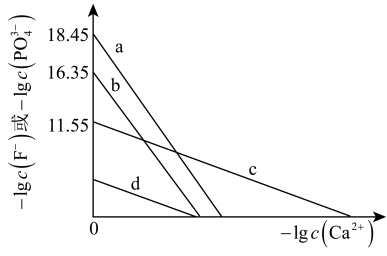
A.曲线a、b均表示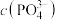 与 与 的关系,氟磷比a>b 的关系,氟磷比a>b |
B. |
C.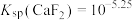 |
D.将氟磷比由10∶1提高至20∶1可有效降低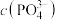 |
您最近一年使用:0次
解题方法
6 . 亚磷酸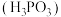 常温下电离平衡常数
常温下电离平衡常数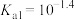 ,
, 。常温下,向
。常温下,向
 溶液中滴加
溶液中滴加 盐酸,利用电位滴定法(在化学计量点附近,指示电极电位发生突跃)得到电极电位
盐酸,利用电位滴定法(在化学计量点附近,指示电极电位发生突跃)得到电极电位 和溶液
和溶液 随盐酸体积变化曲线如下图所示。下列说法正确的是
随盐酸体积变化曲线如下图所示。下列说法正确的是
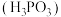 常温下电离平衡常数
常温下电离平衡常数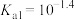 ,
, 。常温下,向
。常温下,向
 溶液中滴加
溶液中滴加 盐酸,利用电位滴定法(在化学计量点附近,指示电极电位发生突跃)得到电极电位
盐酸,利用电位滴定法(在化学计量点附近,指示电极电位发生突跃)得到电极电位 和溶液
和溶液 随盐酸体积变化曲线如下图所示。下列说法正确的是
随盐酸体积变化曲线如下图所示。下列说法正确的是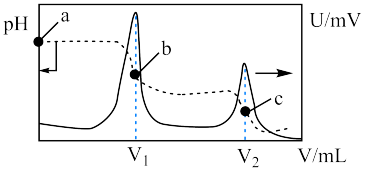
| A.滴定过程需要加入酚酞做指示剂 |
B.水的电离程度: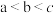 |
C. 点对应的溶液中: 点对应的溶液中: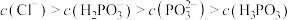 |
D. 点溶液中存在 点溶液中存在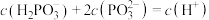 |
您最近一年使用:0次
名校
7 . 常温下,用NaOH溶液分别滴定等物质的量浓度的HX(弱酸)、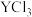 (可溶性盐)和
(可溶性盐)和 (可溶性盐)三种溶液。
(可溶性盐)三种溶液。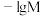 [M表示
[M表示 、
、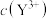 、
、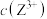 ]随溶液pH的变化如图所示。已知:
]随溶液pH的变化如图所示。已知: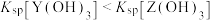 。下列说法错误的是
。下列说法错误的是
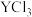 (可溶性盐)和
(可溶性盐)和 (可溶性盐)三种溶液。
(可溶性盐)三种溶液。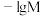 [M表示
[M表示 、
、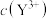 、
、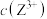 ]随溶液pH的变化如图所示。已知:
]随溶液pH的变化如图所示。已知: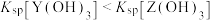 。下列说法错误的是
。下列说法错误的是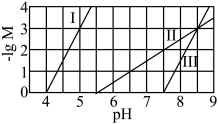
A.曲线I代表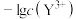 随溶液pH的变化关系 随溶液pH的变化关系 |
B. 的数量级是 的数量级是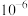 |
C. 固体能完全溶解在 固体能完全溶解在 溶液中 溶液中 |
D.滴定HX溶液至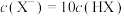 时,溶液中: 时,溶液中: |
您最近一年使用:0次
2024-06-11更新
|
130次组卷
|
2卷引用:湖南省2024届普通高中高三下学期学业水平选择性考试临考预测押题密卷化学试题(B卷)
名校
8 . 草酸常用于稀土加工分离过程,其含草酸根离子废水多用钙离子处理,研究在不同pH下草酸钙存在形态,对污水处理具有指导性意义。以下为足量草酸钙固体与水混合体系,加HCl或NaOH调节pH过程中溶质各微粒浓度 随pH变化曲线,已知:草酸钙的
随pH变化曲线,已知:草酸钙的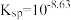 。下列说法正确的是
。下列说法正确的是
 随pH变化曲线,已知:草酸钙的
随pH变化曲线,已知:草酸钙的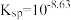 。下列说法正确的是
。下列说法正确的是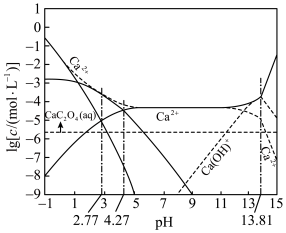
A. 的 的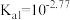 |
B.pH=2.77时,溶液中 的浓度等于 的浓度等于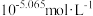 |
C.用 处理草酸根离子废水,应控制溶液pH大约在5~11区间内 处理草酸根离子废水,应控制溶液pH大约在5~11区间内 |
| D.pH=13.81以后,草酸分子浓度保持不变 |
您最近一年使用:0次
名校
解题方法
9 . 一种利用炼锌渣(主要含 、
、 、
、 、
、 和一定量的
和一定量的 、不溶性杂质)为原料制备硫化锌及高纯镓的流程如图所示:
、不溶性杂质)为原料制备硫化锌及高纯镓的流程如图所示: 。
。
(1)基态 的价层电子排布式为
的价层电子排布式为___________ ,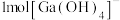 中含有
中含有 键的数目为
键的数目为___________ 。
(2)黄钠铁矾的化学式为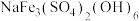 ,晶体颗粒大、易沉降。
,晶体颗粒大、易沉降。
①“沉铁”时生成黄钠铁矾的离子方程式为___________ 。
②不采用调节 的方式沉铁,可能的原因是:
的方式沉铁,可能的原因是: 容易生成
容易生成 而损失;
而损失;___________ (答2点)。
(3)“还原除杂”时先向溶液中加入一定量的铜粉,反应一段时间后再向溶液中加入稍过量 粉,加入铜粉的目的是
粉,加入铜粉的目的是___________ 。
(4) 与
与 的各物种的分布分数随
的各物种的分布分数随 的变化如图所示。“调节
的变化如图所示。“调节 ”时,
”时, 不能过高的原因是
不能过高的原因是___________ 。 。已知:室温时,
。已知:室温时,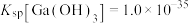 ,
,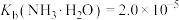 ,
,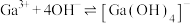
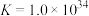 。反应
。反应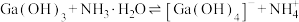 的平衡常数为
的平衡常数为___________ 。
(6)在沉铁前可以加入铁氰化钾检验 是否被完全氧化,若有
是否被完全氧化,若有 则会观察到蓝色沉淀。该蓝色沉淀是一种铁的配合物
则会观察到蓝色沉淀。该蓝色沉淀是一种铁的配合物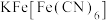 ,其晶胞的
,其晶胞的 如图[
如图[ 未标出,占据四个互不相邻的小立方体(晶胞的
未标出,占据四个互不相邻的小立方体(晶胞的 部分)的体心]。若该晶体的密度为
部分)的体心]。若该晶体的密度为 ,则1个该晶胞含
,则1个该晶胞含___________ 个 ,
,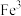 和
和 的最短距离为
的最短距离为___________  (设
(设 为阿伏加德罗常数的值,列出计算式即可)。
为阿伏加德罗常数的值,列出计算式即可)。
 、
、 、
、 、
、 和一定量的
和一定量的 、不溶性杂质)为原料制备硫化锌及高纯镓的流程如图所示:
、不溶性杂质)为原料制备硫化锌及高纯镓的流程如图所示:
 。
。(1)基态
 的价层电子排布式为
的价层电子排布式为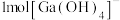 中含有
中含有 键的数目为
键的数目为(2)黄钠铁矾的化学式为
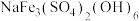 ,晶体颗粒大、易沉降。
,晶体颗粒大、易沉降。①“沉铁”时生成黄钠铁矾的离子方程式为
②不采用调节
 的方式沉铁,可能的原因是:
的方式沉铁,可能的原因是: 容易生成
容易生成 而损失;
而损失;(3)“还原除杂”时先向溶液中加入一定量的铜粉,反应一段时间后再向溶液中加入稍过量
 粉,加入铜粉的目的是
粉,加入铜粉的目的是(4)
 与
与 的各物种的分布分数随
的各物种的分布分数随 的变化如图所示。“调节
的变化如图所示。“调节 ”时,
”时, 不能过高的原因是
不能过高的原因是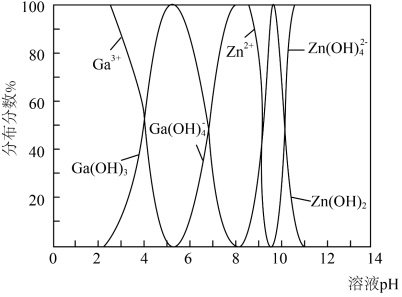
 。已知:室温时,
。已知:室温时,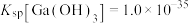 ,
,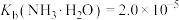 ,
,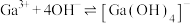
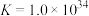 。反应
。反应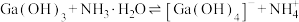 的平衡常数为
的平衡常数为(6)在沉铁前可以加入铁氰化钾检验
 是否被完全氧化,若有
是否被完全氧化,若有 则会观察到蓝色沉淀。该蓝色沉淀是一种铁的配合物
则会观察到蓝色沉淀。该蓝色沉淀是一种铁的配合物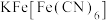 ,其晶胞的
,其晶胞的 如图[
如图[ 未标出,占据四个互不相邻的小立方体(晶胞的
未标出,占据四个互不相邻的小立方体(晶胞的 部分)的体心]。若该晶体的密度为
部分)的体心]。若该晶体的密度为 ,则1个该晶胞含
,则1个该晶胞含 ,
,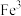 和
和 的最短距离为
的最短距离为 (设
(设 为阿伏加德罗常数的值,列出计算式即可)。
为阿伏加德罗常数的值,列出计算式即可)。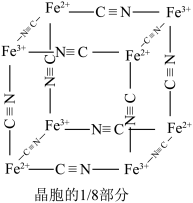
您最近一年使用:0次
名校
10 . 向mg由铁粉和铜粉组成的混合物中,加入某浓度的稀硝酸,充分反应后测得生成NO的体积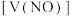 (已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有NO)。下列说法中正确的是
(已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有NO)。下列说法中正确的是
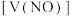 (已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有NO)。下列说法中正确的是
(已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化如图所示(设硝酸的还原产物只有NO)。下列说法中正确的是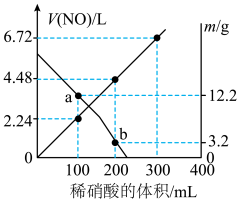
| A.a点时,100mL稀硝酸中溶解了Fe粉5.6g |
B.稀硝酸的浓度为 |
| C.加入稀硝酸的体积从300mL至400mL,期间收集产生的NO物质的量约为0.0083mol |
D.b点对应的溶液中可能含有的金属阳离子为 、 、 和 和 |
您最近一年使用:0次



