名校
解题方法
1 . 结构决定性质是元素周期律和有机化学中展现的淋漓尽致,是高中化学重要思想。
Ⅰ.一种扇形元素周期表的一部分如图所示。字母a~n表示元素周期表中的对应元素。
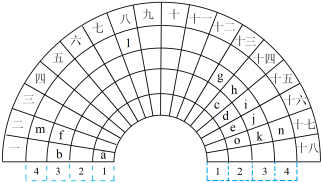
(1)元素n在元素周期表中的位置___________ 。
(2)比较f、o、k简单离子的半径,由大到小的顺序是___________ (用离子符号表示)。
(3)b与e组成的化合物中,含有非极性共价键的化合物的电子式___________ 。
(4)i的最高价氧化物对应水化物的化学式___________ ,i、d的最简单氢化物中稳定性更高的为___________ (用化学式表示)。
Ⅱ.A、B、C、D是四种常见的有机物,其中A的产量通常用来衡量一个国家的石油化工发展水平,B与C在浓硫酸和加热条件下发生反应,生成的有机物有特殊香味;A、B、C、D在一定条件下的转化关系如图所示(反应条件已省略):
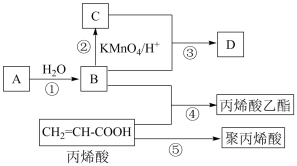
(5)A的结构简式为___________ ,C中官能团的名称为___________ 。
(6)丙烯酸乙酯的结构简式为___________ 。
(7)写出反应①化学方程式和有机反应基本类型:___________ ,___________ 反应。
(8)写出反应⑤化学方程式和有机反应基本类型:___________ ,___________ 反应。
Ⅰ.一种扇形元素周期表的一部分如图所示。字母a~n表示元素周期表中的对应元素。

(1)元素n在元素周期表中的位置
(2)比较f、o、k简单离子的半径,由大到小的顺序是
(3)b与e组成的化合物中,含有非极性共价键的化合物的电子式
(4)i的最高价氧化物对应水化物的化学式
Ⅱ.A、B、C、D是四种常见的有机物,其中A的产量通常用来衡量一个国家的石油化工发展水平,B与C在浓硫酸和加热条件下发生反应,生成的有机物有特殊香味;A、B、C、D在一定条件下的转化关系如图所示(反应条件已省略):

(5)A的结构简式为
(6)丙烯酸乙酯的结构简式为
(7)写出反应①化学方程式和有机反应基本类型:
(8)写出反应⑤化学方程式和有机反应基本类型:
您最近一年使用:0次
2 . 氮及其化合物在工农业生产、生活中被广泛使用,造福人类。
I.元素 X、Y、Z 位于同一周期且原子序数依次增大,它们和氢元素、硫元素组成的含氮化合物(结构如图)常用作丝绸漂白剂。回答下列问题:
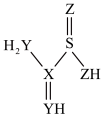
(1)硫元素在元素周期表中的位置为______ ;Y 的元素符号为______ 。
(2)下列说法错误的是______ (选填序号)。
A.原子半径:X>Y>Z
B.简单气态氢化物稳定性:Y<Z
C.该化合物可溶于水
D.该化合物中所有原子均为 8 电子稳定结构
II.工业上用氨气来制造硝酸,NH3转化关系如图所示。
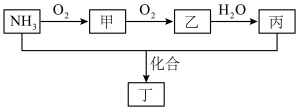
(3)NH3的电子式为______ 。
(4)图中,乙转化为丙的离子方程式为______ 。
(5)检验化合物丁中阳离子的方法:取少量待测液于试管中,______ ,将湿润的 红色石蕊试纸置于试管口,试纸变蓝。
(6)工业上常使用 NH3处理甲,生成无污染的 N2,则 NH3与甲完全反应的物质的量之比为______ 。
I.元素 X、Y、Z 位于同一周期且原子序数依次增大,它们和氢元素、硫元素组成的含氮化合物(结构如图)常用作丝绸漂白剂。回答下列问题:

(1)硫元素在元素周期表中的位置为
(2)下列说法错误的是
A.原子半径:X>Y>Z
B.简单气态氢化物稳定性:Y<Z
C.该化合物可溶于水
D.该化合物中所有原子均为 8 电子稳定结构
II.工业上用氨气来制造硝酸,NH3转化关系如图所示。

(3)NH3的电子式为
(4)图中,乙转化为丙的离子方程式为
(5)检验化合物丁中阳离子的方法:取少量待测液于试管中,
(6)工业上常使用 NH3处理甲,生成无污染的 N2,则 NH3与甲完全反应的物质的量之比为
您最近一年使用:0次
名校
解题方法
3 . A、B、C、X是中学化学常见化合物或单质,均由短周期元素组成,转化关系如图。请据图回答下列问题:

(1)若A、B、C中均含同一种常见金属元素R,R在C中以阴离子形式存在,B为白色胶状沉淀。
①R在元素周期表中的位置为______________ 。
②若A的溶液中混有Fe3+,当向该混合液中加入氨水,生成R(OH)n及Fe(OH)3共沉淀时,溶液中c(Fe3+)/ c(Rn+)=____ 。[已知:Fe(OH)3的 Ksp=4.00×10-38,沉淀B的Ksp=1.32×10-33 ]
(2)若A、B、C的焰色反应均为黄色,水溶液均呈碱性。
①A中含有的化学键是________________________ 。
②将672 mL(标准状况下)X通入100 mL 0.4mol·L- 1 A的溶液后,溶液中离子浓度由大到小的顺序为_______________________ 。
③自然界中存在B、C和H2O按一定比例形成的固体。取一定量该固体制成100mL溶液,测得溶液中金属阳离子的浓度为0.5mol·L-1。若取相同质量的固体加热至恒重,剩余固体的质量为_______ 。
(3)若A、B、C中均含同一种常见非金属元素,其中A为黑色固体单质。已知298K下,1mol A、1 mol B完全燃烧生成稳定氧化物放出的热量分别为393.5 kJ,283 kJ。写出该温度下A与C反应生成B的热化学方程式:______________________ 。

(1)若A、B、C中均含同一种常见金属元素R,R在C中以阴离子形式存在,B为白色胶状沉淀。
①R在元素周期表中的位置为
②若A的溶液中混有Fe3+,当向该混合液中加入氨水,生成R(OH)n及Fe(OH)3共沉淀时,溶液中c(Fe3+)/ c(Rn+)=
(2)若A、B、C的焰色反应均为黄色,水溶液均呈碱性。
①A中含有的化学键是
②将672 mL(标准状况下)X通入100 mL 0.4mol·L- 1 A的溶液后,溶液中离子浓度由大到小的顺序为
③自然界中存在B、C和H2O按一定比例形成的固体。取一定量该固体制成100mL溶液,测得溶液中金属阳离子的浓度为0.5mol·L-1。若取相同质量的固体加热至恒重,剩余固体的质量为
(3)若A、B、C中均含同一种常见非金属元素,其中A为黑色固体单质。已知298K下,1mol A、1 mol B完全燃烧生成稳定氧化物放出的热量分别为393.5 kJ,283 kJ。写出该温度下A与C反应生成B的热化学方程式:
您最近一年使用:0次
解题方法
4 . 已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合下图(反应条件省略)

(1)若甲为气态非金属单质,丙能与人体血液中的血红蛋白结合而使人中毒,则乙的电子式为_______________ 。
(2)若甲为黄绿色气体,X为常见的金属,则X在元素周期表中的位置是_________ ,丙的水溶液呈___ (填酸性、碱性或中性),原因是:______________ (用离子方程式表示)。含amol乙的溶液溶解了一定量X后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的乙的物质的量是________ mol。
(3)若X为酸性氧化物且具有漂白性,甲溶液的焰色反应呈黄色,则标准状况下8.96 L 气体X与2 L 0.25 mol/L的甲溶液反应生成的溶液中乙和丙的物质的量浓度之比为(不考虑离子的水解)___________ 。另有和丙具有相同元素组成的物质丁,丙和丁能反应生成气体,写出该反应的离子方程式______________________ 。
(4)若X为强碱溶液,乙为白色胶状沉淀,则甲与丙反应的离子方程式为____________ 。

(1)若甲为气态非金属单质,丙能与人体血液中的血红蛋白结合而使人中毒,则乙的电子式为
(2)若甲为黄绿色气体,X为常见的金属,则X在元素周期表中的位置是
(3)若X为酸性氧化物且具有漂白性,甲溶液的焰色反应呈黄色,则标准状况下8.96 L 气体X与2 L 0.25 mol/L的甲溶液反应生成的溶液中乙和丙的物质的量浓度之比为(不考虑离子的水解)
(4)若X为强碱溶液,乙为白色胶状沉淀,则甲与丙反应的离子方程式为
您最近一年使用:0次
5 . 甲、乙、丙三种物质均由短周期元素组成,一定条件下,存在下列转化关系:甲+乙→丙+H20
(1)若丙为Na2C03,反应的化学方程式为______ (任写一个)。
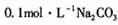 溶液中,所含的离子按物质的量浓度由大到小的顺序排列为
溶液中,所含的离子按物质的量浓度由大到小的顺序排列为______ 。
(2)若甲是石油裂解气的主要成分之一,乙为O2,且甲分子和乙分子具有相同的电子数。25℃、101 kPa时,1g甲完全燃烧生成CO2气体与液态水,放出50.5 kJ的热量,该反应的热化学方程式为_________ ;利用该反应设计的燃料电池中,通入甲的电极为电池的_____ (填“正极”或“负极”)。
(3)若甲、乙是同主族元素的化合物,丙为单质。
①丙所含元素在元素周期表中的位置为_______ ;
②甲与水相比,热稳定性较强的是________ (填化学式)。
(1)若丙为Na2C03,反应的化学方程式为
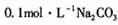 溶液中,所含的离子按物质的量浓度由大到小的顺序排列为
溶液中,所含的离子按物质的量浓度由大到小的顺序排列为(2)若甲是石油裂解气的主要成分之一,乙为O2,且甲分子和乙分子具有相同的电子数。25℃、101 kPa时,1g甲完全燃烧生成CO2气体与液态水,放出50.5 kJ的热量,该反应的热化学方程式为
(3)若甲、乙是同主族元素的化合物,丙为单质。
①丙所含元素在元素周期表中的位置为
②甲与水相比,热稳定性较强的是
您最近一年使用:0次
2016-12-09更新
|
304次组卷
|
3卷引用:2015届福建省普通高中高三4月质量检查理综化学试卷
6 . 镓是一种低熔点、高沸点的稀有金属,有“电子工业脊梁”的美誉,被广泛应用到光电子工业和微波通信工业。回答下列问题:
(1)镓 的原子结构示意图为
的原子结构示意图为 ,镓元素在元素周期表中的位置是
,镓元素在元素周期表中的位置是_______ 。
(2) 的熔点为1238℃,且熔融状态不导电,据此判断,该化合物是
的熔点为1238℃,且熔融状态不导电,据此判断,该化合物是_______ (填“共价化合物”或“离子化合物”)。
(3)已知 与
与 同周期,
同周期, 与N同主族。
与N同主族。
①用原子结构理论推测, 中
中 元素的化合价为
元素的化合价为_______ ;
②下列事实不能用元素周期律解释的是_______ (填标序号);
a.原子半径: b.热稳定性:
b.热稳定性: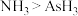
c.碱性: d.酸性:
d.酸性: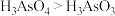
(4) 是一种直接能隙的半导体,自1990年起常用在发光二极管中。一种镍催化法生产
是一种直接能隙的半导体,自1990年起常用在发光二极管中。一种镍催化法生产 的工艺如图。
的工艺如图。_______ 。
(1)镓
 的原子结构示意图为
的原子结构示意图为 ,镓元素在元素周期表中的位置是
,镓元素在元素周期表中的位置是(2)
 的熔点为1238℃,且熔融状态不导电,据此判断,该化合物是
的熔点为1238℃,且熔融状态不导电,据此判断,该化合物是(3)已知
 与
与 同周期,
同周期, 与N同主族。
与N同主族。①用原子结构理论推测,
 中
中 元素的化合价为
元素的化合价为②下列事实不能用元素周期律解释的是
a.原子半径:
 b.热稳定性:
b.热稳定性: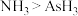
c.碱性:
 d.酸性:
d.酸性: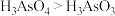
(4)
 是一种直接能隙的半导体,自1990年起常用在发光二极管中。一种镍催化法生产
是一种直接能隙的半导体,自1990年起常用在发光二极管中。一种镍催化法生产 的工艺如图。
的工艺如图。
①“热转化”时 转化为
转化为
 化学方程式是
化学方程式是
您最近一年使用:0次
名校
7 . W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,且四种元素的原子最外层电子数之和为24。以上元素都是工业生产中的常见元素,工业生产中常会产生废气、废水需要无害化处理后再排放。
推进含W元素物质转化的研究对改善人类的生存环境具有重要意义。W元素的固定指的是游离态的W转化为化合态的W,一种新型人工合成固定W元素的原理如图。
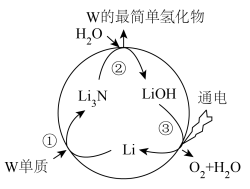
下列说法正确的是:
| W | X | |
| Y | Z |

下列说法正确的是:
| A.该转化过程①②③反应均为氧化还原反应 |
B.假设每一步均完全转化,每生成 ,同时生成 ,同时生成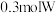 的最简单氢化物 的最简单氢化物 |
C. 的碱性在同主族元素的最高价氧化物的水化物中碱性最弱 的碱性在同主族元素的最高价氧化物的水化物中碱性最弱 |
| D.该过程的总反应中W的单质置换出氧气,说明W的非金属性比氧强 |
您最近一年使用:0次
名校
解题方法
8 . 已知A、B、C、D、E、F为原子序数依次增大的前36号元素,A的一种同位素原子无中子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D的基态原子2p轨道中含有两种不同自旋方向的电子,且电子数之比为3:1;E为短周期中电负性最小的元素;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。含有Y元素的某种钙盐是漂白粉的有效成分。Z元素正三价阳离子的3d轨道为半充满状态。用于回答下列问题(用元素符号或化学式表示):
(1)F在元素周期表中位置为___________ 区。基态原子与F元素同周期且最外层电子数相等元素还有___________ (填元素符号)。元素Z与F的第二电离能 的原因是
的原因是___________ 。
(2)D和E可形成一种既含有共价键又含有离子键的化合物,该化合物的电子式为___________ 。
(3)比较B、C、D最简单气态氢化物的稳定性大到小顺序为:___________ (用分子式表示)。
(4) 分子可与
分子可与 离子结合成
离子结合成 离子,这个过程中发生改变是
离子,这个过程中发生改变是___________ 。(填字母)。
a.微粒的空间构型 b.C原子的杂化类型
c.A-C-A的键角 d.微粒的电子数
(5)某F与Y形成的化合物的晶胞如图所示(黑点代表F原子)。___________ 。
②已知该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体中F原子和Y原子之间的最短距离为
,则该晶体中F原子和Y原子之间的最短距离为___________ cm(只写计算式)(F原子位于体对角线上)。
(6)E的一种晶体如图甲、乙所示,若按甲虚线方向切乙得到的截面图是___________(填字母)。
(1)F在元素周期表中位置为
 的原因是
的原因是(2)D和E可形成一种既含有共价键又含有离子键的化合物,该化合物的电子式为
(3)比较B、C、D最简单气态氢化物的稳定性大到小顺序为:
(4)
 分子可与
分子可与 离子结合成
离子结合成 离子,这个过程中发生改变是
离子,这个过程中发生改变是a.微粒的空间构型 b.C原子的杂化类型
c.A-C-A的键角 d.微粒的电子数
(5)某F与Y形成的化合物的晶胞如图所示(黑点代表F原子)。

②已知该晶体的密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体中F原子和Y原子之间的最短距离为
,则该晶体中F原子和Y原子之间的最短距离为(6)E的一种晶体如图甲、乙所示,若按甲虚线方向切乙得到的截面图是___________(填字母)。

A.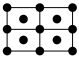 | B.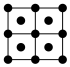 | C.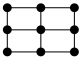 | D. |
您最近一年使用:0次
名校
解题方法
9 . A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,相关信息如下表:
请用化学用语填空:
(1)A元素在元素周期表中的位置___________ ;C元素和F元素的电负性比较,较小的是___________ (填元素符号)。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的电子式为___________ ,B元素所形成的单质分子中σ键与π键数目之比为___________ 。
(3)F元素原子的价电子的轨道表示式是___________ ;G的高价阳离子的溶液与H单质反应的离子方程式为___________ ;元素X与元素E在周期表中呈对角线关系,且元素X的最高价氧化物的水化物也具有两性,试写出X元素的最高价氧化物的水化物与D元素的最高价氧化物的水化物反应的化学方程式___________ 。
| 元素 | 元素相关信息 |
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为 |
| F | 基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反 |
| G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
| H | 是我国使用最早的合金中的最主要元素 |
(1)A元素在元素周期表中的位置
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的电子式为
(3)F元素原子的价电子的轨道表示式是
您最近一年使用:0次
10 . Ⅰ.我国科学家在铁基高温超导体的研究上取得重大突破,发现了该超导体是由Fe、Ba、As三种元素组成,这为进一步理解超导配对机理及其与电荷密度波的关系提供了重要实验证据。回答下列问题:
(1)As元素属于元素周期表的________ 区元素,其价电子排布式是________ 。
(2)基态Fe原子核外电子排布式为________ 。 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为________ 。
Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有________ 种。
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的________ 区(用符号填空),原子序数最大的在周期表位置________ 。
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为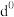 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
________ (填“无”或“有”)颜色。
(1)As元素属于元素周期表的
(2)基态Fe原子核外电子排布式为
 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为
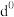 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
您最近一年使用:0次



