1 . 常温下,下列各组离子在给定溶液中能大量共存的是
A.使蓝色石蕊试纸变红的溶液中: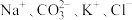 |
B.在 氯化亚铁溶液中: 氯化亚铁溶液中: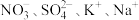 |
C.麦芽糖溶液中: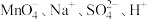 |
D.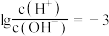 的溶液中: 的溶液中: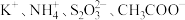 |
您最近一年使用:0次
7日内更新
|
118次组卷
|
3卷引用:第03讲 离子共存、离子的检验与推断(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
(已下线)第03讲 离子共存、离子的检验与推断(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)黑龙江省部分学校2024届高三下学期第三次模拟化学试题 黑龙江省双鸭山市友谊县高级中学2023-2024学年高三下学期第三次模拟考试化学试题
2 . 下列由离子检验有关的实验得出的结论正确的是
选项 | 实验 | 结论 |
A | 溶液X的焰色试验呈黄色 | 溶液X中一定有 ,一定没有 ,一定没有 |
B | 取少量溶液Y于试管中,滴加 溶液后,再滴加 溶液后,再滴加 溶液,溶液变为红色 溶液,溶液变为红色 | 溶液Y中一定有 ,一定没有 ,一定没有 |
C | 取少量溶液Z,向其中加入少量盐酸酸化的 溶液,有白色沉淀产生、无气体生成 溶液,有白色沉淀产生、无气体生成 | 溶液Z中一定有 ,一定没有 ,一定没有 |
D | 取少量溶液W,加入少量淀粉,无明显现象,向其中加入新制氯水,溶液变蓝 | 溶液W中一定有 ,一定没有 ,一定没有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 下列各组离子在对应的溶液中能大量共存的是
A.0.1mol·L-1 K3[Fe(CN)6]溶液中: 、 、 、 、 、 、 |
B.0.1mol·L-1 HNO3溶液中: 、 、 、 、 、 、 |
C.0.1mol·L-1氨水中: 、 、 、 、 、 、 |
D.0.1mol·L-1 Ba(OH)2溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2025高三·全国·专题练习
解题方法
4 .  有较强的配位能力,许多金属离子都可以与
有较强的配位能力,许多金属离子都可以与 形成稳定的配合。反应
形成稳定的配合。反应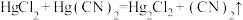 用于制备
用于制备 。
。
(1)上述反应的氧化剂是___________ 。
(2)写出 的结构简式
的结构简式___________ , 的空间构型是
的空间构型是___________ ;1mol 分子中
分子中 键为
键为___________ mol。
(3) 被称为拟卤素,性质与卤素相似,写出
被称为拟卤素,性质与卤素相似,写出 与氢氧化钠溶液反应的离子方程式
与氢氧化钠溶液反应的离子方程式___________ 。
(4)基态N价层电子排布式为___________ 。
 有较强的配位能力,许多金属离子都可以与
有较强的配位能力,许多金属离子都可以与 形成稳定的配合。反应
形成稳定的配合。反应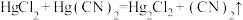 用于制备
用于制备 。
。(1)上述反应的氧化剂是
(2)写出
 的结构简式
的结构简式 的空间构型是
的空间构型是 分子中
分子中 键为
键为(3)
 被称为拟卤素,性质与卤素相似,写出
被称为拟卤素,性质与卤素相似,写出 与氢氧化钠溶液反应的离子方程式
与氢氧化钠溶液反应的离子方程式(4)基态N价层电子排布式为
您最近一年使用:0次
2025高三上·全国·专题练习
解题方法
5 . 现有硫酸钠溶液V mL,它的密度是ρ g· mL-1,其中钠离子的质量分数是a%,则下列有关该溶液的说法错误 的是。
A.溶质的质量分数是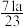 % % |
B.溶液的物质的量浓度是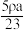 mol·L-1 mol·L-1 |
| C.溶质和溶剂的物质的量之比是9a∶(2300-71a) |
D.硫酸根离子的质量分数是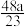 |
您最近一年使用:0次
2025高三上·全国·专题练习
解题方法
6 . 质量、物质的量、物质的量浓度等是用于化学计算的常见物理量。
(1)质量之比为16:7:6的三种气体SO2、CO、NO。分子个数之比为___________ ;氧原子个数之比为___________ ;相同条件下的体积之比为___________ 。
(2)标准状况下,17g NH3的体积为___________ ,含有氢原子个数为___________ ,它与标准状况下___________ L H2S含有相同数目的氢原子。
(3)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为___________ ,R的相对原子质量为___________ 。
(4)同温同压下,A2气体与B2气体等体积化合,生成AxBy气体,已知反应前后气体的密度不变,则AxBy的分子式为___________ 。
(5)在t℃时将a g NH3 完全溶于水得到V mL溶液,该溶液的密度为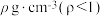 ;质量分数为w,物质的量浓度为c mol·L-1。下列计算结果正确的是___________。
;质量分数为w,物质的量浓度为c mol·L-1。下列计算结果正确的是___________。
(6)将a L Al2(SO4)3和(NH4)2SO4的混合溶液分成两等份,一份加入b mol BaCl2溶液使溶液中的SO 刚好完全沉定,另一份加入足量NaOH溶液并加热可得到c molNH3,则原溶液中Al3+的物质的量浓度为
刚好完全沉定,另一份加入足量NaOH溶液并加热可得到c molNH3,则原溶液中Al3+的物质的量浓度为___________ 。
(7)将0.24g Mg和0.27g Al的混合物投入到100mL 1mol/L的盐酸中,充分反应后固体完全溶解。向所得溶液中加入2mol/L的NaOH溶液,恰好使金属离子全部沉淀完全,需要NaOH溶液的体积为___________ mL。
(1)质量之比为16:7:6的三种气体SO2、CO、NO。分子个数之比为
(2)标准状况下,17g NH3的体积为
(3)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
(4)同温同压下,A2气体与B2气体等体积化合,生成AxBy气体,已知反应前后气体的密度不变,则AxBy的分子式为
(5)在t℃时将a g NH3 完全溶于水得到V mL溶液,该溶液的密度为
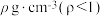 ;质量分数为w,物质的量浓度为c mol·L-1。下列计算结果正确的是___________。
;质量分数为w,物质的量浓度为c mol·L-1。下列计算结果正确的是___________。A.溶质的质量分数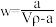 |
B.溶质的物质的量浓度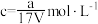 |
C.溶液密度ρ可表示为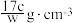 |
| D.上述溶液中再加入V mL水,所得溶液溶质的质量分数小于0.5w |
 刚好完全沉定,另一份加入足量NaOH溶液并加热可得到c molNH3,则原溶液中Al3+的物质的量浓度为
刚好完全沉定,另一份加入足量NaOH溶液并加热可得到c molNH3,则原溶液中Al3+的物质的量浓度为(7)将0.24g Mg和0.27g Al的混合物投入到100mL 1mol/L的盐酸中,充分反应后固体完全溶解。向所得溶液中加入2mol/L的NaOH溶液,恰好使金属离子全部沉淀完全,需要NaOH溶液的体积为
您最近一年使用:0次
2025高三·全国·专题练习
7 . 回答下列问题。
(1)某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数的值。
①该氯原子的相对原子质量为___________ ;
②该氯原子的摩尔质量是___________ ;
③m g该氯原子的物质的量为___________ ;
④n g该氯原子所含的电子数为___________ 。
(2)12.4 g Na2R含Na+ 0.4 mol,则Na2R的摩尔质量为___________ ,R的相对原子质量为___________ 。含R的质量为1.6 g的Na2R,其物质的量为___________ 。
(1)某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数的值。
①该氯原子的相对原子质量为
②该氯原子的摩尔质量是
③m g该氯原子的物质的量为
④n g该氯原子所含的电子数为
(2)12.4 g Na2R含Na+ 0.4 mol,则Na2R的摩尔质量为
您最近一年使用:0次
解题方法
8 . 下列有关实验的离子方程式正确的是
A.将少量 加入蒸馏水中: 加入蒸馏水中: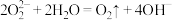 |
B.将铁粉加入足量稀硫酸中: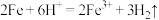 |
C.将 加入过量氢碘酸中: 加入过量氢碘酸中: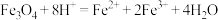 |
D.将少量 溶液加入 溶液加入 溶液中: 溶液中: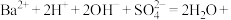 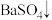 |
您最近一年使用:0次
名校
解题方法
9 . 电解质在水溶液中的反应属于离子反应。下列离子方程式正确的是
A.浓盐酸与 反应制取少量氯气: 反应制取少量氯气: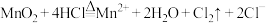 |
B. 溶液中加入过量的 溶液中加入过量的 溶液: 溶液: |
C.1L0.1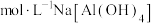 溶液中通入0.28molHCl气体: 溶液中通入0.28molHCl气体: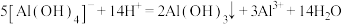 |
D. 通入 通入 溶液中至 溶液中至 恰好完全反应: 恰好完全反应: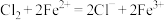 |
您最近一年使用:0次
2025高三上·全国·专题练习
10 . 一块表面已被氧化为氧化钠的钠块17.0 g,投入50 g水中,最多能产生0.2 g气体,则:
(1)涉及的化学方程式为_______ ,_______ 。
(2)钠块中钠的质量是_______ g。
(3)钠块中氧化钠的质量是_______ g。
(4)原来钠块中被氧化的钠的质量是_______ g。
(5)设所得溶液的体积为50 mL,求所得溶液溶质物质的量浓度是_______ 。
(1)涉及的化学方程式为
(2)钠块中钠的质量是
(3)钠块中氧化钠的质量是
(4)原来钠块中被氧化的钠的质量是
(5)设所得溶液的体积为50 mL,求所得溶液溶质物质的量浓度是
您最近一年使用:0次



