名校
解题方法
1 . 立德粉(主要成分为BaSO4 ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示:
ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示:___________ 。
(2)加入H2O2发生反应的离子方程式为___________ 。
(3)分离出Fe(OH)3的实验操作名称为___________ 。
(4)“除杂Ⅱ”中加入过量的锌粉主要除去___________ (填离子符号),该反应的反应类型为___________ 。
(5)“滤渣”的成分是___________ 。
(6)8.34 g绿矾(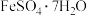 )晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示:
)晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示: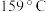 时固体N的化学式为
时固体N的化学式为___________ ,取适量  时所得的样品P,隔绝空气加热至
时所得的样品P,隔绝空气加热至 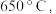 得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式
得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式___________ 。
 ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示:
ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示: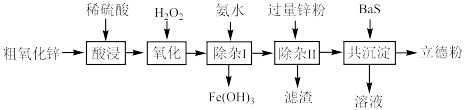
(2)加入H2O2发生反应的离子方程式为
(3)分离出Fe(OH)3的实验操作名称为
(4)“除杂Ⅱ”中加入过量的锌粉主要除去
(5)“滤渣”的成分是
(6)8.34 g绿矾(
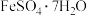 )晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示:
)晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示: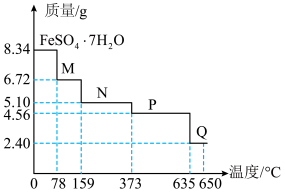
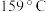 时固体N的化学式为
时固体N的化学式为 时所得的样品P,隔绝空气加热至
时所得的样品P,隔绝空气加热至 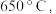 得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式
得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式
您最近一年使用:0次
2024-05-22更新
|
345次组卷
|
2卷引用:安徽省淮北市龙兴中学2023-2024学年高一上学期期末化学试卷
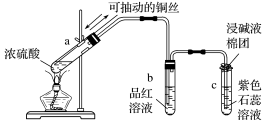
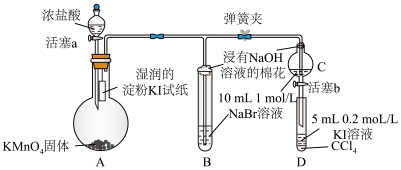
2 . 为验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
实验过程:
 . 打开弹簧夹,打开活塞a,滴加浓盐酸。
. 打开弹簧夹,打开活塞a,滴加浓盐酸。
 . 当B和C中的溶液都变为黄色时,夹紧弹簧夹。
. 当B和C中的溶液都变为黄色时,夹紧弹簧夹。
 . 当B中溶液由黄色变为棕色时,关闭活塞a。
. 当B中溶液由黄色变为棕色时,关闭活塞a。
 .…
.…
(1)写出A中发生反应的离子方程式___________ 。
(2)验证氯气的氧化性强于碘的实验现象是___________ 。
(3)B中溶液发生反应的离子方程式是___________ 。
(4)为验证溴的氧化性强于碘,过程 的操作和现象是
的操作和现象是___________ 。
(5)过程 实验的目的是
实验的目的是___________ 。
(6)ClO2常温下为易溶于水且不与水反应的气体,水溶液呈深黄绿色,11℃时液化成红棕色液体。以 和HCl的乙醇溶液为原料制取ClO2的反应为
和HCl的乙醇溶液为原料制取ClO2的反应为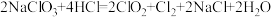 制取装置如图所示。
制取装置如图所示。___________ ,烧杯中混合液用于吸收产生的Cl2同时生成KIO3,反应的离子方程式为___________ 。
实验过程:
 . 打开弹簧夹,打开活塞a,滴加浓盐酸。
. 打开弹簧夹,打开活塞a,滴加浓盐酸。 . 当B和C中的溶液都变为黄色时,夹紧弹簧夹。
. 当B和C中的溶液都变为黄色时,夹紧弹簧夹。 . 当B中溶液由黄色变为棕色时,关闭活塞a。
. 当B中溶液由黄色变为棕色时,关闭活塞a。 .…
.…(1)写出A中发生反应的离子方程式
(2)验证氯气的氧化性强于碘的实验现象是
(3)B中溶液发生反应的离子方程式是
(4)为验证溴的氧化性强于碘,过程
 的操作和现象是
的操作和现象是(5)过程
 实验的目的是
实验的目的是(6)ClO2常温下为易溶于水且不与水反应的气体,水溶液呈深黄绿色,11℃时液化成红棕色液体。以
 和HCl的乙醇溶液为原料制取ClO2的反应为
和HCl的乙醇溶液为原料制取ClO2的反应为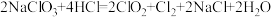 制取装置如图所示。
制取装置如图所示。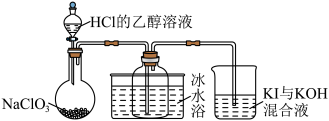
您最近一年使用:0次
解题方法
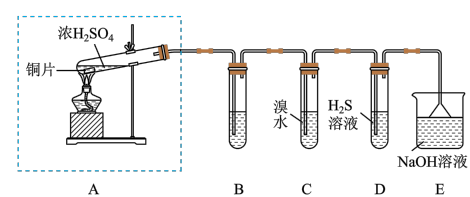
3 . 某实验小组同学欲探究SO2的性质。他们设计了如图所示的实验装置,请你参与探究,并回答问题。___________ 。 浓硫酸表现___________ (填化学性质)。
(2)装置B用于检验SO2的漂白性,其中所盛试剂为___________ 。装置D用于检验SO2的,写出反应方程式___________ 。
(3)若将装置C中的溶液换成氯水,则发生反应的离子方程式为___________ 。
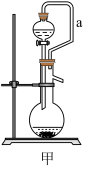
(4)如果用硫酸溶液和Na2SO3固体反应制备SO2,装置如图甲所示。其中a导管的作用是___________ ,所用硫酸溶液为70%浓硫酸,不用稀硫酸的原因是___________ 。
(2)装置B用于检验SO2的漂白性,其中所盛试剂为
(3)若将装置C中的溶液换成氯水,则发生反应的离子方程式为
(4)如果用硫酸溶液和Na2SO3固体反应制备SO2,装置如图甲所示。其中a导管的作用是
您最近一年使用:0次
解题方法
4 . 常温下某学生用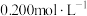 的标准
的标准 溶液滴定未知浓度的醋酸,其操作可分为如下几步:
溶液滴定未知浓度的醋酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入 溶液至“0”刻度线以上
溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线以下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴指示剂
⑤用标准液滴定至终点,记下滴定管液面读数
(1)以上步骤有错误的是_______ (填序号)。
(2)用标准 溶液滴定时,应将标准
溶液滴定时,应将标准 溶液注入
溶液注入_______ 中(从图中选填“甲”或“乙”)。_______ 作指示剂,判断达到滴定终点的依据是_______ 。
(4)第一次滴定前后,碱式滴定管中的液面位置如图所示,则 标准溶液的实际用量为
标准溶液的实际用量为_______ mL。_______ ;滴定结束后读数时俯视液面_______ 。
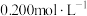 的标准
的标准 溶液滴定未知浓度的醋酸,其操作可分为如下几步:
溶液滴定未知浓度的醋酸,其操作可分为如下几步:①用蒸馏水洗涤碱式滴定管,并注入
 溶液至“0”刻度线以上
溶液至“0”刻度线以上②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线以下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴指示剂
⑤用标准液滴定至终点,记下滴定管液面读数
(1)以上步骤有错误的是
(2)用标准
 溶液滴定时,应将标准
溶液滴定时,应将标准 溶液注入
溶液注入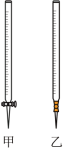
(4)第一次滴定前后,碱式滴定管中的液面位置如图所示,则
 标准溶液的实际用量为
标准溶液的实际用量为
您最近一年使用:0次
解题方法
5 . 实验活动探究---食盐的精制
实验目的:从粗食盐水中除去
实验用品:
试剂:粗食盐水,稀盐酸,稀硫酸, 溶液,
溶液, 溶液,
溶液, 溶液,
溶液, 溶液
溶液
仪器:烧杯,漏斗,玻璃棒,表面皿, 试纸,滤纸,试管,胶头滴管,铁架台(带铁圈)
试纸,滤纸,试管,胶头滴管,铁架台(带铁圈)
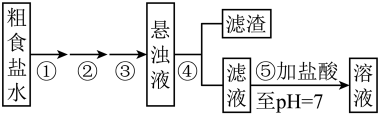
实验操作流程: 离子,需加入过量的
离子,需加入过量的_______ ,写出①中反应的离子方程式_______ 。
(2)操作②加入过量的____ ,写出②中反应的离子方程式___ ;操作③加入过量的 溶液,除了除去
溶液,除了除去 ,还要除去操作①引入的杂质离子
,还要除去操作①引入的杂质离子______ 。
(3)操作④为_______ ,其中玻璃棒的作用是_______ 。
(4)操作⑤向滤液中滴加盐酸,用玻璃棒搅拌,直到_______ ,并用 试纸检验,使滤液呈中性或微酸性。
试纸检验,使滤液呈中性或微酸性。
(5)操作流程④与⑤可以颠倒顺序吗?_______ ,为什么?_______ 。
实验目的:从粗食盐水中除去

实验用品:
试剂:粗食盐水,稀盐酸,稀硫酸,
 溶液,
溶液, 溶液,
溶液, 溶液,
溶液, 溶液
溶液仪器:烧杯,漏斗,玻璃棒,表面皿,
 试纸,滤纸,试管,胶头滴管,铁架台(带铁圈)
试纸,滤纸,试管,胶头滴管,铁架台(带铁圈)实验操作流程:
 离子,需加入过量的
离子,需加入过量的(2)操作②加入过量的
 溶液,除了除去
溶液,除了除去 ,还要除去操作①引入的杂质离子
,还要除去操作①引入的杂质离子(3)操作④为
(4)操作⑤向滤液中滴加盐酸,用玻璃棒搅拌,直到
 试纸检验,使滤液呈中性或微酸性。
试纸检验,使滤液呈中性或微酸性。(5)操作流程④与⑤可以颠倒顺序吗?
您最近一年使用:0次
6 . 健康人体内含铁元素大约 ,人体内铁元素以
,人体内铁元素以 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验:_______ ,试剂2的化学式为_______ 。
(2)加入新制氯水,溶液中发生的氧化还原反应的离子方程式是_______ 。
(3)加入试剂2时溶液为淡红色,说明“速力菲”中的 已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有_______ 性。
(4)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:_______ ,现象为_______ 。
 ,人体内铁元素以
,人体内铁元素以 和
和 的形式存在,
的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
易被吸收,所以给贫血者补充铁元素时,应补充亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如下实验:
的存在,设计并进行了如下实验: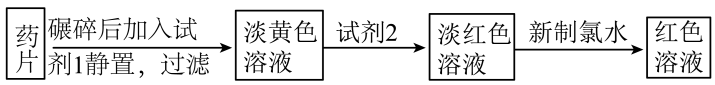
(2)加入新制氯水,溶液中发生的氧化还原反应的离子方程式是
(3)加入试剂2时溶液为淡红色,说明“速力菲”中的
 已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已部分被氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有(4)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:
您最近一年使用:0次
7 . 浓硫酸的特性吸水性、脱水性、强氧化性。
(1)吸水性与脱水性
①吸水性:浓硫酸能够吸收气体、液体中的水分子及固体中的结晶水,故常用作_______ 。
②脱水性____ 固体,并放出有_____ 气味的气体。
(2)强氧化性
(1)吸水性与脱水性
①吸水性:浓硫酸能够吸收气体、液体中的水分子及固体中的结晶水,故常用作
②脱水性
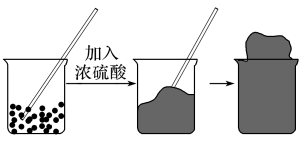
(2)强氧化性
| 实验操作 |
|
| 实验现象 | a试管中铜丝表面 |
| 实验结论 | 在反应中,氧化剂是 与浓硫酸反应的化学方程式: 与浓硫酸反应的化学方程式: |
您最近一年使用:0次
解题方法
8 . A、B、C、D、E、F为短周期元素, 原子序数依次增大。非金属元素A 最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。E+与D2-具有相同的电子层结构。A单质在F单质中燃烧,产物溶于水得到一种强酸M。回答下列问题:
(1)画出E的离子结构示意图___________ 。
(2)F在周期表中的位置是___________ 。
(3)B、D、E组成的一种常见盐,其中D的质量分数约为 45%,该盐与少量M溶液反应的离子方程式为___________ 。
(4)由这些元素组成的物质,相关信息如下:
①a的电子式为___________ 。 写出其与水反应的化学方程式:___________ 。
②b的一种常见用途为___________ 。
③已知c中所有原子均满足8 电子稳定结构,该化合物的结构式为___________ 。
(1)画出E的离子结构示意图
(2)F在周期表中的位置是
(3)B、D、E组成的一种常见盐,其中D的质量分数约为 45%,该盐与少量M溶液反应的离子方程式为
(4)由这些元素组成的物质,相关信息如下:
| 物质 | 组成和结构信息 |
| a | 由 A、E组成的离子化合物 |
| b | 由D、E组成的含非极性键的离子化合物,阴阳离子数之比为1:2 |
| c | 化学式为BDF2的共价化合物 |
②b的一种常见用途为
③已知c中所有原子均满足8 电子稳定结构,该化合物的结构式为
您最近一年使用:0次
2024-04-27更新
|
44次组卷
|
2卷引用:安徽省淮北市龙兴中学2023-2024学年高一上学期期末化学试卷
名校
解题方法
9 . 氨对人类生产、生活有重要影响。回答下列问题:
(1)合成氨是工业上人工固氮的重要方法,写出该反应的化学方程式:__________ 。
(2)氨气的制备
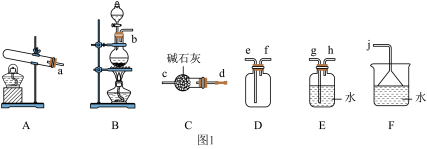
①氨气的发生装置可以选择图1中的__________ (填字母),反应的化学方程式为__________ 。
②欲收集一瓶干燥的氨气,选择图1中的装置,其连接顺序为:发生装置→__________ (按气流方向,用小写字母表示)。
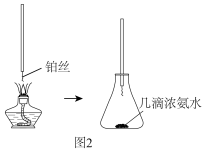
(3)氨的催化氧化:已知NH3在Pt催化和加热条件下与氧气反应,如图2是探究氨的催化氧化简易装置,观察到锥形瓶中铂丝保持红热,有红棕色气体或白烟产生。红棕色气体成分是___________ (填化学式,下同),白烟的成分是____________ 。
(1)合成氨是工业上人工固氮的重要方法,写出该反应的化学方程式:
(2)氨气的制备


①氨气的发生装置可以选择图1中的
②欲收集一瓶干燥的氨气,选择图1中的装置,其连接顺序为:发生装置→
(3)氨的催化氧化:已知NH3在Pt催化和加热条件下与氧气反应,如图2是探究氨的催化氧化简易装置,观察到锥形瓶中铂丝保持红热,有红棕色气体或白烟产生。红棕色气体成分是
您最近一年使用:0次
名校
10 . X、Y、Z是中学化学常见的三种物质,它们之间的相互转化关系如下(X、Y、Z、E、F为英文字母,部分反应条件及产物略去)

I.若Y是一种易溶于水,且能使品红溶液褪色的无色刺激性气味的气体。
(1)则Y和新制氯水主要成分反应生成两种强酸的化学方程式__________ 。
(2)Y气体的大量排放会形成酸雨,在工业上可以用足量氨水吸收,化学方程式为__________
(3)Z的水溶液可以制得某种强酸E。实验室用98%的浓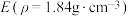 溶液配制1.5mol·L-1稀E溶液240mL。
溶液配制1.5mol·L-1稀E溶液240mL。
①制该稀E溶液需要使用的玻璃仪器有胶头滴管、量筒、烧杯、玻璃棒和__________ ;
②算所需E浓溶液的体积为__________ mL(保留1位小数)。
Ⅱ.若Z是淡黄色固体粉末。
(4)在呼吸面具或潜水艇中由Z和CO2制备氧气的化学反应方程式为__________ 。

I.若Y是一种易溶于水,且能使品红溶液褪色的无色刺激性气味的气体。
(1)则Y和新制氯水主要成分反应生成两种强酸的化学方程式
(2)Y气体的大量排放会形成酸雨,在工业上可以用足量氨水吸收,化学方程式为
(3)Z的水溶液可以制得某种强酸E。实验室用98%的浓
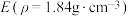 溶液配制1.5mol·L-1稀E溶液240mL。
溶液配制1.5mol·L-1稀E溶液240mL。①制该稀E溶液需要使用的玻璃仪器有胶头滴管、量筒、烧杯、玻璃棒和
②算所需E浓溶液的体积为
Ⅱ.若Z是淡黄色固体粉末。
(4)在呼吸面具或潜水艇中由Z和CO2制备氧气的化学反应方程式为
您最近一年使用:0次