名校
解题方法
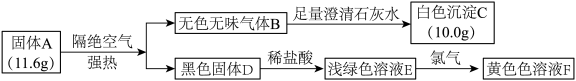
1 . 探究固体A(仅含3种元素)的组成和性质,设计并完成了如图所示实验:
(1)A的组成元素为O及___________ (填元素符号)。
(2)C的化学式为___________ 。
(3)E→F的离子方程式为___________ 。
(4)下列说法正确的是___________。
(1)A的组成元素为O及
(2)C的化学式为
(3)E→F的离子方程式为
(4)下列说法正确的是___________。
| A.固体A中金属原子和O原子物质的量之比为1:3 |
| B.黑色固体D可用作磁性材料 |
| C.将5mL1mol/LF溶液与5mL1mol/LNaOH溶液混合,可制得一种红褐色胶体 |
| D.检验E中金属阳离子的方法:先加KSCN溶液,再通少量Cl2 |
您最近一年使用:0次
名校
解题方法
2 . 甲基丙烯酸甲酯(MMA)可合成有机玻璃,MMA的一种合成方法如下:
(1)MMA的分子式为___________ 。
(2)MMA中官能团的名称为___________ 和___________ 。
(3)MMA合成有机玻璃( )的反应类型为
)的反应类型为___________ 。
(4)甲基丙烯酸与甲醇反应生成MMA的化学方程式为___________ 。

(1)MMA的分子式为
(2)MMA中官能团的名称为
(3)MMA合成有机玻璃(
 )的反应类型为
)的反应类型为(4)甲基丙烯酸与甲醇反应生成MMA的化学方程式为
您最近一年使用:0次
名校
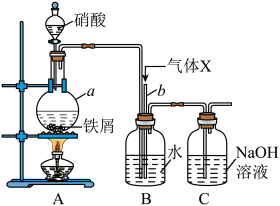
3 . 某同学设计如图所示装置制备硝酸亚铁溶液(气体X制备装置已略去)。
(1)仪器a的名称为___________ 。
(2)通过导管b向装置B内通入的气体X为___________ 。
(3)装置C的作用为___________ 。
(4)设计实验方案检验硝酸亚铁溶液中是否存在铁离子___________ 。
(5)下列说法不正确的是___________。
(1)仪器a的名称为
(2)通过导管b向装置B内通入的气体X为
(3)装置C的作用为
(4)设计实验方案检验硝酸亚铁溶液中是否存在铁离子
(5)下列说法不正确的是___________。
| A.装置A中缺少陶土网 | B.仪器a内始终不会出现红棕色气体 |
| C.铁屑须过量,否则溶液中可能含有硝酸铁 | D.NaOH溶液可以换成 溶液 溶液 |
您最近一年使用:0次
名校
4 . 以氯化钠为原料可以制备纯碱、烧碱、漂白粉等多种工业产品,流程示意图如下:
(1)晶体Z的化学式为___________ 。
(2)漂白粉在潮湿的空气中变质的化学方程式为___________ 。
(3)步骤Ⅲ先后通入的气体X和气体Y分别为___________ 和___________ 。
(4)下列说法不正确的是___________。

(1)晶体Z的化学式为
(2)漂白粉在潮湿的空气中变质的化学方程式为
(3)步骤Ⅲ先后通入的气体X和气体Y分别为
(4)下列说法不正确的是___________。
A.步骤Ⅰ发生的反应 |
| B.步骤Ⅱ制备漂白粉的试剂W为冷的澄清石灰水 |
C.步骤Ⅳ得到的滤液中浓度最大的2种离子为 、 、 |
| D.步骤Ⅴ反应产生的一种气体可以在步骤Ⅲ中循环利用 |
您最近一年使用:0次
5 . 利用反应Ⅰ.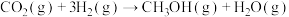
 ,可减少CO2排放,是实现“双碳”目标的途径之一、该反应一般认为可通过以下两步来实现:
,可减少CO2排放,是实现“双碳”目标的途径之一、该反应一般认为可通过以下两步来实现:
反应Ⅱ.
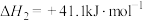
反应Ⅲ.

请回答:
(1)反应Ⅰ自发进行的条件是___________ 。(填“高温”、“低温”或“任何温度”)
(2)一定压强下,往某密闭容器中按投料比 充入H2和CO2反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
充入H2和CO2反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。___________ 。
A.图中X、Y分别代表CO、H2O
B.增大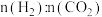 的比值,H2的平衡转化率增大
的比值,H2的平衡转化率增大
C.若容器内混合气体的密度不再随时间改变时,说明反应已达到平衡状态
D.250℃时,反应Ⅱ的平衡常数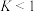
②体系中的CO2物质的量分数受温度的影响不大,试分析原因___________ 。
(3)在一定温度下,在一容积固定的密闭容器中充入1 mol CO2(g)和3 mol H2(g),仅发生反应Ⅰ。起始时容器内气体的总压强为16p kPa,平衡时CH3OH(g)的体积分数为30%,则该温度下反应Ⅰ的平衡常数
___________ 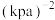 (用含p的表达式表示)。(已知:用气体分压计算的平衡常数为
(用含p的表达式表示)。(已知:用气体分压计算的平衡常数为 ,分压=总压×物质的量分数)。
,分压=总压×物质的量分数)。
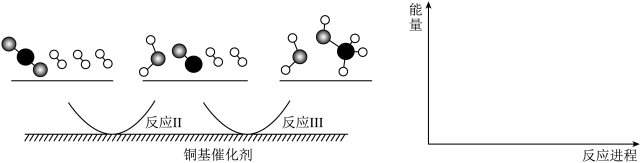
(4)多相催化反应是在催化剂表面通过“扩散→吸附→反应→脱附”四个基本过程进行的。CO2的平衡转化率随着H2浓度的增加先增大后减小,请解释原因___________ 。如图,我国学者发现T℃时,在铜催化剂上二氧化碳加氢的反应机理如下,其中反应Ⅱ为慢反应,请画出反应能量变化图像___________ 。
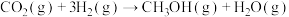
 ,可减少CO2排放,是实现“双碳”目标的途径之一、该反应一般认为可通过以下两步来实现:
,可减少CO2排放,是实现“双碳”目标的途径之一、该反应一般认为可通过以下两步来实现:反应Ⅱ.

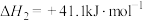
反应Ⅲ.


请回答:
(1)反应Ⅰ自发进行的条件是
(2)一定压强下,往某密闭容器中按投料比
 充入H2和CO2反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
充入H2和CO2反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。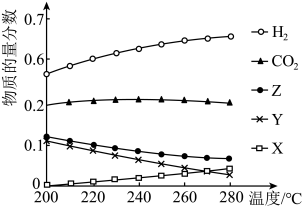
A.图中X、Y分别代表CO、H2O
B.增大
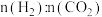 的比值,H2的平衡转化率增大
的比值,H2的平衡转化率增大C.若容器内混合气体的密度不再随时间改变时,说明反应已达到平衡状态
D.250℃时,反应Ⅱ的平衡常数
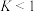
②体系中的CO2物质的量分数受温度的影响不大,试分析原因
(3)在一定温度下,在一容积固定的密闭容器中充入1 mol CO2(g)和3 mol H2(g),仅发生反应Ⅰ。起始时容器内气体的总压强为16p kPa,平衡时CH3OH(g)的体积分数为30%,则该温度下反应Ⅰ的平衡常数

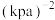 (用含p的表达式表示)。(已知:用气体分压计算的平衡常数为
(用含p的表达式表示)。(已知:用气体分压计算的平衡常数为 ,分压=总压×物质的量分数)。
,分压=总压×物质的量分数)。(4)多相催化反应是在催化剂表面通过“扩散→吸附→反应→脱附”四个基本过程进行的。CO2的平衡转化率随着H2浓度的增加先增大后减小,请解释原因
您最近一年使用:0次
2024-05-18更新
|
190次组卷
|
2卷引用:浙江省宁波市镇海中学2023-2024学年高二下学期期末考试化学试题
名校
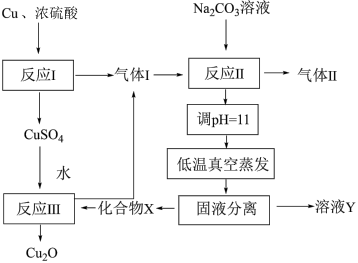
6 . 一种制备 的工艺路线如图所示。反应Ⅱ所得溶液pH在3~4之间,反应Ⅲ需及时补加NaOH以保持反应在pH=5条件下进行。
的工艺路线如图所示。反应Ⅱ所得溶液pH在3~4之间,反应Ⅲ需及时补加NaOH以保持反应在pH=5条件下进行。
已知:常温下, 的电离平衡常数
的电离平衡常数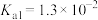 ,
,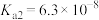 。
。
请回答: 的化学方程式为
的化学方程式为___________ 。
(2)反应 的离子反应方程式为
的离子反应方程式为___________ 。
(3)下列说法正确的是___________。
(4)反应 需及时补加NaOH以保持反应在pH=5条件下进行,原因是
需及时补加NaOH以保持反应在pH=5条件下进行,原因是___________ (结合离子反应方程式和必要的文字说明)。
(5)请用实验验证反应 后的溶液中存在的阳离子
后的溶液中存在的阳离子___________ 。
 的工艺路线如图所示。反应Ⅱ所得溶液pH在3~4之间,反应Ⅲ需及时补加NaOH以保持反应在pH=5条件下进行。
的工艺路线如图所示。反应Ⅱ所得溶液pH在3~4之间,反应Ⅲ需及时补加NaOH以保持反应在pH=5条件下进行。已知:常温下,
 的电离平衡常数
的电离平衡常数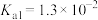 ,
,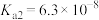 。
。请回答:
 的化学方程式为
的化学方程式为(2)反应
 的离子反应方程式为
的离子反应方程式为(3)下列说法正确的是___________。
A.反应 、 、 、 、 均为氧化还原反应 均为氧化还原反应 |
B.低温真空蒸发主要目的是防止 分解 分解 |
C.溶液Y可循环用于反应 所在操作单元吸收气体 所在操作单元吸收气体 |
D.若 产量不变,参与反应 产量不变,参与反应 的X与 的X与 物质的量之比 物质的量之比 增大时,需补加NaOH的量减少 增大时,需补加NaOH的量减少 |
(4)反应
 需及时补加NaOH以保持反应在pH=5条件下进行,原因是
需及时补加NaOH以保持反应在pH=5条件下进行,原因是(5)请用实验验证反应
 后的溶液中存在的阳离子
后的溶液中存在的阳离子
您最近一年使用:0次
2024-05-13更新
|
101次组卷
|
2卷引用:浙江省宁波市镇海中学2023-2024学年高二下学期期末考试化学试题
名校
解题方法
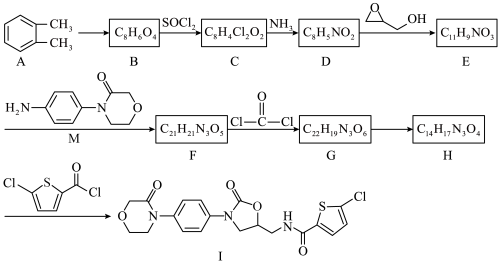
7 . 利伐沙班(Ⅰ)是一种新型抗凝血药物,其合成路线如下:
请回答:
(1)下列说法正确的是______。
(2)化合物F的结构简式是______ 。
(3)写出D→E的化学方程式______ 。
(4)请写出5种同时符合下列条件的M(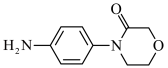 )的同分异构体的结构简式
)的同分异构体的结构简式______ 。
①含有两个六元环,其中一个为苯环,且苯环上一氯代物有两种;
②无氮氧键;
③核磁共振氢谱显示有5组峰。
(5)合成M时,需要先合成中间产物 ,请以乙烯和
,请以乙烯和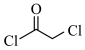 为原料,设计
为原料,设计 的合成路线(用流程图表示,无机试剂任选)
的合成路线(用流程图表示,无机试剂任选)______ 。
已知:①
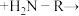
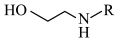

请回答:
(1)下列说法正确的是______。
| A.化合物B和苯甲酸互为同系物 |
| B.化合物F→G的反应类型属于取代反应 |
| C.1mol化合物G可以和5molNaOH反应 |
| D.化合物H和Ⅰ都有碱性,且分子中都有2个手性碳原子 |
(2)化合物F的结构简式是
(3)写出D→E的化学方程式
(4)请写出5种同时符合下列条件的M(
 )的同分异构体的结构简式
)的同分异构体的结构简式①含有两个六元环,其中一个为苯环,且苯环上一氯代物有两种;
②无氮氧键;
③核磁共振氢谱显示有5组峰。
(5)合成M时,需要先合成中间产物
 ,请以乙烯和
,请以乙烯和 为原料,设计
为原料,设计 的合成路线(用流程图表示,无机试剂任选)
的合成路线(用流程图表示,无机试剂任选)
您最近一年使用:0次
2024-05-11更新
|
244次组卷
|
2卷引用:浙江省宁波市镇海中学2023-2024学年高二下学期期末考试化学试题
8 . 某兴趣小组用下图的装置制取ICl,并用ICl的冰醋酸溶液来测定某油脂的不饱和度。油脂的不饱和度是指一个油脂分子最多可加成的氢分子数。
已知:①ICl的熔点为13.9℃,沸点为97.4℃,化学性质与氯气相似易水解;
② ,ICl3的熔点为111℃。
,ICl3的熔点为111℃。
(1)写出第一个装置中发生反应的化学方程式:___________ 。
(2)虚线框内应选用的装置是___________ (填“甲”或“乙”)。___________ (用接口的字母表示)。
(4)下列有关说法正确的是___________。
(5)用ICl的冰醋酸溶液测定某油脂的不饱和度,进行如下实验,实验过程中有关反应为:
将含有0.05mol某油脂的样品溶于CCl4后形成100mL溶液;从中取出10mL,加入20mL含有IC1物质的量为n mol的冰醋酸溶液(过量);充分反应后,加入足量KI溶液;生成的碘单质用a 的
的 标准溶液滴定;重复上述实验两次,测得滴定所需Na2S2O3的平均值为V mL。
标准溶液滴定;重复上述实验两次,测得滴定所需Na2S2O3的平均值为V mL。
①滴定前,需要将装有标准液的滴定管中的气泡排尽,应选择图中___________ 。___________ (用含a、n、V的表达式表示)。
已知:①ICl的熔点为13.9℃,沸点为97.4℃,化学性质与氯气相似易水解;
②
 ,ICl3的熔点为111℃。
,ICl3的熔点为111℃。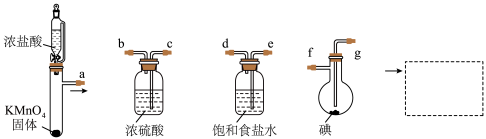
(1)写出第一个装置中发生反应的化学方程式:
(2)虚线框内应选用的装置是
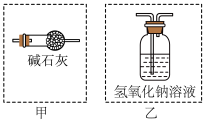
(4)下列有关说法正确的是___________。
| A.上述实验装置中的KMnO4固体也可用MnO2代替 |
| B.恒压滴液漏斗使用时应打开上面的玻璃塞 |
C.ICl与NaOH溶液反应的方程式为: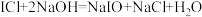 |
| D.若所制得的ICl中溶有少量ICl3杂质,可以采用蒸馏法进行提纯 |
(5)用ICl的冰醋酸溶液测定某油脂的不饱和度,进行如下实验,实验过程中有关反应为:
① ;②
;② ;③
;③
将含有0.05mol某油脂的样品溶于CCl4后形成100mL溶液;从中取出10mL,加入20mL含有IC1物质的量为n mol的冰醋酸溶液(过量);充分反应后,加入足量KI溶液;生成的碘单质用a
 的
的 标准溶液滴定;重复上述实验两次,测得滴定所需Na2S2O3的平均值为V mL。
标准溶液滴定;重复上述实验两次,测得滴定所需Na2S2O3的平均值为V mL。①滴定前,需要将装有标准液的滴定管中的气泡排尽,应选择图中
A.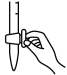 B.
B. 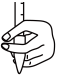 C.
C. 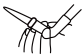 D.
D.
您最近一年使用:0次
2024-05-10更新
|
113次组卷
|
2卷引用:浙江省宁波市镇海中学2023-2024学年高二下学期期末考试化学试题
9 . 硫元素化合物非常丰富,应用广泛。
请回答:
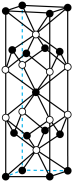
(1)由钾、镍、硫三种元素组成的某电极材料的晶胞如图,已知钾离子位于晶胞顶点及体心,其化学式是___________ ,与钾离子直接相邻的元素是___________ (填元素符号)。
(3)①硫酰卤( ):
):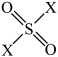 ,分子中S原子的杂化方式为:
,分子中S原子的杂化方式为:___________ ;比较键角
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
请回答:
(1)由钾、镍、硫三种元素组成的某电极材料的晶胞如图,已知钾离子位于晶胞顶点及体心,其化学式是
A.基态S原子的价层电子排布图: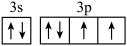 |
B.第一电离能: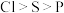 |
| C.K、Ni同为第四周期金属元素,都处于元素周期表d区 |
D.离子半径: |
(3)①硫酰卤(
 ):
): ,分子中S原子的杂化方式为:
,分子中S原子的杂化方式为:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②氟磺酸(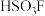 )属于超酸,可看作
)属于超酸,可看作 部分水解形成的产物。氟磺酸酸性比硫酸强。请从分子结构上说明氟磺酸酸性强的原因:
部分水解形成的产物。氟磺酸酸性比硫酸强。请从分子结构上说明氟磺酸酸性强的原因: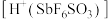 ,由
,由 (
(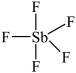 )与
)与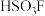 等物质的量化合生成。写出其中阴离子的结构式:
等物质的量化合生成。写出其中阴离子的结构式:
您最近一年使用:0次
2024-05-08更新
|
128次组卷
|
2卷引用:浙江省宁波市镇海中学2023-2024学年高二下学期期末考试化学试题
解题方法
10 . 一种由含铜废催化剂(主要成分为Cu和少量Fe、 、CuO,
、CuO, 等)为原料制备CuCl的工艺流程如下:
等)为原料制备CuCl的工艺流程如下: 浓度较大的体系
浓度较大的体系 ,不溶于乙醇,在潮湿空气中易被氧化。
,不溶于乙醇,在潮湿空气中易被氧化。
(1)下列说法正确的是________。
(2)步骤I中 的实际用量远远超过理论用量,可能原因是
的实际用量远远超过理论用量,可能原因是________ 。
(3)为测定CuCl产品纯度进行如下实验:
A.称量所得CuCl产品10.00g溶于硝酸,配制成250mL溶液;取出25.00mL,加入足量的 溶液,充分反应;
溶液,充分反应;
B.向其中加入少量硝基苯,使沉淀表面被有机物覆盖;
C.加入指示剂,用 标准溶液滴定过量的
标准溶液滴定过量的 溶液;
溶液;
D.重复实验操作三次,消耗 溶液的体积平均为10.00mL。
溶液的体积平均为10.00mL。
已知: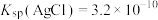 ,
,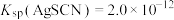 。
。
①加入硝基苯的作用是________ 。
②滴定选用的指示剂是________ ,滴定终点的现象为________ 。
A. B.
B. C.
C. D.
D.
③CuCl的纯度为________ 。
 、CuO,
、CuO, 等)为原料制备CuCl的工艺流程如下:
等)为原料制备CuCl的工艺流程如下:
 浓度较大的体系
浓度较大的体系 ,不溶于乙醇,在潮湿空气中易被氧化。
,不溶于乙醇,在潮湿空气中易被氧化。(1)下列说法正确的是________。
A.步骤Ⅰ,可以用 溶液代替双氧水 溶液代替双氧水 |
B.步骤Ⅱ,试剂X可以是CuO、 、 、 等物质 等物质 |
C.步骤Ⅲ, 适当过量的作用可能是及时除去反应过程中产生的 适当过量的作用可能是及时除去反应过程中产生的 ,避免产生 ,避免产生 |
D.步骤Ⅳ,为了防止CuCl被氧化,可用 水溶液洗涤 水溶液洗涤 |
(2)步骤I中
 的实际用量远远超过理论用量,可能原因是
的实际用量远远超过理论用量,可能原因是(3)为测定CuCl产品纯度进行如下实验:
A.称量所得CuCl产品10.00g溶于硝酸,配制成250mL溶液;取出25.00mL,加入足量的
 溶液,充分反应;
溶液,充分反应;B.向其中加入少量硝基苯,使沉淀表面被有机物覆盖;
C.加入指示剂,用
 标准溶液滴定过量的
标准溶液滴定过量的 溶液;
溶液;D.重复实验操作三次,消耗
 溶液的体积平均为10.00mL。
溶液的体积平均为10.00mL。已知:
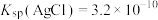 ,
,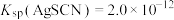 。
。①加入硝基苯的作用是
②滴定选用的指示剂是
A.
 B.
B. C.
C. D.
D.
③CuCl的纯度为
您最近一年使用:0次



