解题方法
1 . 某学生设计下列实验装置制取少量漂白粉。
(1)装置A中仪器a的名称是_______ 。
(2)装置B中盛放的试剂是_______ 。
(3)装置C中制取漂白粉的化学方程式是_______ 。
(4)装置D中 溶液的作用是
溶液的作用是_______ 。
(5)下列说法不正确 的是_______。

(1)装置A中仪器a的名称是
(2)装置B中盛放的试剂是
(3)装置C中制取漂白粉的化学方程式是
(4)装置D中
 溶液的作用是
溶液的作用是(5)下列说法
| A.搭好装置后,先加药品再检查气密性 |
| B.浓盐酸在反应中仅体现还原性 |
| C.漂白粉可用作游泳池的消毒剂 |
D.多孔球泡和搅拌器都能使石灰乳充分吸收 |
您最近一年使用:0次
解题方法
2 . 工业上以黄铁矿为原料制备硫酸的原理示意图如下。
(1)黄铁矿主要成分的化学式是_______ 。
(2)SO2使品红溶液褪色,体现SO2具有_______ 性。
(3)步骤Ⅲ的化学方程式是_______ 。
(4)下列说法不正确 的是_______。

(1)黄铁矿主要成分的化学式是
(2)SO2使品红溶液褪色,体现SO2具有
(3)步骤Ⅲ的化学方程式是
(4)下列说法
| A.步骤Ⅰ前需将黄铁矿粉碎,目的是增大接触面积,加快反应速率 |
| B.步骤Ⅱ中使用催化剂,能使SO2的转化率达到100% |
| C.步骤Ⅲ中选用98.3%的浓硫酸作吸收剂 |
| D.图中每一步含硫物质均发生氧化反应 |
您最近一年使用:0次
解题方法
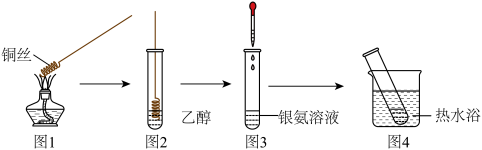
3 . 探究乙醇的氧化反应,并检验其产物,观察思考并回答下列问题 黑
黑 红”可推测,铜丝的作用是
红”可推测,铜丝的作用是_______ 。
(2)图2实验中乙醇的氧化产物是_______ 。
(3)为检验乙醇的氧化产物,需配置银氨溶液,具体操作如下:取洁净的试管,加入1mL____ (填序号,下同),一边振荡试管,一边逐滴加入____ ,直到最初产生的沉淀恰好溶解为止,得到银氨溶液。①氨水,②2%AgNO3溶液
(4)图4中水浴加热的优点是_______ 。
(5)图4试管壁出现光亮的银镜,实验结束后,可选用_______洗去银镜。
 黑
黑 红”可推测,铜丝的作用是
红”可推测,铜丝的作用是(2)图2实验中乙醇的氧化产物是
(3)为检验乙醇的氧化产物,需配置银氨溶液,具体操作如下:取洁净的试管,加入1mL
(4)图4中水浴加热的优点是
(5)图4试管壁出现光亮的银镜,实验结束后,可选用_______洗去银镜。
| A.盐酸 | B.稀硝酸 | C.氨水 | D.氨氧化钠溶液 |
您最近一年使用:0次
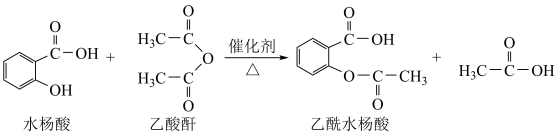
4 . 阿司匹林(乙酰水杨酸)是一具有解热镇痛作用的合成药物,以水杨酸为原料生产阿司匹林的主要反应是:
(1)乙酸酐的分子式是_______ 。
(2)水杨酸中含氧官能团的名称是羧基和_______ 。
(3)该反应的反应类型是_______ 。
(4)乙醇与乙酸酐反应的化学方程式是_______ 。
(1)乙酸酐的分子式是
(2)水杨酸中含氧官能团的名称是羧基和
(3)该反应的反应类型是
(4)乙醇与乙酸酐反应的化学方程式是
您最近一年使用:0次
解题方法
5 . 某合金粉末中含有铜、银、铬(Cr),为了从中回收贵金属银和一种盐晶体,某化学兴趣小组的同学们将这三种金属随意编号为A、B、C,设计了如下实验流程:

(1)A、B、C三种金属的活动性顺序由大到小为___________ (用化学式作答)。
(2)操作a中除烧杯、玻璃棒外还需用到的玻璃仪器是___________ ,操作b的名称是___________ 。
(3)已知A的硫酸盐中A元素是 价,请写出步骤①的化学反应方程式:
价,请写出步骤①的化学反应方程式:___________ 。
(4)已知D易溶于水,溶液D中的溶质是___________ (写化学式),写出步骤②的化学反应方程式:___________ 。
(5)溶液D的质量___________ (选填“大于”“小于”或“等于”)滤液E的质量。

(1)A、B、C三种金属的活动性顺序由大到小为
(2)操作a中除烧杯、玻璃棒外还需用到的玻璃仪器是
(3)已知A的硫酸盐中A元素是
 价,请写出步骤①的化学反应方程式:
价,请写出步骤①的化学反应方程式:(4)已知D易溶于水,溶液D中的溶质是
(5)溶液D的质量
您最近一年使用:0次
解题方法
6 . 一包固体,可能含有镁粉、碳粉、氧化铜、氢氧化钠、氯化钾中的一种或几种。为探究固体的组成,某化学兴趣小组进行了如下图所示实验:
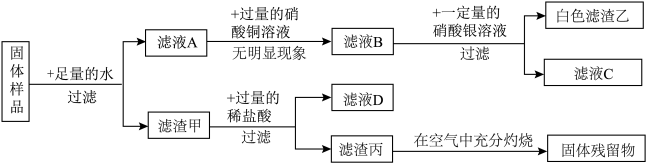
请回答下列问题:
(1)该实验中生成白色沉淀滤渣乙的化学方程式为___________ 。
(2)原固体中一定不含有的物质是(写名称或化学式均可,下同)___________ ,证据是___________ 。
(3)原固体中一定含有的物质是___________ 。
(4)实验结束后,该兴趣小组将滤液C和滤液D都倒入废液缸,有白色沉淀生成,上层清液E为蓝色,经检验,E中不含氯离子,则E中一定含有的溶质是___________ 。

请回答下列问题:
(1)该实验中生成白色沉淀滤渣乙的化学方程式为
(2)原固体中一定不含有的物质是(写名称或化学式均可,下同)
(3)原固体中一定含有的物质是
(4)实验结束后,该兴趣小组将滤液C和滤液D都倒入废液缸,有白色沉淀生成,上层清液E为蓝色,经检验,E中不含氯离子,则E中一定含有的溶质是
您最近一年使用:0次
7 . 有一包粉末,可能由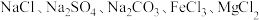 中的一种或几种组成。现做如下实验:
中的一种或几种组成。现做如下实验:
①取少量粉末,加水溶解得无色透明溶液;
②取①所得溶液少许加入氢氧化钠溶液,看不到明显现象;
③另取少量粉末滴加稀盐酸,也看不到明显现象。
试回答:
(1)由以上实验可知,原粉末中一定没有___________ (填化学式,下同)。
(2)根据上述实验,可得原粉末中可能有的物质是___________ 。
(3)为进一步探究原粉末中的成分,按下图进行实验:(提示:在 中选择两种作为A、B试剂,且A、B的阳离子不同)
中选择两种作为A、B试剂,且A、B的阳离子不同)___________ ,试剂A为___________ ,试剂B为___________ ;生成白色沉淀的化学方程式为___________ 。
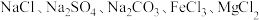 中的一种或几种组成。现做如下实验:
中的一种或几种组成。现做如下实验:①取少量粉末,加水溶解得无色透明溶液;
②取①所得溶液少许加入氢氧化钠溶液,看不到明显现象;
③另取少量粉末滴加稀盐酸,也看不到明显现象。
试回答:
(1)由以上实验可知,原粉末中一定没有
(2)根据上述实验,可得原粉末中可能有的物质是
(3)为进一步探究原粉末中的成分,按下图进行实验:(提示:在
 中选择两种作为A、B试剂,且A、B的阳离子不同)
中选择两种作为A、B试剂,且A、B的阳离子不同)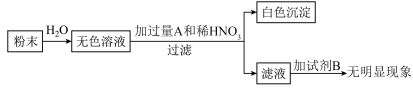
您最近一年使用:0次
解题方法
8 . NBICS化学学习小组为探究由三种元素构成的化合物X的组成和性质,设计并完成如下实验(假设各步反应均完全,反应中气体完全逸出,气体体积为标准状况),已知B为气体,E的焰色为黄色,C为两种正盐的混合物。
(1)固体X的化学式是___________
(2)写出X受热分解的化学方程式:___________ 。
(3)写出混合物C与稀硫酸反应产生F的离子方程式:___________ 。
(4)请设计实验方案,检验气体B常见的化学性质(三种):___________ 。
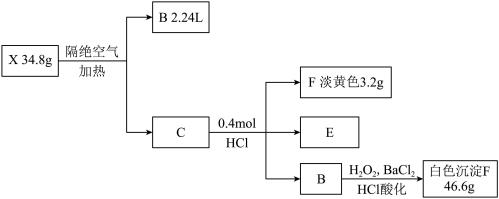
(1)固体X的化学式是
(2)写出X受热分解的化学方程式:
(3)写出混合物C与稀硫酸反应产生F的离子方程式:
(4)请设计实验方案,检验气体B常见的化学性质(三种):
您最近一年使用:0次
9 . 已知卤代烃A是烷烃的一氯代物,A的mol质量为64.5g/mol,B为一种常见调味剂,D为一种无机酸与一种烯烃衍生物的混合物,G是一种芳香物质。
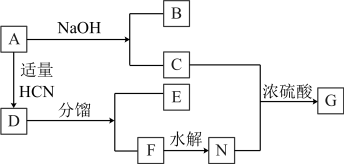
(1)已知CN-的性质和卤素离子类似,那么乙烯和HCN反应的方程式为___________ 。
(2)写出合成G的方程式___________ 。
(3)A到B,C的反应类型___________
(4)下列选项正确的是:___________

(1)已知CN-的性质和卤素离子类似,那么乙烯和HCN反应的方程式为
(2)写出合成G的方程式
(3)A到B,C的反应类型
(4)下列选项正确的是:___________
| A.C可以使酸性高锰酸钾褪色 |
| B.E具有漂白性 |
| C.生成G的过程中,浓硫酸只起到催化作用 |
| D.同H+浓度下,E与N中N的物质的量浓度更大 |
您最近一年使用:0次
解题方法
10 . 某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。
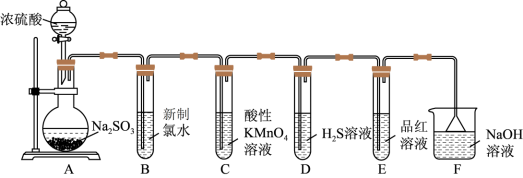
已知: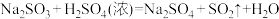 ;请回答下列问题:
;请回答下列问题:
(1)装置A中盛放亚硫酸钠溶液的仪器名称是_______ 。
(2)装置B中发生的离子方程式为_______ 。
(3)以上装置中表现了SO2氧化性的是_______ (填装置字母);
(4)装置F中倒扣漏斗的作用是_______ 。
(5)装置E的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:_______ 。

已知:
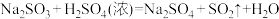 ;请回答下列问题:
;请回答下列问题:(1)装置A中盛放亚硫酸钠溶液的仪器名称是
(2)装置B中发生的离子方程式为
(3)以上装置中表现了SO2氧化性的是
(4)装置F中倒扣漏斗的作用是
(5)装置E的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:
您最近一年使用:0次



