1 . 某研究性学习小组制取 并探究
并探究 及铵盐的相关性质。反应的化学方程式为:
及铵盐的相关性质。反应的化学方程式为:
 。
。
查阅资料得知,铵盐通常是白色晶体,易溶于水,受热易分解,能与碱反应产生 ,浓氨水易挥发。
,浓氨水易挥发。
【制取 】
】
(1)按如图所示装置制取 ,生成的
,生成的 可用
可用_____ (填“浓硫酸”或“碱石灰”干燥)。_____ (填“向上”或“向下”)排气集气法。
(3)若生成标准状况下 ,至少需要
,至少需要 的质量为
的质量为_____ g( 的摩尔质量为
的摩尔质量为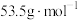 )。
)。
(4)某同学用刚清洗过、含有较多水分的集气瓶收集 ,结果收集不到气体,原因是
,结果收集不到气体,原因是_____ 。
(5)为确认某固体化肥样品中含有 ,不必用到的试纸或试剂是
,不必用到的试纸或试剂是_____ 。
① 溶液②红色石蕊试纸③稀硫酸
溶液②红色石蕊试纸③稀硫酸
 并探究
并探究 及铵盐的相关性质。反应的化学方程式为:
及铵盐的相关性质。反应的化学方程式为: 。
。查阅资料得知,铵盐通常是白色晶体,易溶于水,受热易分解,能与碱反应产生
 ,浓氨水易挥发。
,浓氨水易挥发。【制取
 】
】(1)按如图所示装置制取
 ,生成的
,生成的 可用
可用
(3)若生成标准状况下
 ,至少需要
,至少需要 的质量为
的质量为 的摩尔质量为
的摩尔质量为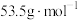 )。
)。(4)某同学用刚清洗过、含有较多水分的集气瓶收集
 ,结果收集不到气体,原因是
,结果收集不到气体,原因是(5)为确认某固体化肥样品中含有
 ,不必用到的试纸或试剂是
,不必用到的试纸或试剂是①
 溶液②红色石蕊试纸③稀硫酸
溶液②红色石蕊试纸③稀硫酸
您最近一年使用:0次
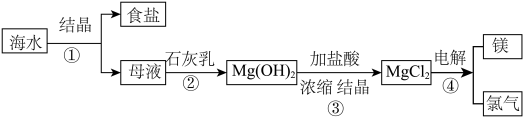
2 . 海水是重要资源,从海水中提取镁的流程如下图所示。_____ (填“降温”或“蒸发”)结晶法。
(2)步骤②分离 沉淀与溶液的实验操作名称为
沉淀与溶液的实验操作名称为_____ 。
(3)流程图的4个步骤中发生了氧化还原反应的是_____ 。(填序号)。
(4)步骤③发生反应的化学方程式为_____ 。
(2)步骤②分离
 沉淀与溶液的实验操作名称为
沉淀与溶液的实验操作名称为(3)流程图的4个步骤中发生了氧化还原反应的是
(4)步骤③发生反应的化学方程式为
您最近一年使用:0次
解题方法
3 . 下表为元素周期表中的一部分,表中列出10种元素在周期表中的位置,按要求回答下列各题。
(1)这10种元素中,化学性质最稳定的元素是_____ (写元素符号)。
(2)地壳中含量最丰富的元素是_____ (写元素名称)。
(3)元素①②③最高价氧化物对应的水化物,碱性最强的物质名称是_____
(4)元素⑥的氢化物的化学式是_____ (写一种)。
(5)④⑥⑦中原子半径由大到小的顺序是_____ (写元素名称)
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ④ | ⑥ | ⑦ | |||||
| 3 | ① | ② | ③ | ⑤ | ⑧ | ⑨ | ⑩ | |
(1)这10种元素中,化学性质最稳定的元素是
(2)地壳中含量最丰富的元素是
(3)元素①②③最高价氧化物对应的水化物,碱性最强的物质名称是
(4)元素⑥的氢化物的化学式是
(5)④⑥⑦中原子半径由大到小的顺序是
您最近一年使用:0次
4 . 某兴趣小组利用下列装置,制取氯气并进行与氯气相关的实验。___________ ;
(2)实验结束后,取装置③中的溶液,经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到 晶体。在蒸发浓缩操作中,不需要的仪器是___________(填字母);
晶体。在蒸发浓缩操作中,不需要的仪器是___________(填字母);
(3)装置②中出现白色沉淀,据此现象能否推测装置①中生成Cl2?___________ (填“能”或“否”),应在①②装置之间增加装有___________ 的洗气瓶(选填“NaOH溶液”或“饱和NaCl溶液”);
(4)若要使③中 溶液20mL恰好完全反应,则①中至少生成Cl2的体积为
溶液20mL恰好完全反应,则①中至少生成Cl2的体积为___________ mL(标准状况)。( )
)

(2)实验结束后,取装置③中的溶液,经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到
 晶体。在蒸发浓缩操作中,不需要的仪器是___________(填字母);
晶体。在蒸发浓缩操作中,不需要的仪器是___________(填字母);| A.蒸发皿 | B.漏斗 | C.玻璃棒 | D.酒精灯 |
(3)装置②中出现白色沉淀,据此现象能否推测装置①中生成Cl2?
(4)若要使③中
 溶液20mL恰好完全反应,则①中至少生成Cl2的体积为
溶液20mL恰好完全反应,则①中至少生成Cl2的体积为 )
)
您最近一年使用:0次
5 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。根据题意回答下列问题:
(1)①的元素符号是___________ ;
(2)③、④的原子半径大小是:③___________ ④(填“>”或“<”);
(3)②、⑤的非金属性从强到弱的顺序是:___________ (填元素符号);
(4)③的最高价氧化物的水化物和④的最高价氧化物的水化物在溶液中反应的离子方程式为___________ 。
| 族 周期 | IA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | VA | VIA | ⅦA | |||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | Ar | |||||
(2)③、④的原子半径大小是:③
(3)②、⑤的非金属性从强到弱的顺序是:
(4)③的最高价氧化物的水化物和④的最高价氧化物的水化物在溶液中反应的离子方程式为
您最近一年使用:0次
解题方法
6 . 以菱铁矿(主要成分是碳酸亚铁 )为原料制取铁的流程如图:
)为原料制取铁的流程如图: 中氧元素的化合价为
中氧元素的化合价为_______ (填“-1”或“-2”)。
(2)“浸取”时通常将菱铁矿石进行粉碎,其目的是_____ (填“增大”或“减小”)反应速率。
(3)“氧化”和“沉淀”是将“浸取”过程中产生的 转化为
转化为 沉淀,则操作①的名称为(填“蒸发”或“过滤”)
沉淀,则操作①的名称为(填“蒸发”或“过滤”)_______ 。
(4)在5L的密闭容器中加入4mol 和8mol
和8mol  生反应
生反应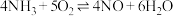 ,反应2s后,NO增加了2mol。
,反应2s后,NO增加了2mol。
①用NO的浓度变化表示反应的平均速率为_______ 。
②其他条件不变,再通入 ,反应速率将
,反应速率将_______ (填“增大”或“减小”)。
 )为原料制取铁的流程如图:
)为原料制取铁的流程如图:
 中氧元素的化合价为
中氧元素的化合价为(2)“浸取”时通常将菱铁矿石进行粉碎,其目的是
(3)“氧化”和“沉淀”是将“浸取”过程中产生的
 转化为
转化为 沉淀,则操作①的名称为(填“蒸发”或“过滤”)
沉淀,则操作①的名称为(填“蒸发”或“过滤”)(4)在5L的密闭容器中加入4mol
 和8mol
和8mol  生反应
生反应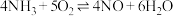 ,反应2s后,NO增加了2mol。
,反应2s后,NO增加了2mol。①用NO的浓度变化表示反应的平均速率为
②其他条件不变,再通入
 ,反应速率将
,反应速率将
您最近一年使用:0次
名校
解题方法
7 . 硫酸是重要的化工原料。工业上以硫黄为原料制备硫酸的流程图如下:
(1)硫磺____________ (填“难”或“易”)溶于水;
(2) 能使品红溶液褪色,体现了
能使品红溶液褪色,体现了 的
的____________ (填“还原性”或“漂白性”);
(3)实验室常用浓硫酸作为气体的干燥剂,表明浓硫酸具有____________ (填“吸水性”或“脱水性”);
(4)流程中 →
→ 发生的反应为:
发生的反应为: 。
。
①此步骤中加入 的作用是
的作用是____________ (填“加快”或“减小”)反应速率;
②为提高 的转化率,可采取的措施有
的转化率,可采取的措施有__________ (填一条)。

(1)硫磺
(2)
 能使品红溶液褪色,体现了
能使品红溶液褪色,体现了 的
的(3)实验室常用浓硫酸作为气体的干燥剂,表明浓硫酸具有
(4)流程中
 →
→ 发生的反应为:
发生的反应为: 。
。①此步骤中加入
 的作用是
的作用是②为提高
 的转化率,可采取的措施有
的转化率,可采取的措施有
您最近一年使用:0次
8 . 某化学课外兴趣小组为探究 的性质,设计了如下实验。
的性质,设计了如下实验。
(1)装置A中发生反应的化学方程式为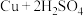 (浓)
(浓)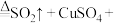
_____ 。
(2)打开K,点燃酒精灯开始反应,装置C中的现象是_____ 。
(3)装置D中酸性高锰酸钾溶液颜色变浅直至褪色,用来验证 具有
具有_____ (填“氧化”或“还原”)性。
(4)装置D中浸有 溶液的棉花的作用是
溶液的棉花的作用是_____ 。
(5)当生成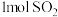 时,转移电子的物质的量是
时,转移电子的物质的量是_____ mol。
 的性质,设计了如下实验。
的性质,设计了如下实验。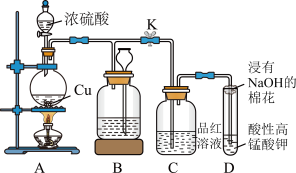
(1)装置A中发生反应的化学方程式为
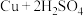 (浓)
(浓)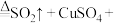
(2)打开K,点燃酒精灯开始反应,装置C中的现象是
(3)装置D中酸性高锰酸钾溶液颜色变浅直至褪色,用来验证
 具有
具有(4)装置D中浸有
 溶液的棉花的作用是
溶液的棉花的作用是(5)当生成
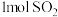 时,转移电子的物质的量是
时,转移电子的物质的量是
您最近一年使用:0次
名校
解题方法
9 . 海洋中有丰富的矿产、能源、水产等资源,部分化学资源获取途径如下:_____ (填“氧化”或“还原”)。
(2)工业上,除去粗盐中 加入
加入_____ [填“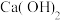 ”或“
”或“ ”]。
”]。
(3) 中含有的是
中含有的是_____ (填“离子键”或“共价键”)。
(4)在一定条件下,向体积为 的容器中加入
的容器中加入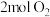 和
和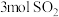 发生可逆反应:
发生可逆反应: ,
, 后测得
后测得 的物质的量为
的物质的量为 ,则:
,则:
①若用 的浓度变化来表示该反应的反应速率,则
的浓度变化来表示该反应的反应速率,则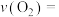
_____ ;
②当反应达到平衡时, 的浓度将
的浓度将_____ (填“增大”“减小”或“不再改变”)。

(2)工业上,除去粗盐中
 加入
加入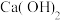 ”或“
”或“ ”]。
”]。(3)
 中含有的是
中含有的是(4)在一定条件下,向体积为
 的容器中加入
的容器中加入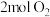 和
和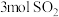 发生可逆反应:
发生可逆反应: ,
, 后测得
后测得 的物质的量为
的物质的量为 ,则:
,则:①若用
 的浓度变化来表示该反应的反应速率,则
的浓度变化来表示该反应的反应速率,则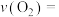
②当反应达到平衡时,
 的浓度将
的浓度将
您最近一年使用:0次
2024-06-28更新
|
70次组卷
|
2卷引用:2024年湖南省娄底市高二下学期学业水平考试化学试题
名校
解题方法
10 . 某化学学习小组利用乙醇、乙酸、浓硫酸来制取乙酸乙酯。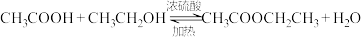
Ⅱ.实验操作:向试管A中加入碎瓷片和药品,按图连接好装置,用酒精灯缓慢加热,将产生的蒸汽经导管通到B试管中的液面上。
Ⅲ.查阅资料:乙酸乙酯不溶于水,密度比水小,且有香味
请回答下列问题:
(1)试管A中加入试剂的顺序是____________ (填标号);
A.先加乙醇,再加浓硫酸,最后加乙酸 B.先加浓硫酸,再加乙醇,最后加乙酸
(2)试管A中加入碎瓷片,其作用是____________ ;
(3)试管B中的溶液是饱和____________ (填“ ”或“NaOH”)溶液;
”或“NaOH”)溶液;
(4)实验完毕后,将B试管中的液体充分振荡,静置后,溶液分为两层,乙酸乙酯在____________ (填“上层”或“下层”);
(5)实验中若加入乙酸的质量为3.0g.其转化率为60%,则得到乙酸乙酯的质量为____________ g。
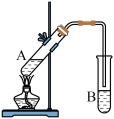
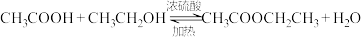
Ⅱ.实验操作:向试管A中加入碎瓷片和药品,按图连接好装置,用酒精灯缓慢加热,将产生的蒸汽经导管通到B试管中的液面上。
Ⅲ.查阅资料:乙酸乙酯不溶于水,密度比水小,且有香味
请回答下列问题:
(1)试管A中加入试剂的顺序是
A.先加乙醇,再加浓硫酸,最后加乙酸 B.先加浓硫酸,再加乙醇,最后加乙酸
(2)试管A中加入碎瓷片,其作用是
(3)试管B中的溶液是饱和
 ”或“NaOH”)溶液;
”或“NaOH”)溶液;(4)实验完毕后,将B试管中的液体充分振荡,静置后,溶液分为两层,乙酸乙酯在
(5)实验中若加入乙酸的质量为3.0g.其转化率为60%,则得到乙酸乙酯的质量为
您最近一年使用:0次



