解题方法
1 .  是重要的供氧剂。图所示装置(省略夹持部件)用于验证
是重要的供氧剂。图所示装置(省略夹持部件)用于验证 和
和 的反应,所需
的反应,所需 由
由 固体与稀盐酸反应制备。回答下列问题:
固体与稀盐酸反应制备。回答下列问题:______ 。
(2)验证装置的气密性时,需用F替换装置中的E。若装置气密性良好,应观察到F中的导管口会有______ 的现象。
(3)装置中的B与C用于除去 气体中的杂质。饱和
气体中的杂质。饱和 溶液的作用是吸收
溶液的作用是吸收______ (填化学式)气体;为了干燥 气体,C中盛放的试剂是足量的
气体,C中盛放的试剂是足量的______ 。
(4)实验过程中,D中部分 固体由淡黄色变为
固体由淡黄色变为______ 色。在E的瓶口放置一条带火星的木条,若木条复燃,则说明生成的气体是______ (填化学式),并且E中的气体______ (填“已集满”或“未集满”)。收集气体时,E的瓶口朝上的主要原因是______ 。
(5)完成上述实验后,除去玻璃纤维,回收D中的所有固体药品共22.76g。使该固体与过量的水充分反应,假定该反应生成的气体共224mL(标准状况)。据此计算,实验中与 反应的
反应的 的物质的量为
的物质的量为______ mol。
 是重要的供氧剂。图所示装置(省略夹持部件)用于验证
是重要的供氧剂。图所示装置(省略夹持部件)用于验证 和
和 的反应,所需
的反应,所需 由
由 固体与稀盐酸反应制备。回答下列问题:
固体与稀盐酸反应制备。回答下列问题:
(2)验证装置的气密性时,需用F替换装置中的E。若装置气密性良好,应观察到F中的导管口会有
(3)装置中的B与C用于除去
 气体中的杂质。饱和
气体中的杂质。饱和 溶液的作用是吸收
溶液的作用是吸收 气体,C中盛放的试剂是足量的
气体,C中盛放的试剂是足量的(4)实验过程中,D中部分
 固体由淡黄色变为
固体由淡黄色变为(5)完成上述实验后,除去玻璃纤维,回收D中的所有固体药品共22.76g。使该固体与过量的水充分反应,假定该反应生成的气体共224mL(标准状况)。据此计算,实验中与
 反应的
反应的 的物质的量为
的物质的量为
您最近一年使用:0次
解题方法
2 . NaHCO3干法脱硫具有无腐蚀、无废水等特点,常用于除去工业烟气中少量的SO2。为探究不同温度下烟气的脱硫效果,设计如图装置(省略夹持装置)进行模拟实验。回答下列问题。

(1)实验开始前,先检查装置的____ 。II中添加的SiO2使NaHCO3分散,从而____ (填“增大”或“减小”)反应物接触面,提高脱硫效果。
(2)通入由SO2、N2组成的模拟烟气,待气流稳定后,点燃II处酒精灯,缓慢升温。当II中脱硫温度低于270℃时,反应为2NaHCO3+SO2=Na2SO3+2CO2+H2O;高于270℃时,NaHCO3完全分解为Na2CO3。由于Na2CO3的碱性比NaHCO3的____ (填“强”或“弱”),因而其脱硫效果更好,Na2CO3脱硫反应的方程式为____ 。
(3)装置IV的作用是吸收体系中的残余SO2,可选用的试剂有____ 。
(4)保持II中反应温度为300℃不变,待气流完全稳定时,从SO2检测器读数并进行换算,得出I和III中SO2的浓度依次为C1、C2,用C1、C2表示的脱硫率计算式为____ 。
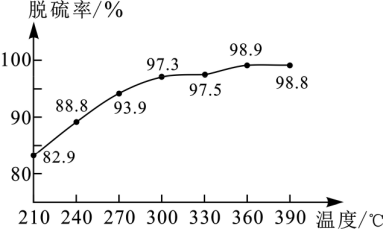
(5)持续测定并处理数据,得出不同温度下的脱硫率(如图)。根据图中实验数据判断,该方法最适宜的脱硫温度范围是____ ,选择该温度范围的理由有____ 。

(1)实验开始前,先检查装置的
(2)通入由SO2、N2组成的模拟烟气,待气流稳定后,点燃II处酒精灯,缓慢升温。当II中脱硫温度低于270℃时,反应为2NaHCO3+SO2=Na2SO3+2CO2+H2O;高于270℃时,NaHCO3完全分解为Na2CO3。由于Na2CO3的碱性比NaHCO3的
(3)装置IV的作用是吸收体系中的残余SO2,可选用的试剂有
| A.NaOH溶液 | B.酸性KMnO4溶液 | C.浓硫酸 | D.盐酸 |
(5)持续测定并处理数据,得出不同温度下的脱硫率(如图)。根据图中实验数据判断,该方法最适宜的脱硫温度范围是

您最近一年使用:0次
2022-08-15更新
|
97次组卷
|
2卷引用:广西壮族自治区普通高中2020—2021学年高三上学期12月学业水平考试化学试题
解题方法
3 . 二氧化硫( )主要用于生产硫酸,也可用作防腐剂和抗氧化剂,还可用作漂白剂。实验室常用
)主要用于生产硫酸,也可用作防腐剂和抗氧化剂,还可用作漂白剂。实验室常用 固体和70%硫酸溶液反应制备
固体和70%硫酸溶液反应制备 。某同学利用如图所示装置(夹持装置已省略)制备
。某同学利用如图所示装置(夹持装置已省略)制备 ,并验证其部分性质。回答下列问题:
,并验证其部分性质。回答下列问题:
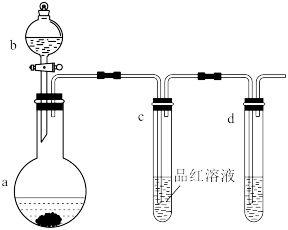
(1)按图组装好仪器后,应先检查装置的_______ 。
(2)仪器a的名称是:_______ ;仪器b中盛放的试剂是_______ 。
(3)实验过程中,试管c中的品红溶液褪色,这说明 具有
具有_______ 性。
(4)从氯水、KI溶液、 饱和溶液、酸性
饱和溶液、酸性 溶液四种试剂中,选择
溶液四种试剂中,选择_______ 加入试管d进行实验,可验证 的氧化性,与此实验有关的化学反应方程式为
的氧化性,与此实验有关的化学反应方程式为_______ 。
(5)从环境保护的角度考虑,进行上述实验还需对该装置加以改进,其措施为_______ 。
(6)上述实验完成后,加热试管c,可观察到的现象是_______ 。
 )主要用于生产硫酸,也可用作防腐剂和抗氧化剂,还可用作漂白剂。实验室常用
)主要用于生产硫酸,也可用作防腐剂和抗氧化剂,还可用作漂白剂。实验室常用 固体和70%硫酸溶液反应制备
固体和70%硫酸溶液反应制备 。某同学利用如图所示装置(夹持装置已省略)制备
。某同学利用如图所示装置(夹持装置已省略)制备 ,并验证其部分性质。回答下列问题:
,并验证其部分性质。回答下列问题:
(1)按图组装好仪器后,应先检查装置的
(2)仪器a的名称是:
(3)实验过程中,试管c中的品红溶液褪色,这说明
 具有
具有(4)从氯水、KI溶液、
 饱和溶液、酸性
饱和溶液、酸性 溶液四种试剂中,选择
溶液四种试剂中,选择 的氧化性,与此实验有关的化学反应方程式为
的氧化性,与此实验有关的化学反应方程式为(5)从环境保护的角度考虑,进行上述实验还需对该装置加以改进,其措施为
(6)上述实验完成后,加热试管c,可观察到的现象是
您最近一年使用:0次
解题方法
4 . 钠及其化合物在生产生活中有广泛应用,下图是部分钠的化合物与钠之间的转化关系。回答下列问题:
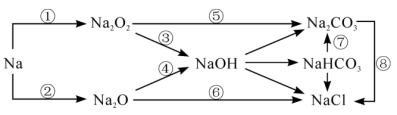
(1)转化①、②的反应条件不同,其中,实现转化①的反应条件为_______ 。
(2)通过Na2O2与CO2的反应可实现转化_______ (填图中的序号),因此,Na2O2可在潜水艇中作为氧气的重要来源。
(3)转化⑥可通过反应Na2O+2HCl=2NaCl+H2O实现,由该反应可推断,Na2O属于_______ (填“酸性”或“碱性”)氧化物。
(4)加热NaHCO3可实现转化⑦,这说明NaHCO3的热稳定性_______ (填“优于”或“不如”) Na2CO3。
(5)若选用BaCl2溶液实现转化⑧,则该转化反应的离子方程式为_______ 。
(6)家庭制作馒头时,面团里加入小苏打可中和面团在酵母菌作用下产生的酸性物质,从而改善馒头的口感,该中和过程中所产生的气体是_______ (填化学式)。
(7)实验室需使用80 mL 1.00 mol/L NaCl溶液。配制溶液时,先计算所需NaCl固体的质量:_______ g,接着称量;然后选择要用到的玻璃仪器:_______ 、烧杯、量筒、胶头滴管和玻璃棒;最后进行其它相关操作完成溶液配制。

(1)转化①、②的反应条件不同,其中,实现转化①的反应条件为
(2)通过Na2O2与CO2的反应可实现转化
(3)转化⑥可通过反应Na2O+2HCl=2NaCl+H2O实现,由该反应可推断,Na2O属于
(4)加热NaHCO3可实现转化⑦,这说明NaHCO3的热稳定性
(5)若选用BaCl2溶液实现转化⑧,则该转化反应的离子方程式为
(6)家庭制作馒头时,面团里加入小苏打可中和面团在酵母菌作用下产生的酸性物质,从而改善馒头的口感,该中和过程中所产生的气体是
(7)实验室需使用80 mL 1.00 mol/L NaCl溶液。配制溶液时,先计算所需NaCl固体的质量:
您最近一年使用:0次
名校
5 . 空气中主要污染有 、
、 、
、 等,其中
等,其中 是造成酸雨的主要成分。某研究小组对
是造成酸雨的主要成分。某研究小组对 导致酸雨的成因进行探究,用下图装置进行实验。
导致酸雨的成因进行探究,用下图装置进行实验。
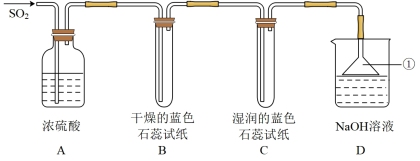
(1)装置A的作用是___________ (填“干燥”或“氧化”)SO2气体。
(2)实验过程中,装置B内干燥的蓝色石蕊试纸的颜色没有发生变化,装置C内湿润的蓝色石蕊试纸变___________ 色,说明 与水反应生成一种酸,该酸的化学式是
与水反应生成一种酸,该酸的化学式是___________ 。
(3)仪器①的名称是___________ ,其倒扣的目的是___________ 。
(4)若通入的 气体中混有少量
气体中混有少量 气体,要完成上述实验,需对该实验装置进行改进的方案是
气体,要完成上述实验,需对该实验装置进行改进的方案是___________ 。
(5)若往盛有水的烧杯中缓慢通入 气体。测得所得溶液的pH
气体。测得所得溶液的pH___________ 7(填“>”或“<”),然后每隔1h测定溶液的pH,发现pH逐渐变小,直至恒定,其原因是___________ (用化学方程式表示)
 、
、 、
、 等,其中
等,其中 是造成酸雨的主要成分。某研究小组对
是造成酸雨的主要成分。某研究小组对 导致酸雨的成因进行探究,用下图装置进行实验。
导致酸雨的成因进行探究,用下图装置进行实验。
(1)装置A的作用是
(2)实验过程中,装置B内干燥的蓝色石蕊试纸的颜色没有发生变化,装置C内湿润的蓝色石蕊试纸变
 与水反应生成一种酸,该酸的化学式是
与水反应生成一种酸,该酸的化学式是(3)仪器①的名称是
(4)若通入的
 气体中混有少量
气体中混有少量 气体,要完成上述实验,需对该实验装置进行改进的方案是
气体,要完成上述实验,需对该实验装置进行改进的方案是(5)若往盛有水的烧杯中缓慢通入
 气体。测得所得溶液的pH
气体。测得所得溶液的pH
您最近一年使用:0次
名校
解题方法
6 . 铁及其重要化合物在日常生活中应用广泛,其之间的部分转化关系如下图所示。
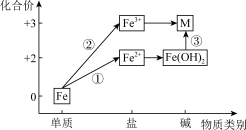
(1)M的化学式为___________ ,物质类别___________ 。
(2)实现①的转化,可选用足量的___________ (填“稀盐酸”或“NaOH溶液”),写出该转化的离子方程式___________ 。
(3)Fe在 中燃烧可实现②的转化,该反应的化学方程式为
中燃烧可实现②的转化,该反应的化学方程式为___________ 。
(4)实现③的转化,可选用下列试剂中的___________
(5)电子工业中,人们常用 溶液腐蚀覆在绝缘体上的铜箔
溶液腐蚀覆在绝缘体上的铜箔 制造印刷电路板。腐蚀后溶液中的阳离子有
制造印刷电路板。腐蚀后溶液中的阳离子有 、
、 、
、___________ 、___________ 。确认腐蚀后溶液中存在 ,可选用的试剂为
,可选用的试剂为___________ 溶液。

(1)M的化学式为
(2)实现①的转化,可选用足量的
(3)Fe在
 中燃烧可实现②的转化,该反应的化学方程式为
中燃烧可实现②的转化,该反应的化学方程式为(4)实现③的转化,可选用下列试剂中的___________
A. | B. | C. | D. |
 溶液腐蚀覆在绝缘体上的铜箔
溶液腐蚀覆在绝缘体上的铜箔 制造印刷电路板。腐蚀后溶液中的阳离子有
制造印刷电路板。腐蚀后溶液中的阳离子有 、
、 、
、 ,可选用的试剂为
,可选用的试剂为
您最近一年使用:0次
名校
解题方法
7 . 下表为元素周期表的一部分,回答以下问题:
(1) 与
与 的原子半径大小关系是:
的原子半径大小关系是:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(2)F与 的非金属性强弱顺序是:F
的非金属性强弱顺序是:F___________  (填“>”或“<”),其简单氢化物的稳定性较强的是
(填“>”或“<”),其简单氢化物的稳定性较强的是___________ (填化学式)。
(3)P、S两种元素的最高价氧化物对应水化物的酸性较弱的是___________ (填化学式)。
(4) 与
与 组成
组成
 所含的化学键类型为
所含的化学键类型为___________ (填“离子键”或“共价键”)。
(5)地壳中含量最高的金属元素是___________ ,能用来做光导纤维的是___________ 元素的氧化物(填元素符号)。
(6)C位于元素周期表中第___________ 周期第___________ 族,易以碳碳键和碳氢键形成甲烷 、乙烷
、乙烷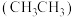 、乙烯
、乙烯 等烃类化合物。甲烷与乙烷属于
等烃类化合物。甲烷与乙烷属于___________ (填“同系物”或“同分异构体”);乙烷与乙烯可相互转化,如:

 生成
生成 的反应类型为
的反应类型为___________
| C | N | F | ||||
 |  |  |  |  |  |
 与
与 的原子半径大小关系是:
的原子半径大小关系是:
 (填“>”或“<”)。
(填“>”或“<”)。(2)F与
 的非金属性强弱顺序是:F
的非金属性强弱顺序是:F (填“>”或“<”),其简单氢化物的稳定性较强的是
(填“>”或“<”),其简单氢化物的稳定性较强的是(3)P、S两种元素的最高价氧化物对应水化物的酸性较弱的是
(4)
 与
与 组成
组成
 所含的化学键类型为
所含的化学键类型为(5)地壳中含量最高的金属元素是
(6)C位于元素周期表中第
 、乙烷
、乙烷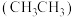 、乙烯
、乙烯 等烃类化合物。甲烷与乙烷属于
等烃类化合物。甲烷与乙烷属于
 生成
生成 的反应类型为
的反应类型为
您最近一年使用:0次
2022-05-15更新
|
409次组卷
|
3卷引用:广西柳州市第三中学2021-2022学年高一下学期高中学业水平合格性考试模拟卷化学试题
8 . 化合物D(C12H11ClO4)为合成某种液晶材料的中间体,其合成路线如图所示。回答下列问题。
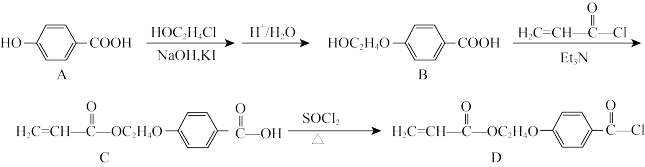
(1)A的分子式为____ ,其核磁共振氢谱有____ 组(个)峰。由A→B的转化过程中加入 的主要作用是
的主要作用是____ 。
(2)B不能 发生的反应是____ (填编号)。
①加成反应 ②取代反应 ③氧化反应 ④加聚反应
(3)写出C与足量NaOH溶液反应的最终产物的结构简式____ 。
(4)写出同时满足下列条件的A的2种同分异构体的结构简式____ 。
①属于醛类 ②能使FeCl3溶液显紫色
(5)写出以 为原料,经过两步化学反应制备
为原料,经过两步化学反应制备 的合成路线
的合成路线____ (其他试剂任选)。

(1)A的分子式为
 的主要作用是
的主要作用是(2)B
①加成反应 ②取代反应 ③氧化反应 ④加聚反应
(3)写出C与足量NaOH溶液反应的最终产物的结构简式
(4)写出同时满足下列条件的A的2种同分异构体的结构简式
①属于醛类 ②能使FeCl3溶液显紫色
(5)写出以
 为原料,经过两步化学反应制备
为原料,经过两步化学反应制备 的合成路线
的合成路线
您最近一年使用:0次
9 . 烟气脱硝(将NOx转化成无害物质)是工业废气处理中的重要工艺。相对传统的处理工艺,活性炭吸附脱硝法具有工艺过程无二次污染、氮资源和脱硝剂可循环利用等优点。回答下列问题。
(1)活性炭吸附脱硝法的工艺流程如图所示。
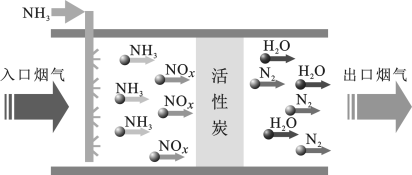
该流程中活性炭的作用是____ ,若入口烟气中NOx以NO形式参加反应,则相应的化学方程式为____ 。
(2)某同学选择如下装置(省略夹持仪器)对该方法进行模拟实验:

①实验前,按h→j,i→k的顺序连接仪器,检查装置____ 。按h→j而不是h→k连接仪器的原因是____ 。
②先通入空气,再打开A、B中分液漏斗的活塞,观察到B中出现红棕色气体,此时,所获得的氮氧化物中一定含有____ 气体。
③装置F除了能用于判断气体流速和脱硝效果外,还可用于____ 。
④为达到更好的脱硝效果,实验中应采取的措施有____ (任写两种)。
⑤常温常压下,以一定流速和比例混合NO、NH3、空气等气体进行模拟实验,现测得NO入口体积分数为3×10-4,出口体积分数为6×10-5,则脱硝百分率为____ %(因混合气体中NO所占比例很小,可忽略脱硝前后气体总体积的变化,计算结果保留小数点后1位)。
(1)活性炭吸附脱硝法的工艺流程如图所示。

该流程中活性炭的作用是
(2)某同学选择如下装置(省略夹持仪器)对该方法进行模拟实验:

①实验前,按h→j,i→k的顺序连接仪器,检查装置
②先通入空气,再打开A、B中分液漏斗的活塞,观察到B中出现红棕色气体,此时,所获得的氮氧化物中一定含有
③装置F除了能用于判断气体流速和脱硝效果外,还可用于
④为达到更好的脱硝效果,实验中应采取的措施有
⑤常温常压下,以一定流速和比例混合NO、NH3、空气等气体进行模拟实验,现测得NO入口体积分数为3×10-4,出口体积分数为6×10-5,则脱硝百分率为
您最近一年使用:0次
2020-12-17更新
|
175次组卷
|
2卷引用:广西壮族自治区2018年12月普通高中学业水平考试化学试题
名校
10 . W、X、Y、Z是汽车尾气中含有的4种主要元素。W元素原子核外只有1个电子;X是金刚石的组成元素;X、Y、Z是原子序数依次递增的同一短周期元素,这三种元素原子最外层电子数之和为15。
(1)W在元素周期表中的位置为____ 。
(2)X的最高价氧化物对应的水化物的化学式为____ 。
(3)Y与Z的原子半径大小关系为:Y____ Z(填“>”或“<”)。
(4)Y的气态氢化物稳定性比Z的气态氢化物稳定性____ (填“强”或“弱”)。
(1)W在元素周期表中的位置为
(2)X的最高价氧化物对应的水化物的化学式为
(3)Y与Z的原子半径大小关系为:Y
(4)Y的气态氢化物稳定性比Z的气态氢化物稳定性
您最近一年使用:0次
2020-12-17更新
|
180次组卷
|
2卷引用:广西壮族自治区2018年12月普通高中学业水平考试化学试题



