解题方法
1 . 电子工业中常用覆铜板为材料,利用FeCl3溶液做“腐蚀液”制作印刷电路板。从废腐蚀液(含FeCl3,FeCl2和CuCl2)中回收Cu并实现FeCl3溶液循环再利用,其工艺流程如下:

回答下列问题:
(1)工业上制作印刷电路板时发生的化学反应方程式为_______ 。
(2)操作方法①为_______ ,固体A的成分为_______ (填化学式)。
(3)实验室检验溶液A中是否含有FeCl3的试剂为_______ 溶液(填化学式)。
(4)溶液A中加入NaOH溶液时产生的实验现象为_______ 。
(5)若回收过程中取废腐蚀液V L,回收到a g Cu,则废腐蚀液中Cu2+的物质的量浓度为_______ mol/L(用含a和V的表达式表示)。

回答下列问题:
(1)工业上制作印刷电路板时发生的化学反应方程式为
(2)操作方法①为
(3)实验室检验溶液A中是否含有FeCl3的试剂为
(4)溶液A中加入NaOH溶液时产生的实验现象为
(5)若回收过程中取废腐蚀液V L,回收到a g Cu,则废腐蚀液中Cu2+的物质的量浓度为
您最近一年使用:0次
2 . 二氧化硫在食品加工中有着重要作用,但过量使用可能导致食品中残留量超标,会对人体健康造成不利影响。实验室可用下图装置制取并探究二氧化硫的性质。回答下列问题:

(1)①中试管内发生反应的化学方程式为_______ ,该反应中体现了浓H2SO4的酸性和_______ 性。在标准状况下生成224 mLSO2时,消耗的H2SO4的物质的量为_______ mol。
(2)实验过程中铜丝可以上下抽动,其作用为_______ 。
(3)②中试管内的溴水褪色,SO2表现出_______ 性,③中试管内的石蕊溶液出现的实验现象为_______ 。
(4)浸有NaOH溶液的棉团的作用为_______ 。

(1)①中试管内发生反应的化学方程式为
(2)实验过程中铜丝可以上下抽动,其作用为
(3)②中试管内的溴水褪色,SO2表现出
(4)浸有NaOH溶液的棉团的作用为
您最近一年使用:0次
解题方法
3 . 发酵法酿酒是我国古代劳动人民的智慧结晶,中国酒文化博大精深。下列有机物转化流程如下图所示:
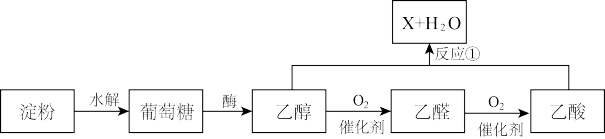
回答下列问题:
(1)葡萄糖的分子式为_______ ,葡萄糖在生命活动中的作用是_______ 。
(2)乙醇分子中官能团的名称为_______ 。
(3)X的结构简式为_______ ,反应①的反应类型为_______ 。
(4)乙醇转化为乙醛的化学方程式为_______ 。

回答下列问题:
(1)葡萄糖的分子式为
(2)乙醇分子中官能团的名称为
(3)X的结构简式为
(4)乙醇转化为乙醛的化学方程式为
您最近一年使用:0次
解题方法
4 . 元素周期表揭示了元素间的内在联系,使元素构成了一个较为系统的体系。下图为人们在研究元素间关系的过程中构建的一种表现形式,请你根据图中信息回答下列问题:
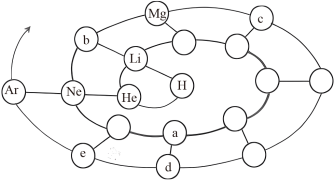
(1)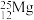 中含有的中子数为
中含有的中子数为_______ 。
(2)元素e的名称为_______ 。
(3)元素a和元素b的原子半径较大的为_______ (填元素符号)。
(4)元素a、d分别形成的简单氢化物中,稳定性较强的为_______ (填氢化物的化学式)。化合物 中化学键类型为
中化学键类型为_______ 。
(5)c单质与元素b的最高价氧化物对应的水化物的溶液反应的化学方程式为_______ 。

(1)
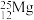 中含有的中子数为
中含有的中子数为(2)元素e的名称为
(3)元素a和元素b的原子半径较大的为
(4)元素a、d分别形成的简单氢化物中,稳定性较强的为
 中化学键类型为
中化学键类型为(5)c单质与元素b的最高价氧化物对应的水化物的溶液反应的化学方程式为
您最近一年使用:0次
名校
解题方法
5 . 我省地处东南沿海,海域面积大,海洋资源十分丰富,从海水中可提取多种化工原料。如图是某工厂利用海水提取铁的工业流程:请回答下列各题:
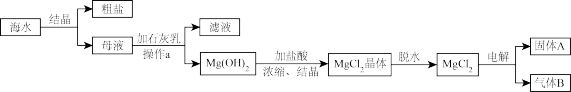
(1)操作a的名称是____ 。
(2)固体A是____ ,气体B是____ 。
(3)海水中的镁元素为____ (填“游离态”或“化合态”)。
(4)该过程中有无氧化还原反应____ (填“有”或“无”)。
(5)写出Mg(OH)2与盐酸反应的化学方程式:____ 。

(1)操作a的名称是
(2)固体A是
(3)海水中的镁元素为
(4)该过程中有无氧化还原反应
(5)写出Mg(OH)2与盐酸反应的化学方程式:
您最近一年使用:0次
名校
解题方法
6 . 某同学用下列各装置设计一个实验,验证氯气的性质。
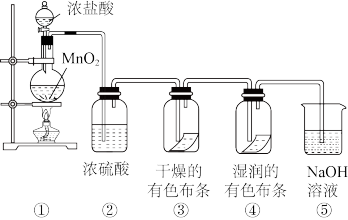
请回答:
(1)①中的化学方程式为____ ;②中浓硫酸的作用是____ 。
(2)③中的实验现象是____ ;④中的实验现象是___ ;上述实验现象说明起漂白作用的是____ (填分子式)。
(3)⑤中NaOH溶液的作用是吸收多余的氯气、防止污染大气,试写出反应的离子方程式:____ 。

请回答:
(1)①中的化学方程式为
(2)③中的实验现象是
(3)⑤中NaOH溶液的作用是吸收多余的氯气、防止污染大气,试写出反应的离子方程式:
您最近一年使用:0次
名校
解题方法
7 . 实验室制取乙酸乙酯的装置如图:
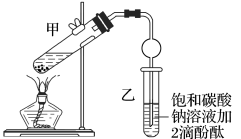
(1)配制该混合溶液的加入顺序为:(填入顺序对应的序号)____ 。
A.2mL浓硫酸 B.2mL乙酸 C.3mL乙醇
反应中浓硫酸的作用是_____ ;导管不深入液面以下的原因是____ 。
(2)写出制取乙酸乙酯的化学方程式____ 。
(3)上述实验中饱和碳酸钠溶液的作用是(填字母)____ 。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
(4)欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器有____ ;分离时,乙酸乙酯应该从仪器____ (填:“下口放”或“上口倒”)出。

(1)配制该混合溶液的加入顺序为:(填入顺序对应的序号)
A.2mL浓硫酸 B.2mL乙酸 C.3mL乙醇
反应中浓硫酸的作用是
(2)写出制取乙酸乙酯的化学方程式
(3)上述实验中饱和碳酸钠溶液的作用是(填字母)
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
(4)欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器有
您最近一年使用:0次
名校
解题方法
8 . 我国有广阔的海岸线,海水的综合利用大有可为。海水中溴含量约为65mg•L-1,从海水中提取溴的工艺流程如图所示。
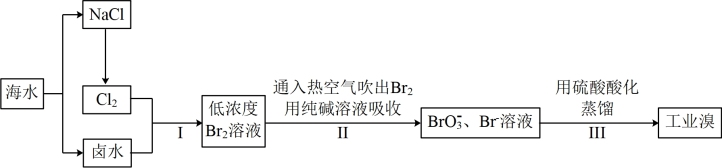
(1)步骤I、步骤III发生反应的离子反应方程式为____ 、____ 。
(2)步骤I中已获得游离态的溴,步骤II又将之转变成化合态的溴,其目的是____ 。
(3)步骤II通入热空气或水蒸气吹出Br2,利用了溴的____ 。(填性质)
(4)步骤II中涉及的离子反应如下,请在下面方框内填入适当的化学计量数。____
 Br2+
Br2+ CO
CO =
= BrO
BrO +
+ Br-+
Br-+ CO2↑
CO2↑
(5)步骤II中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出SO2与溴单质反应的离子方程式____ 。

(1)步骤I、步骤III发生反应的离子反应方程式为
(2)步骤I中已获得游离态的溴,步骤II又将之转变成化合态的溴,其目的是
(3)步骤II通入热空气或水蒸气吹出Br2,利用了溴的
(4)步骤II中涉及的离子反应如下,请在下面方框内填入适当的化学计量数。
 Br2+
Br2+ CO
CO =
= BrO
BrO +
+ Br-+
Br-+ CO2↑
CO2↑(5)步骤II中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出SO2与溴单质反应的离子方程式
您最近一年使用:0次
名校
9 . 已知A是石油化学工业重要的基本原料,在一定的条件下发生如图所示的转化关系,请完成下列空白。
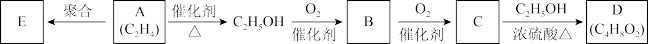
(1)A的结构简式为____ ,B的分子式为____ 。
(2)E的名称为____ ,C分子中的官能团是____ 。
(3)F(C3H6)是A的同系物,F发生加聚反应后,产物的结构简式可以表示为____ 。
(4)由C生成D的化学方程式为____ 。
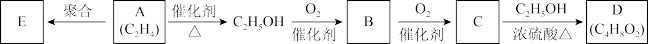
(1)A的结构简式为
(2)E的名称为
(3)F(C3H6)是A的同系物,F发生加聚反应后,产物的结构简式可以表示为
(4)由C生成D的化学方程式为
您最近一年使用:0次
10 . 已知反应: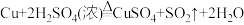 ,某化学兴趣小组用如图所示装置制取SO2,并进行相关性质实验。
,某化学兴趣小组用如图所示装置制取SO2,并进行相关性质实验。
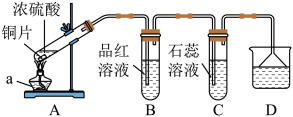
请回答下列问题:
(1)仪器a的名称是_______ ;
(2)B中品红溶液褪色,说明SO2具有_______ (填“漂白性”或“还原性”);
(3)C中石蕊溶液变为_______ (填“蓝色”或“红色”);
(4)为防止SO2污染环境,D中可选用_______ (填“NaOH”或“H2SO4”)溶液;
(5)酸性条件下,SO2与 发生如下反应:
发生如下反应: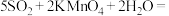
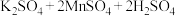 ,使溶液褪色。当
,使溶液褪色。当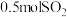 参加反应时,转移电子的物质的量是
参加反应时,转移电子的物质的量是_______ mol。
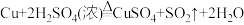 ,某化学兴趣小组用如图所示装置制取SO2,并进行相关性质实验。
,某化学兴趣小组用如图所示装置制取SO2,并进行相关性质实验。
请回答下列问题:
(1)仪器a的名称是
(2)B中品红溶液褪色,说明SO2具有
(3)C中石蕊溶液变为
(4)为防止SO2污染环境,D中可选用
(5)酸性条件下,SO2与
 发生如下反应:
发生如下反应: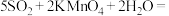
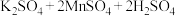 ,使溶液褪色。当
,使溶液褪色。当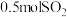 参加反应时,转移电子的物质的量是
参加反应时,转移电子的物质的量是
您最近一年使用:0次
2022-06-17更新
|
788次组卷
|
2卷引用:甘肃省天水市第一中学2021-2022学年高一下学期第一次学业水平检测化学试题



