解题方法
1 . 某同学用固体NaCl配制100mL2.0 NaCl溶液。回答下列问题:
NaCl溶液。回答下列问题:
(1)需要用托盘天平称取NaCl的质量为___________ 。
(2)下图所示的仪器中,不需使用的是___________ 。(填标号)___________ 。
(3)若固体放在托盘天平右盘称量,会导致所配溶液浓度___________ 。(填“偏高”或“偏低”)。
 NaCl溶液。回答下列问题:
NaCl溶液。回答下列问题:(1)需要用托盘天平称取NaCl的质量为
(2)下图所示的仪器中,不需使用的是

(3)若固体放在托盘天平右盘称量,会导致所配溶液浓度
您最近一年使用:0次
解题方法
2 . X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,X原子的L层电子数为5,Z单质与 在暗处能剧烈化合并发生爆炸,W与Y同主族。回答下列问题:
在暗处能剧烈化合并发生爆炸,W与Y同主族。回答下列问题:
(1)元素X为___________ (填名称),Y在元素周期表中的位置为___________ 。
(2)X、Z简单气态氢化物之间反应的化学方程式为___________ 。
(3)Y、W非金属性较强的是___________ (填元素符号);W简单气态氢化物的电子式为___________ 。
(4)Q的最高价氧化物对应水化物属于___________ (填“共价化合物”或“离子化合物”)。
 在暗处能剧烈化合并发生爆炸,W与Y同主族。回答下列问题:
在暗处能剧烈化合并发生爆炸,W与Y同主族。回答下列问题:(1)元素X为
(2)X、Z简单气态氢化物之间反应的化学方程式为
(3)Y、W非金属性较强的是
(4)Q的最高价氧化物对应水化物属于
您最近一年使用:0次
解题方法
3 . 丙烯( )是石油裂解气的主要成分之一,在一定条件下发生如图转化(部分产物及条件已略去):
)是石油裂解气的主要成分之一,在一定条件下发生如图转化(部分产物及条件已略去):
(1)丙烯中官能团的名称为___________ ;A自身发生加聚反应的产物为___________ 。
(2)丙烯与 在一定条件下反应生成B的反应类型为
在一定条件下反应生成B的反应类型为___________ 。
(3)丙烯与 在一定条件下反应生成C的化学方程式为
在一定条件下反应生成C的化学方程式为___________ 。
(4)下列化合物与D互为同分异构体的是___________ (填标号)。
 )是石油裂解气的主要成分之一,在一定条件下发生如图转化(部分产物及条件已略去):
)是石油裂解气的主要成分之一,在一定条件下发生如图转化(部分产物及条件已略去):
(1)丙烯中官能团的名称为
(2)丙烯与
 在一定条件下反应生成B的反应类型为
在一定条件下反应生成B的反应类型为(3)丙烯与
 在一定条件下反应生成C的化学方程式为
在一定条件下反应生成C的化学方程式为(4)下列化合物与D互为同分异构体的是
a. b.
b.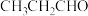 c.
c.
您最近一年使用:0次
解题方法
4 . 元素①~⑤在元素周期表中的位置如下表所示:
回答下列问题:
(1)原子半径最大的是___________ (填元素符号);简单离子半径最小的是___________ (填离子符号)。
(2)①、④简单气态氢化物的稳定性较强的是___________ (填化学式)。
(3)②、③最高价氧化物对应水化物之间反应的离子方程式为___________ 。
(4)④、⑤最高价氧化物对应水化物的酸性较强的是___________ (填化学式)。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ||||
(1)原子半径最大的是
(2)①、④简单气态氢化物的稳定性较强的是
(3)②、③最高价氧化物对应水化物之间反应的离子方程式为
(4)④、⑤最高价氧化物对应水化物的酸性较强的是
您最近一年使用:0次
5 . 某同学进行木炭和浓硫酸反应的实验,并验证产生的气体,装置图如图所示:

回答下列问题:
(1)仪器a的名称为_______ 。
(2)装置B中的现象为_______ ;装置C中的试剂为_______ ;装置D的作用为_______ 。
(3)装置E中发生反应的化学方程式为_______ 。

回答下列问题:
(1)仪器a的名称为
(2)装置B中的现象为
(3)装置E中发生反应的化学方程式为
您最近一年使用:0次
2023-06-05更新
|
301次组卷
|
3卷引用:2022年夏季山东普通高中学业水平考试化学试题
6 . 石蜡是由分子中碳原子数为17~36的多种烷烃或环烷烃组成的混合物。A的产量被用作衡量一个国家石油化工产业发展水平的标志,有关物质的转化关系如图所示(部分产物及条件已略去):
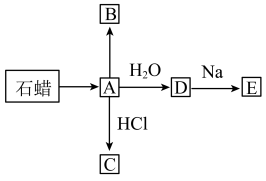
回答下列问题:
(1)石蜡→A为_______ (填“化学变化”或“物理变化”)。
(2)B为A发生加聚反应的产物,其结构简式为_______ ;A→C的反应类型为_______ 。
(3)D中官能团的名称为_______ ;E为气体,其化学式为_______ 。

回答下列问题:
(1)石蜡→A为
(2)B为A发生加聚反应的产物,其结构简式为
(3)D中官能团的名称为
您最近一年使用:0次
2023-06-05更新
|
158次组卷
|
2卷引用:2022年夏季山东普通高中学业水平考试化学试题
7 . 利用图示可以从不同角度研究含氮物质的性质及其转化关系。

回答下列问题:
(1)a溶于水所得溶液呈_______ (填“酸性”或“碱性”)。
(2)a与e反应生成的化合物为_______ (填化学式),该化合物属于_______ (填“共价化合物”或“离子化合物”)。
(3)b→c的化学方程式为_______ 。
(4)d的化学式为_______ 。

回答下列问题:
(1)a溶于水所得溶液呈
(2)a与e反应生成的化合物为
(3)b→c的化学方程式为
(4)d的化学式为
您最近一年使用:0次
2023-06-05更新
|
325次组卷
|
4卷引用:2022年夏季山东普通高中学业水平考试化学试题
8 . 元素①~⑤在元素周期表中的位置如表所示:
回答下列问题:
(1)原子半径最大的是_______ (填元素符号);简单离子半径最小的是_______ (填离子符号)。
(2)①、④简单气态氢化物的稳定性较强的是_______ (填化学式)。
(3)②、③最高价氧化物对应水化物之间反应的离子方程式为_______ 。
(4)④、⑤最高价氧化物对应水化物的酸性较强的是_______ (填化学式)。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ||||
(1)原子半径最大的是
(2)①、④简单气态氢化物的稳定性较强的是
(3)②、③最高价氧化物对应水化物之间反应的离子方程式为
(4)④、⑤最高价氧化物对应水化物的酸性较强的是
您最近一年使用:0次
9 . X、Y、Z、W、Q均为短周期主族元素。X是原子半径最小的元素;Y是地壳中含量最高的元素;Z是非金属性最强的元素,Z和W同主族;Q是短周期金属性最强的元素。回答下列问题:
(1)X与W形成化合物的电子式为_______ ;Y在元素周期表中的位置为_______ 。
(2) 属于
属于_______ (填“共价化合物”或“离子化合物”)。
(3)Z、W简单气态氢化物稳定性较强的是_______ (填化学式)。
(4)W、Q最高价氧化物对应水化物之间W、Q最高价氧化物对应水化物为_______ 。
(1)X与W形成化合物的电子式为
(2)
 属于
属于(3)Z、W简单气态氢化物稳定性较强的是
(4)W、Q最高价氧化物对应水化物之间W、Q最高价氧化物对应水化物为
您最近一年使用:0次
名校
解题方法
10 . I.锂电池有广阔的应用前景。用“循环电沉积”法处理某种锂电池,可使其中的Li电极表面生成只允许Li+通过的Li2CO3和C保护层,工作原理如图1,具体操作如下。
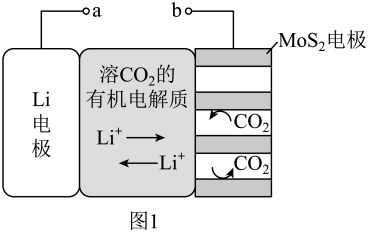
i.将表面洁净的Li电极和MoS2电极浸在溶有CO2的有机电解质溶液中。
ii.0~5min,a端连接电源正极,b端连接电源负极,电解,MoS2电极上生成Li2CO3和C。
iii.5~10min,a端连接电源负极,b端连接电源正极,电解,MoS2电极上消耗Li2CO3和C,Li电极上生成Li2CO3和C。
步骤ii和步骤iii为1个电沉积循环。
iv.重复步骤ii和步骤iii的操作,继续完成9个电沉积循环。
(1)步骤ii内电路中的Li+的迁移方向为____ 。
a.由Li电极向MoS2电极迁移 b.由MoS2电极向Li电极迁移
(2)已知下列反应的热化学方程式。
2Li(s)+2CO2(g)=Li2CO3(s)+CO(g) ΔH1=-539kJ•mol-1
CO2(g)+C(s)=2CO(g) ΔH2=+172kJ•mol-1
步骤ii电解总反应的热化学方程式为____ 。
(3)步骤iii中,Li电极的电极反应式为____ 。
(4)Li2CO3和C只有在MoS2的催化作用下才能发生步骤iii的电极反应,反应历程中的能量变化如图。下列说法正确的是____ (填字母)。

a.反应历程中存在碳氧键的断裂和形成
b.反应历程中涉及电子转移的变化均释放能量
c.MoS2催化剂通过降低电极反应的活化能使反应速率增大
II.如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。

(5)①腐蚀过程中,负极是____ (填“a”“b”或“c”)。
②环境中的Cl-扩散到孔口,并与正极产物和负极产物作用生成多孔铜锈Cu2(OH)3Cl,其离子方程式为_____ 。
③若生成4.29gCu2(OH)3Cl,则理论上消耗氧气的体积为____ L(标准状况)。

i.将表面洁净的Li电极和MoS2电极浸在溶有CO2的有机电解质溶液中。
ii.0~5min,a端连接电源正极,b端连接电源负极,电解,MoS2电极上生成Li2CO3和C。
iii.5~10min,a端连接电源负极,b端连接电源正极,电解,MoS2电极上消耗Li2CO3和C,Li电极上生成Li2CO3和C。
步骤ii和步骤iii为1个电沉积循环。
iv.重复步骤ii和步骤iii的操作,继续完成9个电沉积循环。
(1)步骤ii内电路中的Li+的迁移方向为
a.由Li电极向MoS2电极迁移 b.由MoS2电极向Li电极迁移
(2)已知下列反应的热化学方程式。
2Li(s)+2CO2(g)=Li2CO3(s)+CO(g) ΔH1=-539kJ•mol-1
CO2(g)+C(s)=2CO(g) ΔH2=+172kJ•mol-1
步骤ii电解总反应的热化学方程式为
(3)步骤iii中,Li电极的电极反应式为
(4)Li2CO3和C只有在MoS2的催化作用下才能发生步骤iii的电极反应,反应历程中的能量变化如图。下列说法正确的是

a.反应历程中存在碳氧键的断裂和形成
b.反应历程中涉及电子转移的变化均释放能量
c.MoS2催化剂通过降低电极反应的活化能使反应速率增大
II.如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。

(5)①腐蚀过程中,负极是
②环境中的Cl-扩散到孔口,并与正极产物和负极产物作用生成多孔铜锈Cu2(OH)3Cl,其离子方程式为
③若生成4.29gCu2(OH)3Cl,则理论上消耗氧气的体积为
您最近一年使用:0次
2022-10-19更新
|
212次组卷
|
2卷引用:山东省2022-2023学年高二上学期学业水平测试化学试题



