名校
解题方法
1 . 氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)NH3的电子式______ 。
(2)氯化铵水溶液显酸性,其原因为______ (用离子方程式表示),0.1mol/L的氨水中加入少量的NH4Cl固体,溶液的pH______ (填“升高”或“降低”);若加入少量的明矾固体后,请尝试从平衡移动的角度解释溶液中NH4+浓度的变化原因______ 。
(3)硝酸铵加热分解可得到N2O(g)和H2O(g),250℃时,硝酸铵在密闭容器中分解达到平衡,该温度下反应的平衡常数表达式为______ ;若有1mol硝酸铵完全分解,转移的电子数为______ mol。
(4)3H2(g)+N2(g)⇌2NH3(g)△H=-92kJ/mol,若反应放出9.2kJ 热量,则参加反应的氢气分子数目为______ 。
(1)NH3的电子式
(2)氯化铵水溶液显酸性,其原因为
(3)硝酸铵加热分解可得到N2O(g)和H2O(g),250℃时,硝酸铵在密闭容器中分解达到平衡,该温度下反应的平衡常数表达式为
(4)3H2(g)+N2(g)⇌2NH3(g)△H=-92kJ/mol,若反应放出9.2kJ 热量,则参加反应的氢气分子数目为
您最近一年使用:0次
2020-04-27更新
|
110次组卷
|
3卷引用:重庆市2019-2020学年高二普通高中学业水平合格性模拟考试化学试题
2 . (1)相同物质的量浓度的①CH3COOH 溶液,②盐酸,c(H+)较大的是____________ (填编号);CH3COOH 的电离方程式为____________ 。
(2)FeCl3溶液保存时需加少量____________ (填“盐酸”或“硫酸”)。
(3)甲醇 CH3OH 是一种重要的化工原料,在生产中有着广泛的应用。合成 CH3OH 的一种 反应为:CO(g) + 2H2(g) CH3OH (g)。一定条件下,将 1 mol CO 和 2 mol H2在 1L 容器中发生上述反应,经过 2 min 反应生成了 a mol CH3OH(反应前后体积不变)。
CH3OH (g)。一定条件下,将 1 mol CO 和 2 mol H2在 1L 容器中发生上述反应,经过 2 min 反应生成了 a mol CH3OH(反应前后体积不变)。
①此时 CO 的浓度为____________ mol/L 。
②2min 内用 H2 表示该反应的速率为 v(H2) =____________ mol/(L·min)。
③升高温度,反应的平衡常数 K 减小,则该反应为____________ (填“吸热反应”或“放热反应”)。
(2)FeCl3溶液保存时需加少量
(3)甲醇 CH3OH 是一种重要的化工原料,在生产中有着广泛的应用。合成 CH3OH 的一种 反应为:CO(g) + 2H2(g)
 CH3OH (g)。一定条件下,将 1 mol CO 和 2 mol H2在 1L 容器中发生上述反应,经过 2 min 反应生成了 a mol CH3OH(反应前后体积不变)。
CH3OH (g)。一定条件下,将 1 mol CO 和 2 mol H2在 1L 容器中发生上述反应,经过 2 min 反应生成了 a mol CH3OH(反应前后体积不变)。 ①此时 CO 的浓度为
②2min 内用 H2 表示该反应的速率为 v(H2) =
③升高温度,反应的平衡常数 K 减小,则该反应为
您最近一年使用:0次
3 . 氨是一种重要的化工产品,也是重要的化工原料。某化学小组在实验室制备氨并完成相关性质实验。
(1)实验一:用如图所示装置制备并收集 NH3。
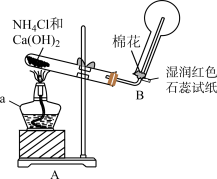
仪器 a 的名称为____________ ,装置 A 中产生 NH3的化学方程式为____________ , 装置 B 中用圆底烧瓶收集 NH3的方法为____________ (填“向上排空气法”或“向下 排空气法”),当湿润红色石蕊试纸颜色变为____________ 色,表示已经收集满 NH3。
(2)实验二:用如图所示装置进行 NH3的喷泉实验。
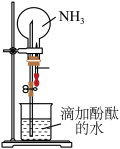
引发该喷泉实验的操作是先____________ ,再打开止水夹,使烧杯内的水通过导管进入烧瓶形成喷泉,说明 NH3具有的物理性质是____________ ,烧瓶内溶液呈红色, 说明 NH3的水溶液呈____________ 性。
(1)实验一:用如图所示装置制备并收集 NH3。

仪器 a 的名称为
(2)实验二:用如图所示装置进行 NH3的喷泉实验。

引发该喷泉实验的操作是先
您最近一年使用:0次



