1 . 丙酮的溴代反应(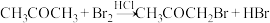 )的速率方程为:
)的速率方程为: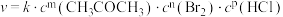 ,其中k为速率常数,与温度有关;“
,其中k为速率常数,与温度有关;“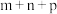 ”为反应级数。某温度时,获得如下实验数据:
”为反应级数。某温度时,获得如下实验数据:
分析该组实验数据所得出的结论错误的是
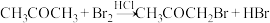 )的速率方程为:
)的速率方程为: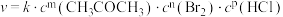 ,其中k为速率常数,与温度有关;“
,其中k为速率常数,与温度有关;“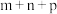 ”为反应级数。某温度时,获得如下实验数据:
”为反应级数。某温度时,获得如下实验数据:| 实验序号 | 初始浓度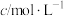 | 溴颜色消失所需时间t/s | ||
 | HCl |  | ||
| ① | 0.80 | 0.20 | 0.0010 | 200 |
| ② | 1.60 | 0.20 | 0.0010 | 100 |
| ③ | 0.80 | 0.40 | 0.0010 | 100 |
| ④ | 0.80 | 0.20 | 0.0020 | 400 |
A.增大 ,能延长溶液颜色消失的时间 ,能延长溶液颜色消失的时间 |
| B.实验②和③的平均速率相等 |
C.实验①在200s内的平均速率 |
| D.反应级数为2 |
您最近一年使用:0次
解题方法
2 . 下图是某同学用500mL容量瓶配制0.10mol·L-1NaOH溶液的过程:
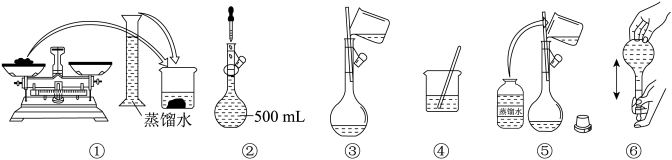
下列关于该实验的叙述正确的是

下列关于该实验的叙述正确的是
| A.如图所示,用托盘直接称量2.0g烧碱 |
| B.配制的正确顺序为①④③⑤②⑥ |
| C.②中定容时仰视刻线会导致溶液浓度偏低 |
| D.能用容量瓶贮存配制好的溶液 |
您最近一年使用:0次
3 . 下列有关电极反应的书写中,错误的是
A.氯碱工业电解装置中,阳极的电极反应: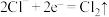 |
B.粗铜精炼时,阴极的电极反应: |
C.钢铁发生电化学腐蚀时,负极的电极反应: |
| D.碱性氢氧燃料电池,正极的电极反应:O2+2H2O+4e-=4OH- |
您最近一年使用:0次
名校
解题方法
4 . 硫元素的几种化合物及其单质存在下列转化关系(反应条件省略)。

下列判断不正确的是

下列判断不正确的是
A.反应①中氧化剂与还原剂物质的量之比为 |
B.反应②表明 具有酸性氧化物的性质 具有酸性氧化物的性质 |
| C.反应③的原子利用率是100% |
D.反应④中稀 是氧化剂 是氧化剂 |
您最近一年使用:0次
2023-12-27更新
|
255次组卷
|
9卷引用:辽宁省锦州市2019-2020学年高一下学期期末考试化学试题
辽宁省锦州市2019-2020学年高一下学期期末考试化学试题(已下线)5.1.3 不同价态含硫物质的转化-2021-2022学年高一化学课后培优练(人教版2019必修第二册)湖北省竹山县第二中学2021-2022学年高一下学期第一次月考化学试题浙江省玉环市玉城中学2021-2022学年高一下学期开学考试化学试题第五章 化工生产中的重要非金属元素(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)(已下线)第01练 硫及其化合物-2023年【暑假分层作业】高一化学(人教版2019必修第二册)第3课时 不同价态含硫物质的转化山东省菏泽市第一中学2023-2024学年高一上学期第三次月考化学试题山东省菏泽市曹县第一中学2023-2024学年高一上学期 月考化学试题
名校
解题方法
5 . 取未知浓度的硫酸、盐酸和醋酸各25.00mL,分别用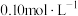 的NaOH溶液或
的NaOH溶液或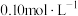 的稀氨水滴定得到下图所示曲线。下列说法不正确的是
的稀氨水滴定得到下图所示曲线。下列说法不正确的是
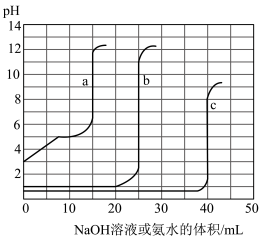
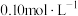 的NaOH溶液或
的NaOH溶液或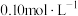 的稀氨水滴定得到下图所示曲线。下列说法不正确的是
的稀氨水滴定得到下图所示曲线。下列说法不正确的是
| A.由图可知曲线c为NaOH滴定硫酸 |
| B.由图可知可求出硫酸的物质的量浓度小于盐酸的物质的量浓度 |
| C.曲线b、c的滴定实验可用酚酞作指示剂 |
| D.由图可知滴定前醋酸电离百分比约为1.67% |
您最近一年使用:0次
名校
解题方法
6 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅等的氧化物,从铬钒渣中分离提取铬和钒的一种流程如图所示。下列说法正确的是
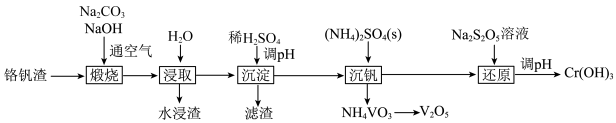
已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
② 。
。

已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
②
 。
。A.“煅烧”后的含铬化合物是 |
B.“滤渣”中只含有 |
C.“沉钒”时 固体可增大 固体可增大 的浓度,有利于沉淀的生成 的浓度,有利于沉淀的生成 |
D.“还原”工序中氧化剂和还原剂的物质的量之比为 |
您最近一年使用:0次
2023-12-03更新
|
385次组卷
|
2卷引用:辽宁省沈阳市第一二0中学2023-2024学年高三上学期第五次质量监测化学试题
名校
解题方法
7 . NH3可消除NO的污染,反应方程式为:6NO+ 4NH3=5N2+6H2O。现有NO与NH3的混合物共1 mol充分反应,若氧化产物与还原产物质量相差1.4g,则下列判断中正确的是
| A.氧化产物与还原产物物质的量之比为3:2 |
| B.反应中有0.2mol NH3被氧化 |
| C.转移电子数为1.2NA |
| D.原混合气体中NO、NH3物质的量之比为3:7或4:1 |
您最近一年使用:0次
解题方法
8 . 下列电离方程式中正确的是
A.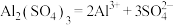 | B. |
C.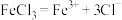 | D. |
您最近一年使用:0次
9 . 已知可逆反应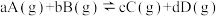 ,在其他条件不变时,C的物质的量分数随温度(T)或压强(P)的变化如下图所示,下列说法正确的是
,在其他条件不变时,C的物质的量分数随温度(T)或压强(P)的变化如下图所示,下列说法正确的是
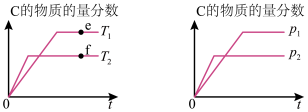
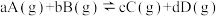 ,在其他条件不变时,C的物质的量分数随温度(T)或压强(P)的变化如下图所示,下列说法正确的是
,在其他条件不变时,C的物质的量分数随温度(T)或压强(P)的变化如下图所示,下列说法正确的是
| A.反应达到平衡后,添加合适的催化剂,D的百分含量增加 |
B.e、f点对应的化学反应速率: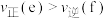 |
C.平衡常数K: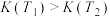 , ,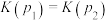 |
D. , ,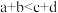 |
您最近一年使用:0次
名校
10 . 2 L恒容密闭容器中通入A、B各10 mol,在一定温度下进行反应:3A(g)+B(g)⇌2C(g)+2D(s),ΔH<0,4 min时达到平衡,生成4 mol D。下列说法不正确的是
| A.①体系气体密度不变;②A的体积分数不变;③2v逆(A)=3v正(C),三种现象均可以说明该反应达到平衡 |
| B.①增加D的质量;②向体系中充入He;③抽出A减小体系压强,三种操作都不能增大逆反应速率 |
| C.4 min末时,C的平均反应速率为0.5 mol·L-1·min-1 |
| D.保持温度不变,起始时四种物质的物质的量均为6 mol,则此时反应v正(A) < v逆(A) |
您最近一年使用:0次



