1 . 25℃时,草酸的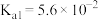 ,
, 。下列说法正确的是
。下列说法正确的是
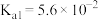 ,
, 。下列说法正确的是
。下列说法正确的是A.  溶液中: 溶液中: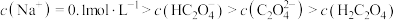 |
B.向 的 的 溶液中通入 溶液中通入 气体(忽略溶液体积的变化)至 气体(忽略溶液体积的变化)至 ,溶液 ,溶液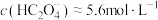 |
C.向 溶液中加入 溶液中加入 溶液至 溶液至 ,则 ,则 |
D.取 的 的 溶液10mL,加蒸馏水稀释至100mL,则该溶液 溶液10mL,加蒸馏水稀释至100mL,则该溶液 |
您最近一年使用:0次
2 . 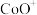 与
与 、
、 反应能高选择性地生成甲醇(氢元素有H、D、T三种同位素,直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢),体系的能量随反应进程的变化如图所示(两者历程相似)。下列分析错误的是
反应能高选择性地生成甲醇(氢元素有H、D、T三种同位素,直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢),体系的能量随反应进程的变化如图所示(两者历程相似)。下列分析错误的是
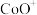 与
与 、
、 反应能高选择性地生成甲醇(氢元素有H、D、T三种同位素,直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢),体系的能量随反应进程的变化如图所示(两者历程相似)。下列分析错误的是
反应能高选择性地生成甲醇(氢元素有H、D、T三种同位素,直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢),体系的能量随反应进程的变化如图所示(两者历程相似)。下列分析错误的是
A.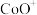 与 与 反应的能量变化应为曲线n 反应的能量变化应为曲线n |
| B.步骤Ⅰ既涉及碳氢键的断裂也涉及氧氢键的形成 |
C.若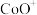 与 与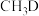 反应,可能生成 反应,可能生成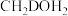 、 、 和 和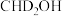 三种氚代甲醇 三种氚代甲醇 |
D.若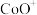 与 与 反应,相同时间内氚代甲醇的产量: 反应,相同时间内氚代甲醇的产量: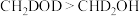 |
您最近一年使用:0次
3 . 一种将苯酚( )氧化为
)氧化为 的原电池—电解池组合装置如图所示(
的原电池—电解池组合装置如图所示( 是自然界中氧化性仅次于氟的氧化剂),该装置能实现发电、环保二位一体。下列说法正确的是
是自然界中氧化性仅次于氟的氧化剂),该装置能实现发电、环保二位一体。下列说法正确的是
 )氧化为
)氧化为 的原电池—电解池组合装置如图所示(
的原电池—电解池组合装置如图所示( 是自然界中氧化性仅次于氟的氧化剂),该装置能实现发电、环保二位一体。下列说法正确的是
是自然界中氧化性仅次于氟的氧化剂),该装置能实现发电、环保二位一体。下列说法正确的是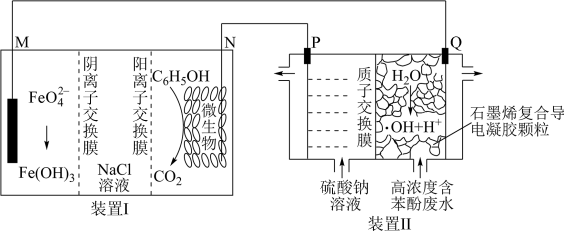
| A.装置Ⅰ为电解池,Ⅱ为原电池,M电极为阴极 |
B.一段时间后,装置Ⅰ中“ 溶液”浓度降低 溶液”浓度降低 |
C.装置Ⅱ,废水中每除掉 苯酚,消耗 苯酚,消耗 的质量为47.6g 的质量为47.6g |
| D.相同条件下,N电极和P电极产生的气体体积之比为4:7 |
您最近一年使用:0次
4 . 1,6—烯炔类化合物在膦配位的铑催化剂的作用下,可进行不对称环化异构,生成五元杂环化合物,反应如下。下列说法正确的是

甲 乙
| A.甲和乙均不存在手性碳原子 | B.甲中所有碳原子不可能共平面 |
| C.可用新制银氨溶液鉴别甲和乙 | D.甲的同分异构体中苯环上有5个取代基的共有6种 |
您最近一年使用:0次
解题方法
5 . 已知橙红色的配离子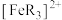 可被
可被 氧化成淡蓝色的配离子
氧化成淡蓝色的配离子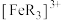 (
( 的还原产物是
的还原产物是 ),现用浓度分别为
),现用浓度分别为 、
、 、
、 的
的 溶液进行实验,
溶液进行实验,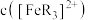 随时间
随时间 的变化曲线如图所示。下列有关说法错误的是
的变化曲线如图所示。下列有关说法错误的是
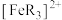 可被
可被 氧化成淡蓝色的配离子
氧化成淡蓝色的配离子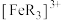 (
( 的还原产物是
的还原产物是 ),现用浓度分别为
),现用浓度分别为 、
、 、
、 的
的 溶液进行实验,
溶液进行实验,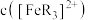 随时间
随时间 的变化曲线如图所示。下列有关说法错误的是
的变化曲线如图所示。下列有关说法错误的是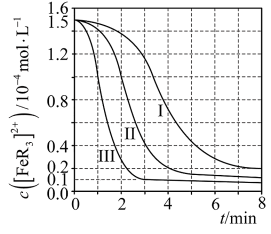
A.实验中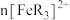 、 、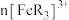 之和不变时,反应达到平衡状态 之和不变时,反应达到平衡状态 |
| B.三组实验中,反应速率都是前期速率增加,后期速率减小 |
C. 的硝酸进行实验,平衡时 的硝酸进行实验,平衡时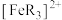 的平均消耗速率为 的平均消耗速率为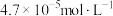 |
D.平衡后加水稀释, 增大 增大 |
您最近一年使用:0次
6 . Y是一种降血脂药物,合成路线片段如图所示:
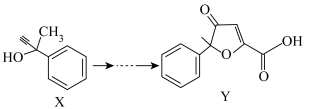
| A.X中所有碳原子可能共平面 |
| B.X能发生消去反应 |
| C.Y中含有2个手性碳原子 |
D.1molY最多能与5mol 发生加成反应 发生加成反应 |
您最近一年使用:0次
7 . 氟硼酸铵( )易溶于水,溶液呈酸性,可用作铝、铜和铝合金焊接助熔剂。
)易溶于水,溶液呈酸性,可用作铝、铜和铝合金焊接助熔剂。 与HF反应后再用
与HF反应后再用 中和得到
中和得到 。下列叙述正确的是
。下列叙述正确的是
 )易溶于水,溶液呈酸性,可用作铝、铜和铝合金焊接助熔剂。
)易溶于水,溶液呈酸性,可用作铝、铜和铝合金焊接助熔剂。 与HF反应后再用
与HF反应后再用 中和得到
中和得到 。下列叙述正确的是
。下列叙述正确的是A.HF、 都是由极性键构成的极性分子 都是由极性键构成的极性分子 |
B.1mol 中含有配位键的数目为 中含有配位键的数目为 |
C. 与 与 的VSEPR模型相同 的VSEPR模型相同 |
D.推测 可与HF反应生成 可与HF反应生成 |
您最近一年使用:0次
解题方法
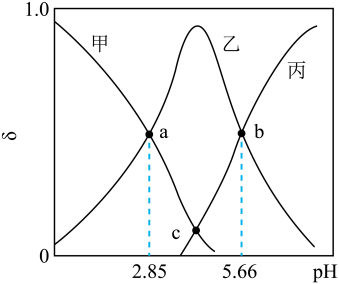
8 . 25℃时,向一定浓度二元弱酸 溶液[
溶液[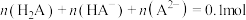 ]中滴加NaOH溶液,滴加过程中,溶液中
]中滴加NaOH溶液,滴加过程中,溶液中 、
、 、
、 的分布系数与pH的关系如图所示。已知分布系数
的分布系数与pH的关系如图所示。已知分布系数 (其中X分别代表
(其中X分别代表 、
、 、
、 )。
)。
 溶液[
溶液[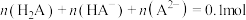 ]中滴加NaOH溶液,滴加过程中,溶液中
]中滴加NaOH溶液,滴加过程中,溶液中 、
、 、
、 的分布系数与pH的关系如图所示。已知分布系数
的分布系数与pH的关系如图所示。已知分布系数 (其中X分别代表
(其中X分别代表 、
、 、
、 )。
)。
A.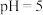 时, 时,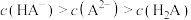 |
B.c点时溶液中 的物质的量恰好为0.1mol 的物质的量恰好为0.1mol |
C.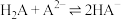 的化学平衡常数 的化学平衡常数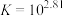 |
| D.b点溶液中水的电离受到促进 |
您最近一年使用:0次
9 . 用铁泥(主要成分为Fe2O3,还含有少量FeO和Fe)制备纳米Fe3O4的流程如下。下列说法正确的是

| A.步骤②④发生的反应均为氧化还原反应 |
| B.步骤②中发生的反应为2Fe3++Fe = 3Fe2+、Fe+2H+ = Fe2++H2↑ |
| C.步骤④中使用过量的H2O2有利于提高纳米Fe3O4产率 |
| D.纳米Fe3O4能产生丁达尔效应 |
您最近一年使用:0次
解题方法
10 . 下列反应的离子方程式书写正确的是
| A.铜和硫酸溶液反应:Cu + 2H+ = Cu2++H2↑ |
| B.氯化铁溶液与氢氧化钡溶液反应:Fe3++ 3OH-= Fe(OH)3↓ |
| C.铁与稀盐酸反应:Fe+2H+=Fe3++H2↑ |
| D.醋酸除水垢:2CH3COOH+CaCO3=2CH3COO﹣+Ca2++CO2↑+H2O |
您最近一年使用:0次



