解题方法
1 . N元素的单质及其化合物之间的转化关系如图所示:
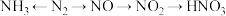
回答下列问题:
(1)N元素在元素周期表中的位置为__________ ,画出N原子结构示意图_________ 。
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式_____________ 。
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学方程式___________
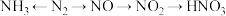
回答下列问题:
(1)N元素在元素周期表中的位置为
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学方程式
您最近一年使用:0次
2 . N元素的单质及其化合物之间的转化关系如图所示:NH3←N2→NO→NO2→HNO3
回答下列问题:
(1)N元素在元素周期表中的位置为第___ 周期,第___ 族;画出N原子结构示意图___ 。
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式___ 。
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学反应方程式___ ;并写出实验室检验氨气的具体操作___ 。
(4)NO是治疗心血管疾病的信使分子,NO与空气接触的反应现象是___ ,写出该反应的化学方程式___ ,若该反应转移0.4mole-,则消耗的NO分子数是___ (用NA表示阿伏加 德罗常数)。
(5)浓硝酸具有不稳定性,实验室应该将浓硝酸保存在带玻璃塞的___ (填“无色”或“棕色”)试剂瓶中。
回答下列问题:
(1)N元素在元素周期表中的位置为第
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学反应方程式
(4)NO是治疗心血管疾病的信使分子,NO与空气接触的反应现象是
(5)浓硝酸具有不稳定性,实验室应该将浓硝酸保存在带玻璃塞的
您最近一年使用:0次
名校
解题方法
3 . A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
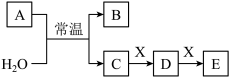
(1)若A为常见的金属单质,焰色试验呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:__ 。证明D已经氧化变质的方法是:取少量D固体溶于水中,__ 。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强。该元素在元素周期表中的位置为__ ,则X可能为__ (填代号)。
a.NaHCO3 b.Na2CO3 c.Fe(OH)3 d.NaAlO2
(3)若A为淡黄色粉末,则A的电子式为__ 。若X为一种最常见的造成温室效应的气体。若鉴别等浓度的D、E两种溶液,可选择的试剂为__ (填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为__ ,E是__ (填化学式)。

(1)若A为常见的金属单质,焰色试验呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强。该元素在元素周期表中的位置为
a.NaHCO3 b.Na2CO3 c.Fe(OH)3 d.NaAlO2
(3)若A为淡黄色粉末,则A的电子式为
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为
您最近一年使用:0次
名校
解题方法
4 . 元素X、Y、Z、M、N均为原子序数依次增大的短周期主族元素;R在地壳金属元素中的含量仅次于Z。已知Y原子最外层电子数与核外电子总数之比为3∶4,M原子的最外层电子数与次外层电子数之比为3∶4;N-、Z3+、X+离子半径逐渐减小;化合物XN常温下为气体,请回答下列问题:
(1)R在元素周期表中的位置是____________ ;Z3+的离子结构示意图是____________ 。
(2)写出X、Y、N按原子个数之比1∶1∶1形成的化合物的电子式___________ ;M和N气态氢化物的稳定性大小比较为________ (用化学式和“>”“<”或“=”表示)。
(3)Z元素的单质能与Y和R形成的红棕色化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为__________ 。
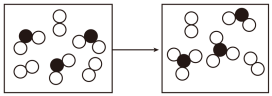
(4)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,在该转化关系中还原剂是___________ (填化学式),示意图中转移电子的数目为_________ 。
(5)由X、Y、M三种元素组成的离子,在水溶液中与H+和OH-均不能大量共存,它能和氯水反应,写出其与新制氯水反应的离子方程式_________ 。
(1)R在元素周期表中的位置是
(2)写出X、Y、N按原子个数之比1∶1∶1形成的化合物的电子式
(3)Z元素的单质能与Y和R形成的红棕色化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为
(4)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,在该转化关系中还原剂是

(5)由X、Y、M三种元素组成的离子,在水溶液中与H+和OH-均不能大量共存,它能和氯水反应,写出其与新制氯水反应的离子方程式
您最近一年使用:0次
名校
解题方法
5 . 元素周期表是学习和研究化学的重要工具。
(1)原子序数为 1~18 的元素在元素周期表中的位置如下表所示。
①Al原子的核电荷数为____ 。②钠离子的结构示意图为____ 。
③周期表中磷元素的有关信息为 ,图中“30.97”所表示的含义是
,图中“30.97”所表示的含义是____ 。
(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价﹣物质类别”关系图。
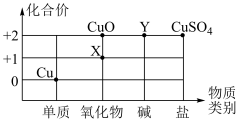
①写出物质 X 的化学式:________________ 。
②写出由物质 Y 转化为 CuSO4的化学反应方程式:_______________ 。
③氧化还原反应是化学学习中的核心概念,对氧化还原反应的定义为有化合价升降的反应,下列转化中属于氧化还原反应的是_________________ 。
A、Cu—X B、X—CuO C、CuO—Y D、Y—CuSO4
(1)原子序数为 1~18 的元素在元素周期表中的位置如下表所示。
| 第1周期 | H | He | ||||||
| 第2周期 | Li | Be | B | C | N | O | F | Ne |
| 第3周期 | Na | Mg | Al | Si | P | S | Cl | Ar |
①Al原子的核电荷数为
③周期表中磷元素的有关信息为
 ,图中“30.97”所表示的含义是
,图中“30.97”所表示的含义是(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价﹣物质类别”关系图。

①写出物质 X 的化学式:
②写出由物质 Y 转化为 CuSO4的化学反应方程式:
③氧化还原反应是化学学习中的核心概念,对氧化还原反应的定义为有化合价升降的反应,下列转化中属于氧化还原反应的是
A、Cu—X B、X—CuO C、CuO—Y D、Y—CuSO4
您最近一年使用:0次
解题方法
6 . X、Y、Z、W 是原子序数依次增大的短周期元素,Y 和W同主族,且X、Z原子序数之和是Y、W原子序数之和的 。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
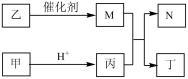
(1)W在元素周期表中的位置是_______________________ 。
(2)Y、Z、W的离子半径由大到小的顺序为__________ (用元素符号表示)。
(3)写出乙的电子式_____________ ,M 的结构式_____________________ 。
(4)丁与H2S相比沸点高的是_______ (用化学式表示);原因是_______________ 。
(5)N 与乙烯均能使酸性 KMnO4溶液褪色,原理______________ (填“相同”或“不相同”);N使酸性KMnO4溶液褪色的离子方程式为 ________________________ 。
 。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
(1)W在元素周期表中的位置是
(2)Y、Z、W的离子半径由大到小的顺序为
(3)写出乙的电子式
(4)丁与H2S相比沸点高的是
(5)N 与乙烯均能使酸性 KMnO4溶液褪色,原理
您最近一年使用:0次
名校
解题方法
7 . N元素的单质及其化合物之间的转化关系:NH3N2NO NO2HNO3。回答下列问题:
(1)N元素在元素周期表中的位置为_______ ;
(2)上述四种气体只能用排水法收集的是_______ (填化学式,下同),只能用排空气法收集的是______ ;
(3)氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是_____ ;
A. 酸雨 B. 光化学烟雾 C. 白色污染 D. 臭氧层空洞
(4)NO2形成酸雨的化学方程式为______ ;
(5)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程______ ;
(6)若将12.8 g铜与 50 mL一定浓度的浓硝酸反应,两者恰好完全反应共产生气体5.6 L(标准状况),计算此浓硝酸的物质的量浓度_______ (写出解题过程)。
(1)N元素在元素周期表中的位置为
(2)上述四种气体只能用排水法收集的是
(3)氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是
A. 酸雨 B. 光化学烟雾 C. 白色污染 D. 臭氧层空洞
(4)NO2形成酸雨的化学方程式为
(5)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程
(6)若将12.8 g铜与 50 mL一定浓度的浓硝酸反应,两者恰好完全反应共产生气体5.6 L(标准状况),计算此浓硝酸的物质的量浓度
您最近一年使用:0次
8 . 氮及其化合物在工农业生产、生活中被广泛使用,造福人类。
I.元素 X、Y、Z 位于同一周期且原子序数依次增大,它们和氢元素、硫元素组成的含氮化合物(结构如图)常用作丝绸漂白剂。回答下列问题:
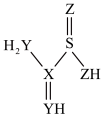
(1)硫元素在元素周期表中的位置为______ ;Y 的元素符号为______ 。
(2)下列说法错误的是______ (选填序号)。
A.原子半径:X>Y>Z
B.简单气态氢化物稳定性:Y<Z
C.该化合物可溶于水
D.该化合物中所有原子均为 8 电子稳定结构
II.工业上用氨气来制造硝酸,NH3转化关系如图所示。
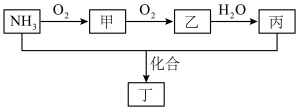
(3)NH3的电子式为______ 。
(4)图中,乙转化为丙的离子方程式为______ 。
(5)检验化合物丁中阳离子的方法:取少量待测液于试管中,______ ,将湿润的 红色石蕊试纸置于试管口,试纸变蓝。
(6)工业上常使用 NH3处理甲,生成无污染的 N2,则 NH3与甲完全反应的物质的量之比为______ 。
I.元素 X、Y、Z 位于同一周期且原子序数依次增大,它们和氢元素、硫元素组成的含氮化合物(结构如图)常用作丝绸漂白剂。回答下列问题:

(1)硫元素在元素周期表中的位置为
(2)下列说法错误的是
A.原子半径:X>Y>Z
B.简单气态氢化物稳定性:Y<Z
C.该化合物可溶于水
D.该化合物中所有原子均为 8 电子稳定结构
II.工业上用氨气来制造硝酸,NH3转化关系如图所示。

(3)NH3的电子式为
(4)图中,乙转化为丙的离子方程式为
(5)检验化合物丁中阳离子的方法:取少量待测液于试管中,
(6)工业上常使用 NH3处理甲,生成无污染的 N2,则 NH3与甲完全反应的物质的量之比为
您最近一年使用:0次
解题方法
9 . A、B、C是中学化学中常见的物质,且A、B、C均含有同一种元素,在一定条件下相互转化关系如下图所示(部分产物已略去)。请回答:
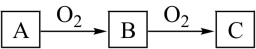
(1)若B是无色气体,C是红棕色气体。
① A、B、C所含相同元素在元素周期表中的位置是______ 。
② 下列说法正确的是______ (填字母)。
a.常温下,A为无色气体
b.A、B、C中所含相同元素的化合价依次升高
c.C与水反应只做还原剂。
③若A是化合物,写出由A氧化生产B的化学方程式__________________ 。
(2)若B是一种有刺激性气味的有毒气体,C与水反应生成硫酸
① A、B、C所含相同元素的原子结构示意图是______ 。
② 下列说法不正确的是______ (填字母)。
a.A一定是黄色晶体
b.可以用上述转化关系制备硫酸
c.B与水反应做还原剂。
③C的水溶液与氢氧化钠的反应为______________ (填吸热或放热)反应。
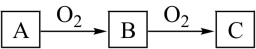
(1)若B是无色气体,C是红棕色气体。
① A、B、C所含相同元素在元素周期表中的位置是
② 下列说法正确的是
a.常温下,A为无色气体
b.A、B、C中所含相同元素的化合价依次升高
c.C与水反应只做还原剂。
③若A是化合物,写出由A氧化生产B的化学方程式
(2)若B是一种有刺激性气味的有毒气体,C与水反应生成硫酸
① A、B、C所含相同元素的原子结构示意图是
② 下列说法不正确的是
a.A一定是黄色晶体
b.可以用上述转化关系制备硫酸
c.B与水反应做还原剂。
③C的水溶液与氢氧化钠的反应为
您最近一年使用:0次
2020-07-07更新
|
197次组卷
|
2卷引用:北京市延庆区2019-2020学年高一下学期期中考试化学试题
解题方法
10 . 如图为相关物质间的转化关系,其中甲、丙为生活中常见的金属单质,乙、丁为非金属单质且丁为气态,E为白色沉淀,D为浅绿色溶液。请回答:
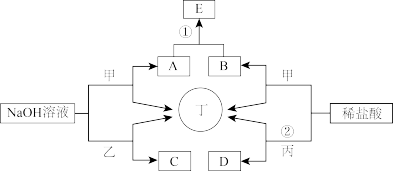
(1)组成甲的元素在元素周期表中的位置为__ ,请列举乙单质的一种用途__ ;用电子式表示丁的形成过程___ 。
(2)在C溶液中滴入2滴酚酞,再逐滴加入稀盐酸至红色消失,可得到一种胶体,该胶体的胶粒成分是__ (化学式);
(3)反应①的离子方程式为__ ;
(4)将B的稀溶液加水稀释,溶液的pH__ (填能或不能)大于7;
(5)若反应②中盐酸过量,向D溶液中滴加84消毒液,溶液的颜色发生了变化,该反应的离子方程式为__ 。

(1)组成甲的元素在元素周期表中的位置为
(2)在C溶液中滴入2滴酚酞,再逐滴加入稀盐酸至红色消失,可得到一种胶体,该胶体的胶粒成分是
(3)反应①的离子方程式为
(4)将B的稀溶液加水稀释,溶液的pH
(5)若反应②中盐酸过量,向D溶液中滴加84消毒液,溶液的颜色发生了变化,该反应的离子方程式为
您最近一年使用:0次



