名校
解题方法
1 . 某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
已知:CuCl为白色固体,难溶于水,能溶于浓盐酸。下列说法不正确的是
| 装置 |
| |
| 序号 | 试管中的药品 | 现象 |
| 实验Ⅰ | 1.5mL1mol·L-1CuSO4溶液和3.5mL1mol·L-1NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5mL1mol·L-1CuCl2溶液和3.5mL1mol·L-1NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
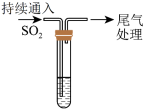
| A.取少量Cu2O固体于试管中,加入5mL0.1mol·L-1NaOH溶液,持续通入SO2,若试管底部有少量紫红色固体,溶液呈绿色,证明实验Ⅰ中砖红色沉淀为Cu2O |
| B.将实验Ⅱ中白色沉淀洗涤干净后,加入浓盐酸,沉淀溶解,然后加入蒸馏水,产生白色沉淀,证明白色沉淀为CuCl |
| C.实验Ⅱ与实验Ⅰ现象不同是因为阴离子不同造成的 |
D.实验Ⅰ、Ⅱ中不一定生成了SO |
您最近一年使用:0次
2 . 富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:

已知生成相应氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)如下:
(1)酸浸时发生反应:2MgO·SiO2+2H2SO4=2MgSO4+SiO2+2H2O,2MgO·B2O3+2H2SO4=2H3BO3+2MgSO4。
①根据上述反应可知,酸性:H2SO4___________ (填“>”或“<”)H3BO3。
②已知硼酸与过量NaOH溶液发生中和反应的离子方程式为:H3BO3+OH-= 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是___________ (填字母)
A.硼酸是一元酸
B.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
C.硼酸的电离方程式可表示为H3BO3+H2O +H+
+H+
(2)检验褐色浸出液中的杂质离子:取少量浸出液,___________ (填操作和现象),证明溶液中含有Fe2+。
(3)除去浸出液中的杂质离子:用MgO调节溶液的pH至___________ 以上,使杂质离子转化为___________ (填化学式)沉淀,过滤。
(4)获取晶体:
ⅰ.浓缩滤液,使MgSO4溶液和H3BO3溶液接近饱和;
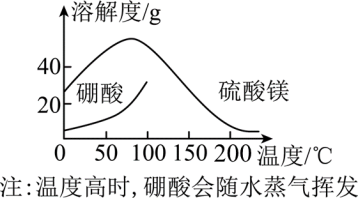
ⅱ.控制温度使两种晶体分别从溶液中结晶。结合图中溶解度曲线,简述ⅱ的方法:将浓缩液加入高压釜中升温结晶得到___________ 晶体,分离后,再将母液降温结晶,分离得到另一种物质的晶体。

已知生成相应氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)如下:
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀时 | 1.9 | 3.4 | 7.0 | 9.1 |
| 完全沉定时 | 3.2 | 4.7 | 9.0 | 11.1 |
①根据上述反应可知,酸性:H2SO4
②已知硼酸与过量NaOH溶液发生中和反应的离子方程式为:H3BO3+OH-=
 。下列关于硼酸的说法正确的是
。下列关于硼酸的说法正确的是A.硼酸是一元酸
B.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
C.硼酸的电离方程式可表示为H3BO3+H2O
 +H+
+H+(2)检验褐色浸出液中的杂质离子:取少量浸出液,
(3)除去浸出液中的杂质离子:用MgO调节溶液的pH至
(4)获取晶体:
ⅰ.浓缩滤液,使MgSO4溶液和H3BO3溶液接近饱和;
ⅱ.控制温度使两种晶体分别从溶液中结晶。结合图中溶解度曲线,简述ⅱ的方法:将浓缩液加入高压釜中升温结晶得到

您最近一年使用:0次
2023-03-19更新
|
466次组卷
|
5卷引用:山东省枣庄滕州市第二中学2021-2022学年高三上学期第一次质量检测化学试题
山东省枣庄滕州市第二中学2021-2022学年高三上学期第一次质量检测化学试题(已下线)第八章 水溶液中的离子反应与平衡 第55练 无机化工流程题的解题策略重庆市万州第二高级中学2023届高三下学期第二次质量检测化学试题(已下线)05 无机化工流程题(5) (解析)-备战2023年高考化学大题逐空突破系列(全国通用)(已下线)题型38 非金属元素相关的工艺流程
解题方法
3 . 设计如下实验验证氧化性: 。(已知:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)
。(已知:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)
下列说法错误的是
 。(已知:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)
。(已知:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色;忽略氧气的影响)| 实验① | 实验② | 实验③ | 实验④ |
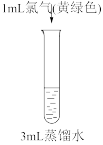 | 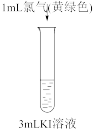 | 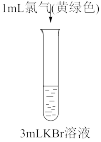 | 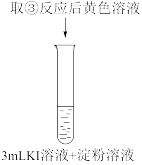 |
| 溶液变为浅黄绿色 | 溶液变为棕黄色 | 溶液变为黄色 | 溶液变为蓝色 |
A.实验①中发生反应: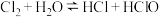 |
B.实验①②的现象可以证明氧化性: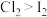 |
C.实验③发生反应: |
D.实验③④能证明氧化性: |
您最近一年使用:0次
4 . 为探究铁和硫反应产物中铁的化合价,某同学设计了如下实验过程:
Fe、S混合粉末 黑色固体
黑色固体 滤渣
滤渣 溶液A
溶液A ……
……
已知:①铁和硫反应产物不溶于碱,能溶于硫酸;
②硫可溶于热碱溶液,发生类似Cl2和NaOH溶液的化学反应。
下列说法不正确的是
Fe、S混合粉末
 黑色固体
黑色固体 滤渣
滤渣 溶液A
溶液A ……
……已知:①铁和硫反应产物不溶于碱,能溶于硫酸;
②硫可溶于热碱溶液,发生类似Cl2和NaOH溶液的化学反应。
下列说法不正确的是
| A.混合粉末应在N2氛围中进行加热,所用H2SO4溶液应先煮沸 |
| B.取溶液A,滴加KSCN溶液,未出现红色,可证明铁和硫反应只有+2价铁生成 |
| C.滤渣用稀H2SO4溶解时应在通风橱中进行 |
D.硫溶于热碱溶液可能发生的离子反应是3S+6OH-  2S2-+ 2S2-+ +3H2O +3H2O |
您最近一年使用:0次
名校
解题方法
5 . 10mL0.1mol•L-1KI溶液与5mL0.1mol•L-1FeCl3溶液发生反应:2Fe3+(aq)+2I-(aq)⇌2Fe2+(aq)+I2(aq),达到平衡。下列说法不正确的是
| A.加入少量氯化钾固体,平衡不移动 |
| B.加适量水稀释,平衡正向移动 |
| C.经过CCl4多次萃取分离后,向水溶液中滴加KSCN溶液,若溶液出现血红色,证明该反应是可逆反应 |
D.该反应的平衡常数K=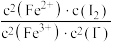 |
您最近一年使用:0次
2022-04-01更新
|
494次组卷
|
12卷引用:浙江省2021届高三下学期3月联考化学试题
浙江省2021届高三下学期3月联考化学试题(已下线)浙江省“超级全能生”2021年3月高考选考科目联考化学试题(已下线)第21讲 化学平衡状态 化学平衡的移动(精练)-2022年高考化学一轮复习讲练测(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)上海市华东师范大学第二附属中学2021-2022年高三下学期3月等级考化学试题(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第21讲 化学平衡状态 化学平衡的移动(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)2019年高考浙江卷化学试题变式题(单选题21-25)课时3影响化学平衡的因素随堂练习
解题方法
6 . 25℃时,下列说法错误的是
A.室温下向10 mL 0. 1 mol/L的氨水中加水稀释后,溶液中 的值不变 的值不变 |
| B.欲证明HA为弱酸,可将pH=3的HA溶液稀释为原体积的10倍,若测得溶液pH=4,可证明HA为弱酸 |
| C.向H2S溶液中加入CuSO4溶液时, H2S电离平衡向右移动 |
| D.在1 mol· L-1(NH4)2S溶液中存在:c(NH3·H2O) +c(OH- )=c(HS-) +2c(H2S)+c(H+ ) |
您最近一年使用:0次
名校
7 . 以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如图所示。下列说法不正确 的是
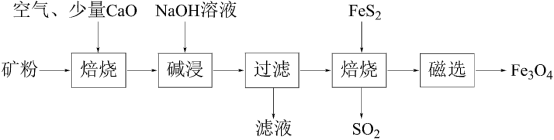

| A.“焙烧”时产生的气体可以用NaOH溶液吸收 |
| B.滤液中的铝元素主要以[Al(OH)4]-形式存在. |
| C.可以将少量Fe3O4产品溶于稀硫酸中,再滴入酸性高锰酸钾溶液,若溶液褪色则证明产品中含有FeO |
| D.可用磁选操作的原因是Fe3O4具有磁性 |
您最近一年使用:0次
2022-02-28更新
|
813次组卷
|
5卷引用:新疆昌吉教育体系2021-2022学年高三上学期第三次模考化学试题
新疆昌吉教育体系2021-2022学年高三上学期第三次模考化学试题(已下线)第十单元 化学实验基础(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)福建省南平高级中学2021-2022学年高三上学期12月月考化学试题(已下线)专题14物质的反应和转化-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题13物质的反应和转化-2022年高考真题+模拟题汇编(全国卷)
名校
解题方法
8 . 为探究SO2与Fe3+间是否发生氧化还原反应,按如图装置进行实验(夹持、加热仪器略),下列说法不正确 的是


| A.A中的反应体现了浓硫酸的氧化性和酸性 |
| B.试剂a不能使用饱和NaHCO3溶液 |
| C.C中溶液c(H+)增大,可证明Fe3+氧化了SO2 |
| D.尾气可用NaOH溶液吸收 |
您最近一年使用:0次
2022-02-28更新
|
414次组卷
|
8卷引用:北京师范大学附属中学2021-2022学年高三上学期期中考试化学试题
北京师范大学附属中学2021-2022学年高三上学期期中考试化学试题(已下线)专题36 物质的制备及实验方案的设计与评价(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)河北省邯郸市大名县第一中学2021-2022学年高一上学期第二次月考化学试题广东省广州市育才中学2021-2022学年高一下学期期中考试化学试题广东省广州科学城中学2022-2023学年高一下学期期中考试化学试题浙江省嘉兴八校联盟2021-2022学年高一下学期期中联考化学试题江苏省苏州市吴中区苏苑高级中学2023-2024学年高一上学期12月月考化学试题
名校
9 . 下列说法中正确的是
| A.离子键就是使阴、阳离子结合成化合物的静电引力 |
B. 晶体中含共价键,是共价化合物 晶体中含共价键,是共价化合物 |
C.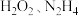 分子中只含有共价键 分子中只含有共价键 |
| D.某化合物在水溶液中能导电,可以证明该化合物内一定存在离子键 |
您最近一年使用:0次
2022-05-23更新
|
240次组卷
|
9卷引用:第13讲 原子结构 化学键(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)
(已下线)第13讲 原子结构 化学键(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)四川省自贡市田家炳中学2021届高三上学期开学考试化学试题四川省成都外国语学校2020-2021学年高一下学期第三次(6月)月考化学试题(已下线)专题五 元素周期律 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第五章 物质结构与性质元素周期律 第29练 化学键 分子的空间结构2015-2016学年四川省资阳市高一下学期期末化学试卷山东师范大学附属中学2021-2022学年高一下学期期中考试(等级考)化学试题浙江省舟山市普陀中学2021-2022学年高一下学期6月月考化学试题(已下线)【2022】【高二上】【期中考】【高中化学】61
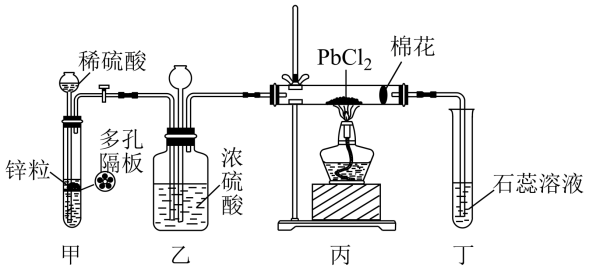
10 . 二氯化铅常温下为白色固体,沸点为 ,工业上常用作助焊剂。某小组同学欲证明氢气能否在加热的条件下还原二氯化铅,设计如下实验。下列说法错误的是
,工业上常用作助焊剂。某小组同学欲证明氢气能否在加热的条件下还原二氯化铅,设计如下实验。下列说法错误的是
 ,工业上常用作助焊剂。某小组同学欲证明氢气能否在加热的条件下还原二氯化铅,设计如下实验。下列说法错误的是
,工业上常用作助焊剂。某小组同学欲证明氢气能否在加热的条件下还原二氯化铅,设计如下实验。下列说法错误的是
| A.乙中长颈漏斗的作用是平衡压强 |
| B.点燃丙中酒精灯后,应先对直形玻璃管进行预热,然后再集中加热 |
| C.若丁中溶液变红,则可证明氢气能在加热的条件下还原二氯化铅 |
| D.甲中试剂可用浓盐酸代替,丁中试剂可用硝酸银溶液代替 |
您最近一年使用:0次