1 . 某工厂采用软锰矿(主要成分为 )与辉铋矿(主要成分为
)与辉铋矿(主要成分为 ,含有
,含有 、
、 杂质)联合焙烧法制备电池级的
杂质)联合焙烧法制备电池级的 和BiOCl,工艺流程如下:
和BiOCl,工艺流程如下:

已知:①焙烧时过量的 分解为
分解为 ,加热时
,加热时 在酸性溶液中转化为
在酸性溶液中转化为 和Mn²⁺,MnO与酸反应生成
和Mn²⁺,MnO与酸反应生成 ;
;
②金属活动性顺序:Fe>(H)>Bi>Cu;
③相关金属离子形成氢氧化物的pH范围:
④BiOCl的式量:260.5
回答下列问题:
(1)下列有关说法错误的是___________。
(2) 经热解、酸浸等步骤可制备
经热解、酸浸等步骤可制备 。
。 在空气气流中热解得到三种价态锰的氧化物,锰元素所占比例(某价态锰的元素的中锰元素质量×100%)随热解温度变化的曲线如图所示。为获得较高产率的
在空气气流中热解得到三种价态锰的氧化物,锰元素所占比例(某价态锰的元素的中锰元素质量×100%)随热解温度变化的曲线如图所示。为获得较高产率的 ,请选出正确操作并按序排列:取一定量
,请选出正确操作并按序排列:取一定量 置于热解装置中,通空气气流,
置于热解装置中,通空气气流,___________ ,充分反应后过滤、洗涤、干燥,得到 。
。

a.冷却至室温
b.加热到450℃分解一段时间
c.加热到480℃分解一段时间
d.边搅拌边加入一定量1 mol⋅L-1的 溶液
溶液
e.边搅拌边加入一定量1 mol⋅L-1的HCl溶液0
(3)BiOCl含量的测定。称取产品0.1302g于锥形瓶中,加15 mL 36%的盐酸溶解,加掩蔽剂防止杂质离子对终点判断产生干扰,调pH至1.5~1.8,加入饱和硫脲与 形成黄色络合物,再用0.0200 mol⋅L-1的EDTA滴定至终点,消耗溶液22.50 mL。已知EDTA与
形成黄色络合物,再用0.0200 mol⋅L-1的EDTA滴定至终点,消耗溶液22.50 mL。已知EDTA与 1∶1发生络合反应,所得产物的稳定性远大于硫脲与
1∶1发生络合反应,所得产物的稳定性远大于硫脲与 形成的黄色络合物。
形成的黄色络合物。
①根据滴定实验测得的数据计算,产品的质量分数为___________ 。
②临近滴定终点时的操作方法是:将旋塞稍稍转动,使半滴溶液悬于管口,___________ ,再用洗瓶以少量蒸馏水吹洗锥形瓶内壁,直到滴入最后半滴EDTA,溶液恰好由黄色变为无色,半分钟内不变色。
③下列关于滴定分析的操作,错误的是___________ 。
A.装入滴定管中的溶液无需用量筒量取
B.滴定时要适当控制滴定速度
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.①中计算所得数据即为产品纯度
 )与辉铋矿(主要成分为
)与辉铋矿(主要成分为 ,含有
,含有 、
、 杂质)联合焙烧法制备电池级的
杂质)联合焙烧法制备电池级的 和BiOCl,工艺流程如下:
和BiOCl,工艺流程如下:
已知:①焙烧时过量的
 分解为
分解为 ,加热时
,加热时 在酸性溶液中转化为
在酸性溶液中转化为 和Mn²⁺,MnO与酸反应生成
和Mn²⁺,MnO与酸反应生成 ;
;②金属活动性顺序:Fe>(H)>Bi>Cu;
③相关金属离子形成氢氧化物的pH范围:
| 开始沉淀pH | 完全沉淀pH | |
 | 6.5 | 8.3 |
 | 1.6 | 2.8 |
 | 8.1 | 10.1 |
回答下列问题:
(1)下列有关说法错误的是___________。
A.焙烧时,只有 是还原剂 是还原剂 |
| B.为提高焙烧效率,鼓入适当过量的空气 |
C.滤渣A是 ,气体A是 ,气体A是 |
D.加入金属铋的作用是将 转化为Fe 转化为Fe |
 经热解、酸浸等步骤可制备
经热解、酸浸等步骤可制备 。
。 在空气气流中热解得到三种价态锰的氧化物,锰元素所占比例(某价态锰的元素的中锰元素质量×100%)随热解温度变化的曲线如图所示。为获得较高产率的
在空气气流中热解得到三种价态锰的氧化物,锰元素所占比例(某价态锰的元素的中锰元素质量×100%)随热解温度变化的曲线如图所示。为获得较高产率的 ,请选出正确操作并按序排列:取一定量
,请选出正确操作并按序排列:取一定量 置于热解装置中,通空气气流,
置于热解装置中,通空气气流, 。
。
a.冷却至室温
b.加热到450℃分解一段时间
c.加热到480℃分解一段时间
d.边搅拌边加入一定量1 mol⋅L-1的
 溶液
溶液e.边搅拌边加入一定量1 mol⋅L-1的HCl溶液0
(3)BiOCl含量的测定。称取产品0.1302g于锥形瓶中,加15 mL 36%的盐酸溶解,加掩蔽剂防止杂质离子对终点判断产生干扰,调pH至1.5~1.8,加入饱和硫脲与
 形成黄色络合物,再用0.0200 mol⋅L-1的EDTA滴定至终点,消耗溶液22.50 mL。已知EDTA与
形成黄色络合物,再用0.0200 mol⋅L-1的EDTA滴定至终点,消耗溶液22.50 mL。已知EDTA与 1∶1发生络合反应,所得产物的稳定性远大于硫脲与
1∶1发生络合反应,所得产物的稳定性远大于硫脲与 形成的黄色络合物。
形成的黄色络合物。①根据滴定实验测得的数据计算,产品的质量分数为
②临近滴定终点时的操作方法是:将旋塞稍稍转动,使半滴溶液悬于管口,
③下列关于滴定分析的操作,错误的是
A.装入滴定管中的溶液无需用量筒量取
B.滴定时要适当控制滴定速度
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.①中计算所得数据即为产品纯度
您最近一年使用:0次
解题方法
2 . 甲烷水蒸气重整反应是工业制备氢气的重要方式,在催化剂(如镍)表面发生的主要反应有:
①
 kJ⋅mol-1
kJ⋅mol-1
②

副反应: ,
,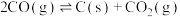 ,
,
Ⅰ.已知: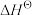 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其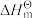 为零。
为零。
例如C(石墨)
 kJ·mol-1,则
kJ·mol-1,则 的标准生成焓为-393.5 kJ⋅mol-1。
的标准生成焓为-393.5 kJ⋅mol-1。
(1)
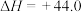 kJ⋅mol-1,结合表中数据计算反应
kJ⋅mol-1,结合表中数据计算反应
___________ 。
(2)在镍催化剂表面甲烷和水蒸气发生反应,最后生成CO、 和
和 ,反应机理如下,请补充其中的两个反应方程式(Z表示催化剂的活性中心)。
,反应机理如下,请补充其中的两个反应方程式(Z表示催化剂的活性中心)。
a. ;
;
b.___________ ;
c. ;
;
d.___________ ;
e.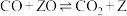
Ⅱ.在一体积可变的密闭容器中,投入一定量的 和
和 发生甲烷水蒸气重整反应。
发生甲烷水蒸气重整反应。
(3)下列有关说法正确的是___________。
(4)维持压强100 kPa,平衡时 、
、 、CO、
、CO、 的体积分数分别为a、b、c、d,反应①的平衡常数
的体积分数分别为a、b、c、d,反应①的平衡常数
___________  (用含字母的式子表示。
(用含字母的式子表示。 是以分压表示的平衡常数,分压=总压×体积分数)。
是以分压表示的平衡常数,分压=总压×体积分数)。
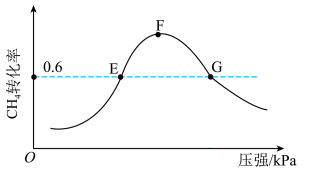
(5)500℃时,反应相同时间后测得 的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(E)
的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(E)___________ c(G)(填“>”“<”或“=”)。
(6)通过甲烷水蒸气重整反应的平衡含量计算,以及析碳条件的判断,该转化需适当增大水碳比[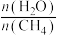 ],请分析可能的原因:
],请分析可能的原因:___________ 。
①

 kJ⋅mol-1
kJ⋅mol-1②


副反应:
 ,
,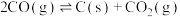 ,
,
Ⅰ.已知:
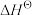 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其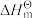 为零。
为零。例如C(石墨)

 kJ·mol-1,则
kJ·mol-1,则 的标准生成焓为-393.5 kJ⋅mol-1。
的标准生成焓为-393.5 kJ⋅mol-1。| 物质 |  |  | CO |
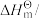 /kJ⋅mol-1 /kJ⋅mol-1 | -285.8 | -393.5 | -110.5 |

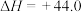 kJ⋅mol-1,结合表中数据计算反应
kJ⋅mol-1,结合表中数据计算反应
(2)在镍催化剂表面甲烷和水蒸气发生反应,最后生成CO、
 和
和 ,反应机理如下,请补充其中的两个反应方程式(Z表示催化剂的活性中心)。
,反应机理如下,请补充其中的两个反应方程式(Z表示催化剂的活性中心)。a.
 ;
; b.
c.
 ;
;d.
e.
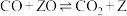
Ⅱ.在一体积可变的密闭容器中,投入一定量的
 和
和 发生甲烷水蒸气重整反应。
发生甲烷水蒸气重整反应。(3)下列有关说法正确的是___________。
A. 浓度不变,说明体系已达平衡状态 浓度不变,说明体系已达平衡状态 |
| B.反应②前后气体物质的量不变,所以此反应熵变为0 |
C.在催化剂表面, 、 、 分子中的化学键被削弱 分子中的化学键被削弱 |
D.在体系中通入适量的 ,有利于减少积碳,从而有利于反应进行 ,有利于减少积碳,从而有利于反应进行 |
 、
、 、CO、
、CO、 的体积分数分别为a、b、c、d,反应①的平衡常数
的体积分数分别为a、b、c、d,反应①的平衡常数
 (用含字母的式子表示。
(用含字母的式子表示。 是以分压表示的平衡常数,分压=总压×体积分数)。
是以分压表示的平衡常数,分压=总压×体积分数)。(5)500℃时,反应相同时间后测得
 的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(E)
的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(E)
(6)通过甲烷水蒸气重整反应的平衡含量计算,以及析碳条件的判断,该转化需适当增大水碳比[
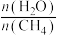 ],请分析可能的原因:
],请分析可能的原因:
您最近一年使用:0次
3 . 下列说法正确的是
| A.所有α-氨基酸都存在对映异构体 |
| B.淀粉、纤维素、蛋白质和核苷酸都属于高分子化合物 |
C.以CO和 为原料,通过加成反应可合成液态烃和甲醇等有机物 为原料,通过加成反应可合成液态烃和甲醇等有机物 |
| D.石油裂解的产物除了乙烯、丙烯等不饱和烃外,还含有甲烷、乙烷等 |
您最近一年使用:0次
名校
4 . 下列实验装置(部分夹持装置略)或现象错误的是
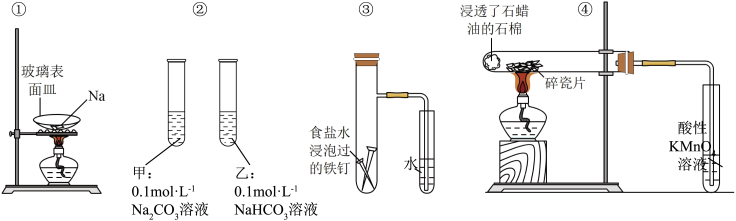

| A.图①:观察到钠燃烧的火焰颜色为黄色,且有淡黄色固体生成 |
| B.图②:两支试管中滴入酚酞溶液后,甲中溶液为红色,乙中溶液为浅红色 |
| C.图③:一段时间后,观察到右侧导管有一段高于液面的水柱 |
D.图④:石蜡油受热分解,右侧试管盛放的酸性 溶液褪色 溶液褪色 |
您最近一年使用:0次
2023-07-15更新
|
208次组卷
|
2卷引用:浙江省嘉兴市2022届高三一模考试化学试题
解题方法
5 . 青霉素类药物是人类史上最重要的抗菌药物,其中两种药物阿莫西林(P)、非奈西林(Q)、重要中间体6-APA的结构以及阿莫西林的合成路线如下图所示。
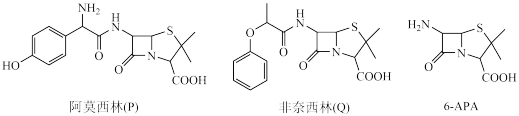
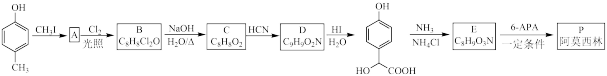
已知:①
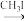

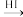
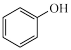
②RCHO + HCN → RCH(OH)CN
③RCN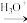 RCOOH + NH
RCOOH + NH
回答下列问题:
(1)C中含有的不饱和官能团的名称为_______ 。
(2)下列说法错误 的是_______。(填序号)
(3)D与足量氢碘酸反应的化学方程式为_______ 。
(4)写出6-APA满足下列条件的所有同分异构体的结构简式:__ 。
①含有苯环;
②含有磺酸基(-SO3H);
③核磁共振氢谱有4组峰
(5)试设计以苯酚、乙醛和6-APA为原料,制备非奈西林(Q)的合成路线__ 。(无机试剂任选)


已知:①

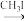

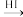
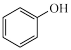
②RCHO + HCN → RCH(OH)CN
③RCN
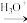 RCOOH + NH
RCOOH + NH
回答下列问题:
(1)C中含有的不饱和官能团的名称为
(2)下列说法
| A.1mol对甲基苯酚能与含2mol溴的溴水反应 |
| B.B能发生取代、加成、消去、氧化反应 |
| C.E能发生缩聚反应形成高分子 |
| D.阿莫西林分子中含有5个手性碳原子 |
(4)写出6-APA满足下列条件的所有同分异构体的结构简式:
①含有苯环;
②含有磺酸基(-SO3H);
③核磁共振氢谱有4组峰
(5)试设计以苯酚、乙醛和6-APA为原料,制备非奈西林(Q)的合成路线
您最近一年使用:0次
名校
解题方法
6 . 黄色固体X是由四种元素组成的化合物,用作颜料和食品的抗结剂,为测定其组成,进行如下实验。已知气体D能使澄清石灰水变浑浊,溶液F中只含有一种溶质。回答下列问题:
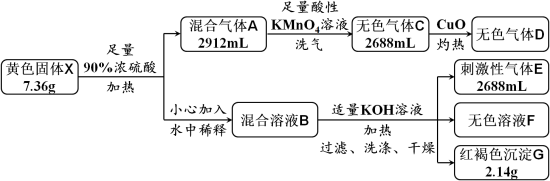
(1)固体X的组成元素是_______ 。
(2)混合气体A中所含物质的化学式为_______ 。
(3)实验中溶液B由X转化而来的溶质与KOH反应的总离子方程式为_______ 。
(4)证明沉淀G中的金属元素已完全沉淀的方法是_______ 。
(5)X与酸性KMnO4溶液反应,可生成一种与X组成元素相同,但式量比其小39的化合物,该反应的化学方程式为_______ 。

(1)固体X的组成元素是
(2)混合气体A中所含物质的化学式为
(3)实验中溶液B由X转化而来的溶质与KOH反应的总离子方程式为
(4)证明沉淀G中的金属元素已完全沉淀的方法是
(5)X与酸性KMnO4溶液反应,可生成一种与X组成元素相同,但式量比其小39的化合物,该反应的化学方程式为
您最近一年使用:0次
2022-12-09更新
|
422次组卷
|
4卷引用:浙江省诸暨海亮高级中学2021-2022学年高三12月份选考模拟化学试题
浙江省诸暨海亮高级中学2021-2022学年高三12月份选考模拟化学试题浙江省舟山中学2022-2023学年高三上学期首考模拟卷(三)化学试题(已下线)浙江省温州市普通高中2023届高三下学期第二次适应性考试化学试题变式题(无机推断题)甘肃省两县高中联考2023-2024学年高三上学期12月月考化学试题
7 . 在常温常压下,下列属于自发过程的是
| A.2C(s) + O2(g) = 2CO(g) |
| B.NH4Cl(s) = NH3(g) + HCl(g) |
| C.CH3COOH(l) = CH3COOH(s) |
D.2Cr3+(aq) + 3Cl2(aq) + 7H2O(l) = Cr2O (aq) + 6Cl-(aq)+14H+(aq) (aq) + 6Cl-(aq)+14H+(aq) |
您最近一年使用:0次
解题方法
8 . 在Cl·(氯自由基)参与下,CH4与Cl2反应生成CH3Cl和HCl的能量-反应进程图如图所示,下列说法正确的是


| A.该反应的决速步是第二步 |
| B.Cl·是该反应的催化剂 |
| C.CH3·+ Cl2 + HCl是该反应的过渡态 |
| D.升高温度,Ea1和Ea2变小,反应速率增大 |
您最近一年使用:0次
名校
解题方法
9 . 以海水和贝壳为原料制备金属镁和漂白粉的流程如下图所示。下列说法不正确 的是
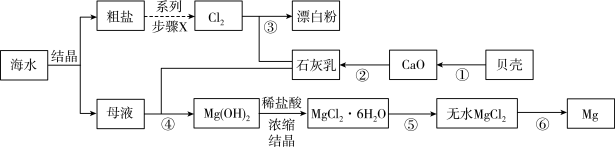

| A.图中的系列步骤x包括粗盐提纯和电解 |
| B.步骤③反应的离子方程式为Cl2 + Ca(OH)2 =Ca2++ Cl-+ClO-+H2O |
| C.在实验室实现步骤④所需要的玻璃仪器有漏斗、烧杯、玻璃棒 |
| D.为防止生成氧化镁,步骤⑥制得的镁应在氮气氛围中冷却 |
您最近一年使用:0次
2022-12-09更新
|
289次组卷
|
2卷引用:浙江省诸暨海亮高级中学2021-2022学年高三12月份选考模拟化学试题
解题方法
10 . 下列工业提取物质的方法不正确 的是
| A.工业上用电解饱和食盐水制备氯气 |
| B.用“吹出法”从海水中提取溴需要用到SO2 |
| C.可以直接加热分解氧化银制备金属银 |
| D.碳酸钠是烘制糕点所用发酵剂的主要成分之一 |
您最近一年使用:0次



