名校
1 . 科技的进步为二氧化碳的资源化利用提供了广阔的前景,我国科学家首次在实验室实现 CO2到淀粉的合成,其路线如下,

设NA为阿伏加德罗常数的值。下列说法错误的是

设NA为阿伏加德罗常数的值。下列说法错误的是
| A.标准状况下,11.2 L CO2含有的共用电子对的数目为NA |
| B.常温常压下,16 gCH3OH 含有的极性键数目为2.5NA |
| C.标准状况下,42 g C2H4和CO混合气体的体积为33.6 L |
| D.已知:2CO(g)+O2(g)=2CO2(g) ΔH=-565.8kJ/mol,则CO的燃烧热为282.9 kJ/mol |
您最近一年使用:0次
2 . 低碳经济已成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。回答下列问题:
(1)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
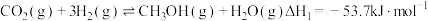
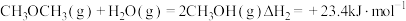
则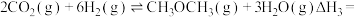
_______ kJ∙mol-1。
(2)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由 制取
制取 的太阳能工艺如图:
的太阳能工艺如图: ,则
,则 的化学式为
的化学式为_______ ,“热分解系统”中每转移 电子,需消耗
电子,需消耗
_______  。
。
(3)催化时还可以使用一种无机固体电解质作催化剂,其由正离子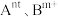 和负离子
和负离子 组成,该物质
组成,该物质 以上形成无序结构(高温相),
以上形成无序结构(高温相), 以下变为有序结构(低温相),二者晶体晶胞结构如图所示:
以下变为有序结构(低温相),二者晶体晶胞结构如图所示:_______ 。
ii.“高温相”具有良好的离子导电性,其主要原因是_______ 。
(4)铜基催化剂 (
( 为
为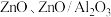 等)是
等)是 加氢制甲醇常用的催化剂,部分合成路线如图所示。
加氢制甲醇常用的催化剂,部分合成路线如图所示。 上发生反应的总化学方程式
上发生反应的总化学方程式_______ 。
(5)利用电解法在碱性或酸性条件下将 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示: 和法拉第效率(
和法拉第效率(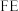 )的定义(X代表
)的定义(X代表 或
或 )如下:
)如下:
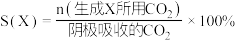

①实验测得,碱性条件生成 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是_______ 。
②实验测得,酸性条件生成 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是_______ 。
(1)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知: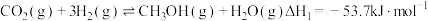
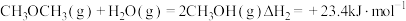
则
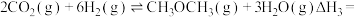
(2)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由
 制取
制取 的太阳能工艺如图:
的太阳能工艺如图: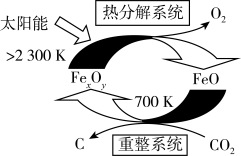
 ,则
,则 的化学式为
的化学式为 电子,需消耗
电子,需消耗
 。
。(3)催化时还可以使用一种无机固体电解质作催化剂,其由正离子
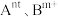 和负离子
和负离子 组成,该物质
组成,该物质 以上形成无序结构(高温相),
以上形成无序结构(高温相), 以下变为有序结构(低温相),二者晶体晶胞结构如图所示:
以下变为有序结构(低温相),二者晶体晶胞结构如图所示: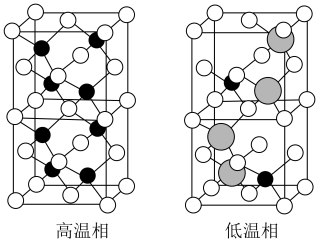
说明:图中,○球为负离子;高温相中的●深色球为正离子或空位;低温相中的 球为
球为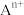 离子,●球为
离子,●球为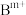 离子。
离子。
ii.“高温相”具有良好的离子导电性,其主要原因是
(4)铜基催化剂
 (
( 为
为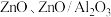 等)是
等)是 加氢制甲醇常用的催化剂,部分合成路线如图所示。
加氢制甲醇常用的催化剂,部分合成路线如图所示。 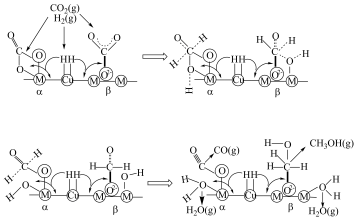
 上发生反应的总化学方程式
上发生反应的总化学方程式(5)利用电解法在碱性或酸性条件下将
 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示: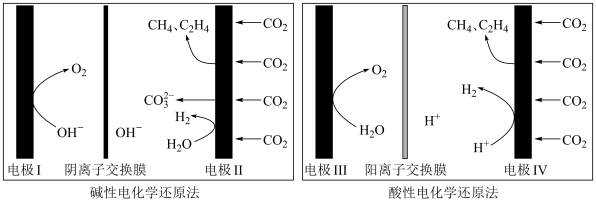
 和法拉第效率(
和法拉第效率(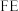 )的定义(X代表
)的定义(X代表 或
或 )如下:
)如下: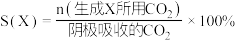

①实验测得,碱性条件生成
 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是②实验测得,酸性条件生成
 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是
您最近一年使用:0次
3 . 乙烯的产量可以用来衡量一个国家的石油化工发展水平,A和B是生活中两种常见的有机物,C是一种具有香味的物质,且碳原子数是A的两倍。现以乙烯为主要原料合成C,其合成路线如图所示,请回答下列问题:
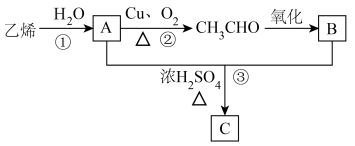
(1)乙烯的结构简式:______ 。
(2)A分子中含有的官能团名称为______ 。
(3)②的反应类型为______ ,③的反应类型为______ 。
(4)写出反应①的化学方程式_______ 。

(1)乙烯的结构简式:
(2)A分子中含有的官能团名称为
(3)②的反应类型为
(4)写出反应①的化学方程式
您最近一年使用:0次
名校
解题方法
4 . 我国科学家成功制得新型的可化学循环的高分子材料,其合成路线如下(部分试剂和反应条件略去)。

下列说法不正确 的是

下列说法
| A.反应①中,标记*的碳原子被氧化 |
| B.可用银氨溶液检验化合物Ⅲ中的官能团 |
| C.反应②和反应③都发生了π键的断裂 |
| D.聚合物Ⅳ充分水解后的产物仍为高分子 |
您最近一年使用:0次
名校
5 . 甘氨酸亚铁晶体是一种新型的固体整合补铁剂。其实验室合成路线为:铁片 甘氨酸亚铁晶体粗品
甘氨酸亚铁晶体粗品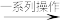 甘氨酸亚铁晶体纯品。
甘氨酸亚铁晶体纯品。
已知:①相关物质的信息如下表所示
②含有多个配位原子的配体与同一中心离子通过螯合配位成环而形成的配合物称为螯合物。
(一) 固体的制备
固体的制备

(1)实验开始时应先开 和
和_______ ,关_______ (填“ ”或“
”或“ ”);一段时间后,改变开关状态,生成
”);一段时间后,改变开关状态,生成 。
。
(2)三颈瓶中生成 沉淀的离子方程式为
沉淀的离子方程式为_______ 。
(二)甘氨酸亚铁的制备
(3)用如图装置制备甘氨酸亚铁。反应开始时,先通过滴液口滴入适量的NaOH溶液调节pH为5左右,pH过高或过低都会使产率下降,原因是_______ 。

(4)当 固体完全溶解后,再通过滴液口加入乙醇,其作用是
固体完全溶解后,再通过滴液口加入乙醇,其作用是_______ 。
(5)反应结束后,过滤出产品粗品,依次用_______ 、_______ (填序号)洗涤,再经过一系列操作得纯品。
a.热水 b.冰水 c.乙醇
(三)甘氨酸亚铁晶体结构的分析
步骤1:准确称取甘氨酸亚铁晶体纯品0.4800 g于锥形瓶中,加 溶液15 mL将样品溶解完全后,加入指示剂,立即用
溶液15 mL将样品溶解完全后,加入指示剂,立即用 标准液滴定至终点,用去标准液20.20 mL(反应为
标准液滴定至终点,用去标准液20.20 mL(反应为 )。
)。
步骤2:不加产品,重复步骤1操作,滴定至终点,用去标准液0.20 mL。
回答下列问题:
(6)甘氨酸亚铁晶体中Fe的质量分数为_______ %(保留小数点后一位)。
(7)进一步分析表明:甘氨酸亚铁晶体中,阴阳离子只有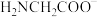 和
和 ;
; 的配位数为6,且存在五元整合环;该配合物呈中心对称,甘氨酸亚铁晶体的结构简式为
的配位数为6,且存在五元整合环;该配合物呈中心对称,甘氨酸亚铁晶体的结构简式为_______ 。
 甘氨酸亚铁晶体粗品
甘氨酸亚铁晶体粗品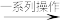 甘氨酸亚铁晶体纯品。
甘氨酸亚铁晶体纯品。已知:①相关物质的信息如下表所示
| 物质 | 化学式 | 摩尔质量 | 性质 |
| 甘氨酸 |  | 75 g/mol | 两性物质,易溶于水,微溶于乙醇 |
| 甘氨酸亚铁晶体 | 易溶于水,溶解度随温度升高而增大;难溶于乙醇,在潮湿的空气中易被氧化 |
(一)
 固体的制备
固体的制备
(1)实验开始时应先开
 和
和 ”或“
”或“ ”);一段时间后,改变开关状态,生成
”);一段时间后,改变开关状态,生成 。
。(2)三颈瓶中生成
 沉淀的离子方程式为
沉淀的离子方程式为(二)甘氨酸亚铁的制备
(3)用如图装置制备甘氨酸亚铁。反应开始时,先通过滴液口滴入适量的NaOH溶液调节pH为5左右,pH过高或过低都会使产率下降,原因是

(4)当
 固体完全溶解后,再通过滴液口加入乙醇,其作用是
固体完全溶解后,再通过滴液口加入乙醇,其作用是(5)反应结束后,过滤出产品粗品,依次用
a.热水 b.冰水 c.乙醇
(三)甘氨酸亚铁晶体结构的分析
步骤1:准确称取甘氨酸亚铁晶体纯品0.4800 g于锥形瓶中,加
 溶液15 mL将样品溶解完全后,加入指示剂,立即用
溶液15 mL将样品溶解完全后,加入指示剂,立即用 标准液滴定至终点,用去标准液20.20 mL(反应为
标准液滴定至终点,用去标准液20.20 mL(反应为 )。
)。步骤2:不加产品,重复步骤1操作,滴定至终点,用去标准液0.20 mL。
回答下列问题:
(6)甘氨酸亚铁晶体中Fe的质量分数为
(7)进一步分析表明:甘氨酸亚铁晶体中,阴阳离子只有
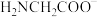 和
和 ;
; 的配位数为6,且存在五元整合环;该配合物呈中心对称,甘氨酸亚铁晶体的结构简式为
的配位数为6,且存在五元整合环;该配合物呈中心对称,甘氨酸亚铁晶体的结构简式为
您最近一年使用:0次
6 . 甘氨酸亚铁晶体是一种新型的固体整合补铁剂。其实验室合成路线为:
铁片

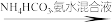

 甘氨酸亚铁晶体粗品
甘氨酸亚铁晶体粗品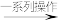 甘氨酸亚铁晶体纯品
甘氨酸亚铁晶体纯品
已知:
相关物质的信息如下表所示
(一) 固体的制备
固体的制备
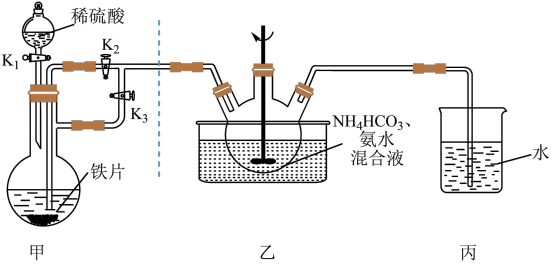
(1)实验开始时应先开 和
和_______ ,关_______ (填“ ”或“
”或“ ”)一段时间后,改变开关状态,生成
”)一段时间后,改变开关状态,生成 。
。
(2)三颈瓶中生成 的离子方程式为
的离子方程式为_______ 。
(二)甘氨酸亚铁的制备
(3)用如图装置制备甘氨酸亚铁。反应开始时,先通过滴液口滴入适量的 溶液调节
溶液调节 为5左右,
为5左右, 过高或过低都会使产率下降,原因是
过高或过低都会使产率下降,原因是_______ 。
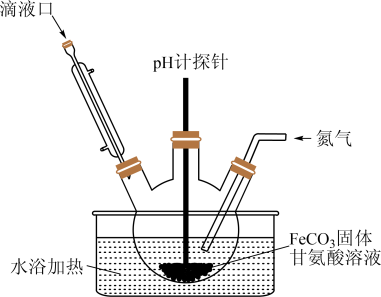
(4)当 固体完全溶解后,再通过滴液口加入乙醇,其作用是
固体完全溶解后,再通过滴液口加入乙醇,其作用是_______ 。
(5)反应结束后,过滤出产品粗品,依次用_______ 、_______ (填序号)洗涤,再经过一系列操作得纯品。
a.热水 b.冰水 c.乙醇
(三)甘氨酸亚铁晶体结构的分析
步骤1:准确称取甘氨酸亚铁晶体纯品0.4800g于锥形瓶中,加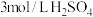 溶液15mL将样品溶解完全后,加入指示剂,立即用
溶液15mL将样品溶解完全后,加入指示剂,立即用 标准液滴定至终点,用去标准液20.20mL(反应为
标准液滴定至终点,用去标准液20.20mL(反应为 )。
)。
步骤2:不加产品,重复步骤1操作,滴定至终点,用去标准液0.20mL。
回答下列问题:
(6)滴定时应选择_______ 滴定管。
(7)甘氨酸亚铁晶体中 的质量分数为
的质量分数为_______ %(保留小数点后一位)。
(8)进一步分析表明:甘氨酸亚铁晶体中,阴阳离子只有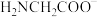 和
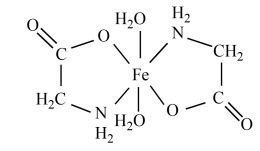
和 且存在五元鳌合环,甘氨酸亚铁晶体的结构简式如下图所示,则
且存在五元鳌合环,甘氨酸亚铁晶体的结构简式如下图所示,则 的配位数为
的配位数为_______ 。
铁片


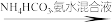

 甘氨酸亚铁晶体粗品
甘氨酸亚铁晶体粗品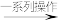 甘氨酸亚铁晶体纯品
甘氨酸亚铁晶体纯品已知:
相关物质的信息如下表所示
| 物质 | 化学式 | 摩尔质量 | 性质 |
| 甘氨酸 |  | 75g/mol | 两性物质,易溶于水,微溶于乙醇 |
| 甘氨酸亚铁晶体 | 易溶于水,溶解度随温度升高而增大:难溶于乙醇,在潮湿的空气中易被氧化 |
 固体的制备
固体的制备
(1)实验开始时应先开
 和
和 ”或“
”或“ ”)一段时间后,改变开关状态,生成
”)一段时间后,改变开关状态,生成 。
。(2)三颈瓶中生成
 的离子方程式为
的离子方程式为(二)甘氨酸亚铁的制备
(3)用如图装置制备甘氨酸亚铁。反应开始时,先通过滴液口滴入适量的
 溶液调节
溶液调节 为5左右,
为5左右, 过高或过低都会使产率下降,原因是
过高或过低都会使产率下降,原因是
(4)当
 固体完全溶解后,再通过滴液口加入乙醇,其作用是
固体完全溶解后,再通过滴液口加入乙醇,其作用是(5)反应结束后,过滤出产品粗品,依次用
a.热水 b.冰水 c.乙醇
(三)甘氨酸亚铁晶体结构的分析
步骤1:准确称取甘氨酸亚铁晶体纯品0.4800g于锥形瓶中,加
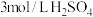 溶液15mL将样品溶解完全后,加入指示剂,立即用
溶液15mL将样品溶解完全后,加入指示剂,立即用 标准液滴定至终点,用去标准液20.20mL(反应为
标准液滴定至终点,用去标准液20.20mL(反应为 )。
)。步骤2:不加产品,重复步骤1操作,滴定至终点,用去标准液0.20mL。
回答下列问题:
(6)滴定时应选择
(7)甘氨酸亚铁晶体中
 的质量分数为
的质量分数为(8)进一步分析表明:甘氨酸亚铁晶体中,阴阳离子只有
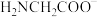 和
和 且存在五元鳌合环,甘氨酸亚铁晶体的结构简式如下图所示,则
且存在五元鳌合环,甘氨酸亚铁晶体的结构简式如下图所示,则 的配位数为
的配位数为
您最近一年使用:0次
名校
7 . 已知有机化合物A的产量可以用来衡量一个国家的石油化工发展水平。现以A为主要原料合成乙酸乙酯,其合成路线如图甲所示。
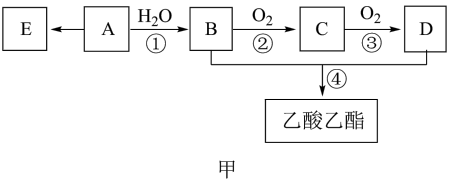
(1)A分子的电子式为_______ ,D分子中官能团的名称是______ ,反应①的反应类型是_______ 反应。
(2)反应②的化学方程式是______ 。
(3)某同学用如图乙所示的实验装置制取少量乙酸乙酯。实验结束后,试管甲中上层为透明的、难溶于水的油状液体。
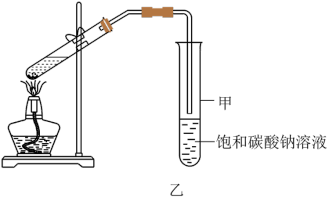
①若实验中用D和含18O的B反应,该反应的化学方程式为_______ 。
②反应物混合溶液加入的用量及顺序依次为_______ 。
③实验开始时,试管甲中的导管不伸入液面下的原因是______ 。
④上述实验中饱和碳酸钠溶液的作用是______ 。

(1)A分子的电子式为
(2)反应②的化学方程式是
(3)某同学用如图乙所示的实验装置制取少量乙酸乙酯。实验结束后,试管甲中上层为透明的、难溶于水的油状液体。

①若实验中用D和含18O的B反应,该反应的化学方程式为
②反应物混合溶液加入的用量及顺序依次为
③实验开始时,试管甲中的导管不伸入液面下的原因是
④上述实验中饱和碳酸钠溶液的作用是
您最近一年使用:0次
8 . “从二氧化碳到淀粉的人工合成”入选2021年度“中国生命科学十大进展”。实验室实现由CO2到淀粉的合成路线如图,下列说法正确的是


| A.标准状况下,11.2 L CO2中含有共用电子对数目为3 NA |
| B.反应②的原子利用率为100% |
| C.其他条件相同,温度越高,反应②的反应速率越快 |
| D.“人工合成淀粉”有助于“双碳”达标和缓解粮食危机 |
您最近一年使用:0次
9 . 托莫西汀(W)是一种神经系统药物,临床上主要用于注意缺陷障碍的治疗,它的一种合成路线如图所示。下列说法错误的是
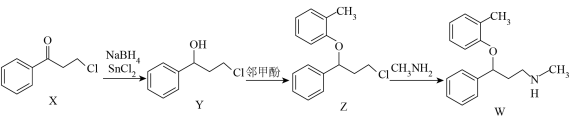
A. 中的H的化合价为 中的H的化合价为 ,该物质有较强还原性,常用作还原剂 ,该物质有较强还原性,常用作还原剂 |
B. 邻甲酚与足量浓溴水反应,最多消耗 邻甲酚与足量浓溴水反应,最多消耗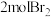 |
| C.每个Z分子中含有1个手性碳原子 |
| D.在一定条件下,W能分别和氢气,氧气反应,但不能和盐酸反应 |
您最近一年使用:0次
2024-04-16更新
|
211次组卷
|
3卷引用:2024届名校联盟(T8联盟)高三下学期模拟信息(五)理科综合试题-高中化学
10 . “从二氧化碳到淀粉的人工合成”入选2021年度“中国生命科学十大进展”。实验室实现由CO2到淀粉的合成路线如图,下列说法正确的是


| A.标准状况下,11.2LCO2中含有共用电子对数目为3NA |
| B.反应②的原子利用率为100% |
| C.淀粉的分子式为(C6H10O5)n,与纤维素互为同分异构体 |
| D.“人工合成淀粉”有助于“双碳”达标和缓解粮食危机 |
您最近一年使用:0次



