1 . 下列关于金属铝的叙述中,说法不正确的是
| A.铝的化学性质很活泼,但在空气中不易锈蚀 |
| B.铝是比较活泼的金属,在化学反应中容易失去电子,表现出还原性 |
| C.铝箔在空气中受热可以熔化,且发生剧烈燃烧 |
| D.铝箔在空气中受热可以熔化,但由于氧化膜的存在,熔化的铝并不滴落 |
您最近一年使用:0次
2018-11-15更新
|
470次组卷
|
6卷引用:鲁教版高中化学必修1第四章《材料家族中的元素》测试卷1
2018高一上·全国·专题练习
2 . 现有两瓶失去标签的Na2CO3和NaHCO3无色的饱和溶液,请提出简便的鉴别方法,其中不合理的是
①用干燥的pH试纸检验,pH大的是Na2CO3
②取同量的溶液于两支试管中,各滴入酚酞试液,红色较深的是Na2CO3
③取同量的溶液于两支试管中,加热,有气泡产生的是NaHCO3
④取同量的溶液于两支试管中,逐滴加入稀盐酸,开始就有气体放出的是NaHCO3
⑤取同量的溶液于两支试管中,滴加BaCl2溶液,生成白色沉淀的是Na2CO3
⑥取同量的溶液于两支试管中,滴加Ba(OH)2溶液,生成白色沉淀的是Na2CO3
①用干燥的pH试纸检验,pH大的是Na2CO3
②取同量的溶液于两支试管中,各滴入酚酞试液,红色较深的是Na2CO3
③取同量的溶液于两支试管中,加热,有气泡产生的是NaHCO3
④取同量的溶液于两支试管中,逐滴加入稀盐酸,开始就有气体放出的是NaHCO3
⑤取同量的溶液于两支试管中,滴加BaCl2溶液,生成白色沉淀的是Na2CO3
⑥取同量的溶液于两支试管中,滴加Ba(OH)2溶液,生成白色沉淀的是Na2CO3
| A.①② | B.⑥ | C.④⑤ | D.②⑤ |
您最近一年使用:0次
名校
解题方法
3 . 下列关于金属性质的叙述正确的是
| A.金属一般都容易导电导热,有延展性 |
| B.金属具有较高的硬度和熔点 |
| C.所有金属都是固态 |
| D.金属单质都能与稀H2SO4反应产生H2 |
您最近一年使用:0次
2018-10-16更新
|
270次组卷
|
4卷引用:专题9 本专题达标检测-高中化学必修第二册苏教版2019
专题9 本专题达标检测-高中化学必修第二册苏教版2019河北省衡水市安平中学2017-2018学年高一上学期第三次月考化学试题2(已下线)2018年10月8日 《每日一题》人教必修1-金属在自然界中的存在与通性四川省雅安市2019-2020学年高一上学期期末检测化学试题
13-14高一上·云南玉溪·期末
名校
解题方法
4 . 氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是 ( )。
| A.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 |
| B.通常状况下,干燥的氯气能与Fe反应 |
| C.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照H2和Cl2的混合气体时,因迅速化合而爆炸 |
| D.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸 |
您最近一年使用:0次
2018-09-15更新
|
886次组卷
|
10卷引用:第二章 海水中的重要元素——钠和氯(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)
(已下线)第二章 海水中的重要元素——钠和氯(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)(已下线)2012-2013学年云南省玉溪一中高一上学期期末考试化学试卷(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第2讲 氧及其化合物【教学案】(已下线)【新东方】2020-59(已下线)2.2.1 氯气的性质-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)山东省泰安市第一实验学校2021届高三10月月考化学试题辽宁省东港市第三中学2020-2021学年高一上学期期中考试化学试题(已下线)练习3 钠、氯及其化合物-2020-2021学年【补习教材·寒假作业】高一化学(人教版2019)(已下线)2.2.1 氯气的性质-2021-2022学年高一化学10分钟课前预习练(人教版2019必修第一册)(附参考答案)安徽省安庆市第二中学2023-2024学年高一上学期12月月考化学试题
解题方法
5 . A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
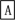

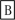
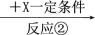
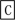
试回答:
(1)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为________ ;C溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示)________________ ,检验此C溶液中金属元素价态的操作方法是__________ 。
(2)若A、B、C为含有金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为________ ,X的化学式可能为(写出不同类物质)________ 或________ ,反应①的离子方程式为____________ 或_____________________ 。
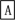

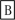
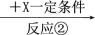
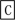
试回答:
(1)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为
(2)若A、B、C为含有金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为
您最近一年使用:0次
2018-09-06更新
|
198次组卷
|
2卷引用:2018-2019学年苏教版高中化学必修一 专题综合测评3
解题方法
6 . 工业上用铝土矿(含氧化铝、氧化铁)制取铝的过程如下:
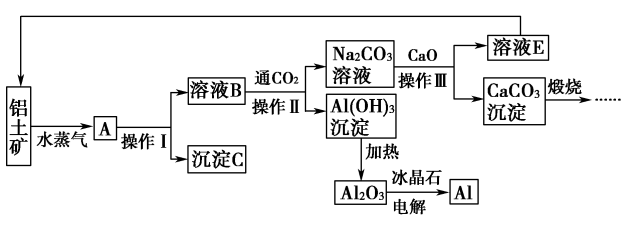
请回答下列问题:
(1)请说出沉淀C在工业上的一种用途:_____________________ 。
(2)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有_____ (填化学式)。
(3)操作Ⅰ、操作Ⅱ和操作Ⅲ都是________ (填操作名称)。实验室洗涤Al(OH)3沉淀的方法是__________________________________________ 。
(4)电解熔融的氧化铝,若得到标准状况下22.4 L O2,则同时生成铝的质量为________ g。
(5)写出Na2CO3溶液与CaO反应的离子方程式:_____________________ 。

请回答下列问题:
(1)请说出沉淀C在工业上的一种用途:
(2)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有
(3)操作Ⅰ、操作Ⅱ和操作Ⅲ都是
(4)电解熔融的氧化铝,若得到标准状况下22.4 L O2,则同时生成铝的质量为
(5)写出Na2CO3溶液与CaO反应的离子方程式:
您最近一年使用:0次
解题方法
7 . 霞石是一种硅酸盐,其组成可表示为K2O·3Na2O·4Al2O3·8SiO2,某小组同学设计以霞石为原料制备Al2O3的方案如下:

请回答下列问题:
(1)沉淀1的化学式为______________________________________________ 。
(2)滤液1与过量NaOH溶液反应的所有的离子方程式为____________ 。
(3)写出由溶液2生成Al(OH)3的离子方程式:_______________________ 。
(4)通入过量的CO2,过滤后的滤液中含有的阴离子主要是________ 。
(5)由Al(OH)3→Al2O3的反应条件为_________________________________ 。

请回答下列问题:
(1)沉淀1的化学式为
(2)滤液1与过量NaOH溶液反应的所有的离子方程式为
(3)写出由溶液2生成Al(OH)3的离子方程式:
(4)通入过量的CO2,过滤后的滤液中含有的阴离子主要是
(5)由Al(OH)3→Al2O3的反应条件为
您最近一年使用:0次
解题方法
8 . 下列说法正确的是( )
| A.向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色,该溶液中一定含有Fe2+ |
| B.将过量锌粉加入氯化铁溶液中,离子方程式为:Zn+2Fe3+===Zn2++2Fe2+ |
| C.除去FeCl2中少量的FeBr2,加入适量氯水,再加四氯化碳萃取分液 |
| D.FeCl3溶液可以腐蚀线路板上的Cu,说明Fe的金属活泼性大于Cu |
您最近一年使用:0次
9 . 含硫化合物的种类很多,现有H2SO4、H2SO3、SO2、Na2SO3、BaSO4、CuSO4、Na2SO4这7种常见的含硫化合物。回答下列问题:
(1)H2SO3转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式,并标明电子转移的方向和数目:_______________________________________ 。
(2)常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面_______________________ ,则发生了钝化;若铁棒表面____________________ ,则未发生反应。
(3)用Na2SO3吸收法是治理SO2污染的一种方法,其原理为(用化学方程式表示):_______________________________________________________________ 。
(4)减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2,该反应的化学方程式:______________________ 。
(1)H2SO3转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式,并标明电子转移的方向和数目:
(2)常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面
(3)用Na2SO3吸收法是治理SO2污染的一种方法,其原理为(用化学方程式表示):
(4)减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2,该反应的化学方程式:
您最近一年使用:0次
解题方法
10 . A、B、C、D、E、F、X存在如图所示转换关系,其中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。X可能是强酸,也可能是强碱。











(1)A的化学式是________ 。
(2)若X是强酸,将D与Cl2同时通入水中发生反应的离子方程式为____________________ 。
(3)若X是强碱,过量的B跟Cl2反应除生成C外,另一产物是氯化物。
①过量的B跟Cl2反应的化学方程式为___________________________ 。
②工业生产中B→D的化学方程式为_______________________________ 。











(1)A的化学式是
(2)若X是强酸,将D与Cl2同时通入水中发生反应的离子方程式为
(3)若X是强碱,过量的B跟Cl2反应除生成C外,另一产物是氯化物。
①过量的B跟Cl2反应的化学方程式为
②工业生产中B→D的化学方程式为
您最近一年使用:0次



