1 . 现有一块金属钠露置于空气中一段时间,为检验该固体是否部分变质为碳酸钠,先将固体样品溶解于水得到溶液,并采取下列措施,其中可以实现实验目的的是 。
| A.测所得溶液的pH |
| B.取溶液少量,向其中滴入酚酞观察溶液是否变红 |
| C.取溶液少量,向其中加入盐酸观察是否有气泡产生 |
| D.取溶液少量,向其中加入CuSO4溶液,观察是否有沉淀产生 |
您最近一年使用:0次
2017-12-21更新
|
126次组卷
|
8卷引用:2018年12月31日 《每日一题》人教必修1-钠露置在空气中的变化
(已下线)2018年12月31日 《每日一题》人教必修1-钠露置在空气中的变化(已下线)3.2.2 碳酸钠 碳酸氢钠(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)(已下线)2013-2014江西省南昌三中高二下学期期末考试化学试卷2017届内蒙古准格尔旗世纪中学高三上月考二化学卷宁夏育才中学学益校区2017-2018学年高一12月月考化学试题河南省兰考县第二高级中学2017-2018学年高一上学期期末考试化学试题广东省东莞市北师大石竹附属学校2020届高三上学期9月月考化学试题安徽省六安市新安中学2020-2021学年高一下学期入学考试化学试题
2 . 食用二氧化硫漂白过的食品,对人体的肝、肾脏等有严重损害。某科研小组设计实验检验二氧化硫的漂白性。回答下列问题:
(一)二氧化硫的制备
实验室一般采用亚硫酸钠与硫酸(浓硫酸与水1:1混合)反应制取二氧化硫:
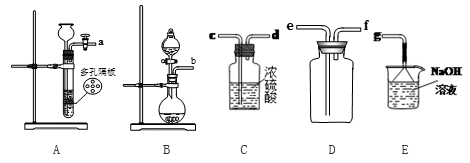
(1)欲收集一瓶干燥的二氧化硫,选择上图中的装置,其最佳连接顺序为:________ (按气流方向,用小写字母表示)。
(二)二氧化硫性质的检验
将上述收集到的SO2通入下列装置中,在一定温度下按图示装置进行实验。
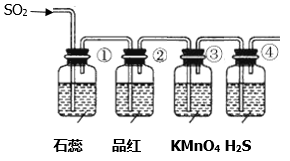
(2)根据上述实验,回答下列问题:
(3)实验中发现Na2SO3可能部分变质,现需测定Na2SO3的纯度,称15.0g Na2SO3样品,配成250mL溶液,取25.00mL溶液,用0.20 mol·L―1酸性KMnO4溶液进行滴定,达到滴定终点时消耗KMnO4溶液20.00mL。达到滴定终点时锥形瓶中溶液颜色变化是________________________ ,样品中Na2SO3质量分数是_______ 。
(一)二氧化硫的制备
实验室一般采用亚硫酸钠与硫酸(浓硫酸与水1:1混合)反应制取二氧化硫:

(1)欲收集一瓶干燥的二氧化硫,选择上图中的装置,其最佳连接顺序为:
(二)二氧化硫性质的检验
将上述收集到的SO2通入下列装置中,在一定温度下按图示装置进行实验。

(2)根据上述实验,回答下列问题:
| 序号 | 实验现象 | 解释原因 |
| ① | ||
| ② | 品红试液褪色 | SO2具有漂白性 |
| ③ | 反应的离子方程式 | |
| ④ | 溶液变浑浊,有黄色沉淀生成 | SO2+2H2S=3S↓+2H2O |
您最近一年使用:0次
名校
3 . 由下列实验及现象不能推出相应结论的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向添有KIO3的食盐中加入淀粉溶液、稀盐酸及KI | 溶液变蓝色 | 氧化性:IO3- >I2 |
| B | 将SO2气体通入到Ba(NO3)2溶液中 | 生成白色沉淀 | 此沉淀是BaSO3 |
| C | 将FeCl2样品溶于盐酸后,滴加KSCN溶液 | 溶液变成红色 | 原FeCl2样品已变质 |
| D | 燃烧的钠粒放入CO2中 | 燃烧且有白色和黑色颗粒产生 | 黑色颗粒是炭,白色颗粒可能是Na2CO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-12-23更新
|
324次组卷
|
2卷引用:2020届高三化学二轮冲刺新题专练——化学综合实验的设计与评价方案
2018高三下·全国·专题练习
名校
4 . 下列实验操作所得的现象及结论均正确的是
| 选项 | 实验操作 | 现象及结论 |
| A | 向酸性KMnO4溶液中通入乙烯 | 溶液紫红色褪去,说明乙烯具有还原性 |
| B | 向FeI2溶液中滴入少量氯水 | 溶液变黄,说明还原性:I−>Fe2+ |
| C | 将AlCl3溶液加热蒸干 | 得到白色固体,成分为纯净的AlCl3 |
| D | 将少量Na2SO3样品溶于水,滴入盐酸酸化的Ba(NO3)2溶液 | 有白色沉淀产生,说明Na2SO3已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-04-20更新
|
79次组卷
|
5卷引用:2018年3月2018届高三第一次全国大联考(新课标Ⅰ卷)-化学试题
(已下线)2018年3月2018届高三第一次全国大联考(新课标Ⅰ卷)-化学试题(已下线)2018年5月25日 押高考化学第11题(2)——《每日一题》2018年高三化学四轮复习(已下线)2019年5月24日 《每日一题》四轮复习——押高考化学第11题(2)甘肃省临泽县第一中学2017-2018学年高二下学期6月月考化学试题湖南省永州市祁阳县2018-2019学年高二上学期期末考试化学试题
名校
5 . 下列有关实验操作、现象和目的或结论的说法正确的是
选项 | 操作 | 目的或结论 |
A | 将Fe(NO3)2晶体溶于稀硫酸后,滴加KSCN溶液,观察溶液是否变红 | 检验Fe(NO3)2样品是否已被氧化而变质 |
B | 海带提碘实验中,为了制取海带灰的浸取液,需要煮沸海带灰和水的混合物1~2min | 主要目的是去除溶液中的氧气,避免氧气氧化碘离子 |
C | 在试管中依次加入2mL浓硫酸、3mL乙醇和2mL乙酸,用酒精灯缓慢加热 | 制备乙酸乙酯 |
D | 向盛有少量Mg(OH)2固体的试管中加入适量NH4Cl浓溶液,充分振荡,白色固体溶解 | NH4+与Mg(OH)2溶解出的OH-结合,导致Mg(OH)2溶解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-03-15更新
|
885次组卷
|
2卷引用:2020届高三化学二轮冲刺新题专练——仪器的连接和实验的操作顺序(提升练)
6 . 石灰石—石膏法脱硫是除去工业烟气中所含SO2的重要方法,其工艺分为两步: —是吸收产生亚硫酸氢钙,二是氧化产生石膏。某校化学兴趣小组实验模拟该工艺,设计装置如下:
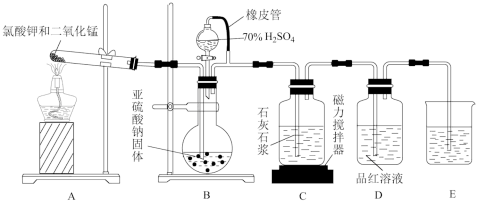
(1)装置B模拟产生含SO2的工业烟气,则E装置的作用是___________ 。
(2)实验开始时,打开装置B中分液漏斗的活塞,向烧瓶中逐滴滴加硫酸,D中立即产生了明显的现象,造成产生这一现象的原因是___________。
(3)预计当装置C中产生___________ 的现象时,关闭装置B中分液漏斗的活塞,再点燃装置A处的酒精灯。实际实验过程中却始终未观察到C中产生这一现象,小组成员多次逬行实验探究,最终发现是药品Na2SO3部分变质,请写出定性实验发现药品Na2SO3问题的有关操作及现象:取少量的亚硫酸钠固体于试管中,___________ 。
(4)小组成员进一步定量实验,测量Na2SO3的纯度:
①称取12.0 g Na2SO3固体配成l00 mL溶液,取25.00mL于锥形瓶中,并加入几滴淀粉溶液。
②用0.1000 mol •L-1酸性KIO3溶液滴定,三次平行实验测得标准液的体积为20.00mL。则滴定终点时锥形瓶中产生的现象为___________ ,写出与产生终点现象有关反应的离子方程式___________ ,样品中Na2SO3的质量分数为___________ 。(计算结果保留三位有效数字)。

(1)装置B模拟产生含SO2的工业烟气,则E装置的作用是
(2)实验开始时,打开装置B中分液漏斗的活塞,向烧瓶中逐滴滴加硫酸,D中立即产生了明显的现象,造成产生这一现象的原因是___________。
| A.该装置的气密性不够好 | B.滴加硫酸的速率较快 |
| C.使用的硫酸浓度较小 | D.石灰石浆液中碳酸钙粉末的颗粒太小 |
(4)小组成员进一步定量实验,测量Na2SO3的纯度:
①称取12.0 g Na2SO3固体配成l00 mL溶液,取25.00mL于锥形瓶中,并加入几滴淀粉溶液。
②用0.1000 mol •L-1酸性KIO3溶液滴定,三次平行实验测得标准液的体积为20.00mL。则滴定终点时锥形瓶中产生的现象为
您最近一年使用:0次
7 . 下列依据相关实验得出的结论正确的是
| A.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
| B.将Fe(NO3)2样品溶于稀盐酸中,然后滴加KSCN溶液,溶液变红,说明Fe(NO3)2样品已氧化变质 |
| C.在食盐试样中加入盐酸和KI溶液,加入淀粉溶液后变蓝,说明食盐试样中可能含有KIO3 |
| D.加入AgNO3溶液后生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有Cl-存在 |
您最近一年使用:0次
2016-12-09更新
|
128次组卷
|
3卷引用:2020届高三化学二轮微专题突破训练:物质的检验、分离与提纯
8 . 下列化学实验事实及解释都正确的是
| A.向Na2SO3溶液中加入硝酸酸化的Ba(NO3)2溶液,有白色沉淀出现,说明Na2SO3溶液已经变质 |
| B.某溶液中加入盐酸产生无色气体,该气体能使澄清石灰水变浑浊,说明该溶液中一定有CO32- |
| C.某溶液中加入BaCl2溶液,产生白色沉淀,加稀硝酸后,白色沉淀不溶解,也无其他现象,说明该溶液中一定含有SO42- |
| D.取少量久置的Na2SO3样品溶于水,加足量盐酸有气体产生,然后加BaCl2溶液,产生白色沉淀,说明Na2SO3样品已部分变质 |
您最近一年使用:0次
2017·浙江·一模
9 . 实验室有一瓶久置的Na2SO3固体试剂,已部分变质,为测定其纯度,实验设计与操作如下,请回答问题:
(1)Na2SO3变质的原因(用化学方程式表示)___________ 。
(2)取一定量的样品溶于水,加入过量的BaCl2溶液,然后过滤(如图)、洗涤、干燥、称量,其中洗涤沉淀的具体操作为___________ 。
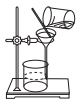
(3)实验时用BaCl2比用CaCl2好,写出两点理由:___________ 。
(1)Na2SO3变质的原因(用化学方程式表示)
(2)取一定量的样品溶于水,加入过量的BaCl2溶液,然后过滤(如图)、洗涤、干燥、称量,其中洗涤沉淀的具体操作为

(3)实验时用BaCl2比用CaCl2好,写出两点理由:
您最近一年使用:0次
名校
解题方法
10 . 乙基溴化镁( )是一种性质极为活泼的有机试剂。其制备和使用过程如下:
)是一种性质极为活泼的有机试剂。其制备和使用过程如下:
已知:
①制备原理: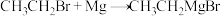
 ,反应决速步为
,反应决速步为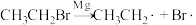 ,该步所需能量决定了反应的活性;
,该步所需能量决定了反应的活性;
② 极易在空气、潮湿、酸性环境下变质;
极易在空气、潮湿、酸性环境下变质;
③几种物质的物理性质
Ⅰ.制备
在仪器A中加入3.6gMg屑(已在稀盐酸中浸泡2小时并干燥),向恒压滴液漏斗中倒入10.1mL(0.10mol) 和25.0mL无水乙醚的混合液备用。之后将少量混合液加入A中,并添加少量引发剂,使用热风枪吹热A,待液体微沸,再逐滴缓慢加入余下的混合液,冰浴1.5h后反应结束。
和25.0mL无水乙醚的混合液备用。之后将少量混合液加入A中,并添加少量引发剂,使用热风枪吹热A,待液体微沸,再逐滴缓慢加入余下的混合液,冰浴1.5h后反应结束。
打开恒压滴液漏斗上口的玻璃塞,加入6.7mL(0.12mol)乙醛,之后打开其下口使乙醛逐滴与 反应,然后滴加20.0mL饱和
反应,然后滴加20.0mL饱和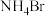 溶液生成产物X(伴有一种盐和碱性气体产生)。将X从混合液中提纯后,其质量为5.92g。
溶液生成产物X(伴有一种盐和碱性气体产生)。将X从混合液中提纯后,其质量为5.92g。
回答下列问题:
(1)仪器A的名称是______ , 的晶体类型为
的晶体类型为______ 。
(2)Ar气球的作用是______ 。
(3)研究发现,卤代烃均有和Mg反应的性质,则以下物质中反应活性最高的为______(填序号)。
(4)“制备”过程中使用热风枪替代酒精灯的原因是______ 。若迟迟未能引发反应,则将溶剂更换为四氢呋喃即可顺利进行,其原因是______ 。
(5)“使用”过程中,X在提纯后进行了氢谱和质谱的表征,结果如下: 与乙醛反应生成X(碳骨架无支链)的总反应为
与乙醛反应生成X(碳骨架无支链)的总反应为______ 。
(6) 在“制备”中的产率为
在“制备”中的产率为______ %(“使用”过程中反应均完全,且提纯无损耗)。
 )是一种性质极为活泼的有机试剂。其制备和使用过程如下:
)是一种性质极为活泼的有机试剂。其制备和使用过程如下:已知:
①制备原理:
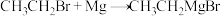
 ,反应决速步为
,反应决速步为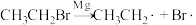 ,该步所需能量决定了反应的活性;
,该步所需能量决定了反应的活性;②
 极易在空气、潮湿、酸性环境下变质;
极易在空气、潮湿、酸性环境下变质;③几种物质的物理性质
| 物质 | 熔点/℃ | 沸点/℃ | 物理性质(25℃) |
| 乙醚 | ―116.2 | 34.5 | 无色液体、易挥发、易燃 |
| 四氢呋喃 | ―108.5 | 66.0 | 无色液体,可溶于水、乙醛 |
| 乙基溴化镁 | ―116.3 | 34.6 | 深棕色液体 |
在仪器A中加入3.6gMg屑(已在稀盐酸中浸泡2小时并干燥),向恒压滴液漏斗中倒入10.1mL(0.10mol)
 和25.0mL无水乙醚的混合液备用。之后将少量混合液加入A中,并添加少量引发剂,使用热风枪吹热A,待液体微沸,再逐滴缓慢加入余下的混合液,冰浴1.5h后反应结束。
和25.0mL无水乙醚的混合液备用。之后将少量混合液加入A中,并添加少量引发剂,使用热风枪吹热A,待液体微沸,再逐滴缓慢加入余下的混合液,冰浴1.5h后反应结束。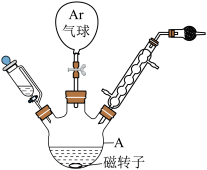
打开恒压滴液漏斗上口的玻璃塞,加入6.7mL(0.12mol)乙醛,之后打开其下口使乙醛逐滴与
 反应,然后滴加20.0mL饱和
反应,然后滴加20.0mL饱和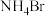 溶液生成产物X(伴有一种盐和碱性气体产生)。将X从混合液中提纯后,其质量为5.92g。
溶液生成产物X(伴有一种盐和碱性气体产生)。将X从混合液中提纯后,其质量为5.92g。回答下列问题:
(1)仪器A的名称是
 的晶体类型为
的晶体类型为(2)Ar气球的作用是
(3)研究发现,卤代烃均有和Mg反应的性质,则以下物质中反应活性最高的为______(填序号)。
A.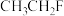 | B. | C. | D.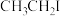 |
(4)“制备”过程中使用热风枪替代酒精灯的原因是
(5)“使用”过程中,X在提纯后进行了氢谱和质谱的表征,结果如下:
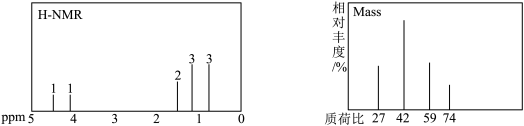
 与乙醛反应生成X(碳骨架无支链)的总反应为
与乙醛反应生成X(碳骨架无支链)的总反应为(6)
 在“制备”中的产率为
在“制备”中的产率为
您最近一年使用:0次



