解题方法
1 . 回答下列问题
(1)用做消化系统X射线检查的内服药剂“钡餐”的化学式为___________ 。
(2)酸雨的
___________ 5.6(填“>”、“<”、“=”)。
(3) 的电子式
的电子式___________ 。
(4)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅,化学方程式为___________ 。
(5)己知:①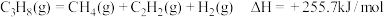
②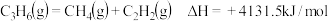
则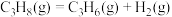 的
的
___________ 。
(1)用做消化系统X射线检查的内服药剂“钡餐”的化学式为
(2)酸雨的

(3)
 的电子式
的电子式(4)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅,化学方程式为
(5)己知:①
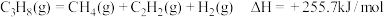
②
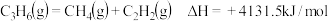
则
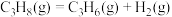 的
的
您最近一年使用:0次
解题方法
2 . 请回答:
(1)NH3的电子式是___________ ;金刚砂的化学式___________ 。
(2)工业制粗硅的化学方程式是___________
(3)铜和稀硝酸反应的离子方程式是___________
(1)NH3的电子式是
(2)工业制粗硅的化学方程式是
(3)铜和稀硝酸反应的离子方程式是
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)①写出NH3的电子式_______ ;
②甘氨酸的结构简式为_______ 。
(2)写出碳和浓硫酸加热时发生反应的化学方程式_______ ;
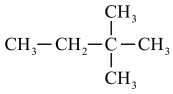
(3)图的系统命名法的名称_______ ,其二氯代物有_______ 种。
(1)①写出NH3的电子式
②甘氨酸的结构简式为
(2)写出碳和浓硫酸加热时发生反应的化学方程式
(3)图的系统命名法的名称
您最近一年使用:0次
名校
4 . 请按要求回答下列问题:
(1)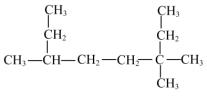 系统命名为
系统命名为________ 。
(2)三元乙丙橡胶的一种单体的键线式为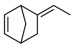 ,它的分子式为
,它的分子式为_______ 。
(3)A的化学式为 ,已知A只有一种类型的氢原子:则A的结构简式为
,已知A只有一种类型的氢原子:则A的结构简式为_______ 。
(4)某烃的分子式为 ,其能使酸性高锰酸钾溶液褪色,写出该物质生成高分子化合物的反应方程式
,其能使酸性高锰酸钾溶液褪色,写出该物质生成高分子化合物的反应方程式______ ,此反应类型为______ 。
(5)请写出环己烷(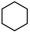 )与
)与 在光照条件下生成一氯环己烷的化学方程式
在光照条件下生成一氯环己烷的化学方程式_______ 。
(6)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系: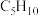 ,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸和丙酸,则此烯烃的结构简式是
,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸和丙酸,则此烯烃的结构简式是______ 。
(1)
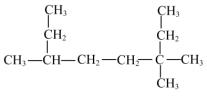 系统命名为
系统命名为(2)三元乙丙橡胶的一种单体的键线式为
 ,它的分子式为
,它的分子式为(3)A的化学式为
 ,已知A只有一种类型的氢原子:则A的结构简式为
,已知A只有一种类型的氢原子:则A的结构简式为(4)某烃的分子式为
 ,其能使酸性高锰酸钾溶液褪色,写出该物质生成高分子化合物的反应方程式
,其能使酸性高锰酸钾溶液褪色,写出该物质生成高分子化合物的反应方程式(5)请写出环己烷(
 )与
)与 在光照条件下生成一氯环己烷的化学方程式
在光照条件下生成一氯环己烷的化学方程式(6)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系:
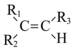
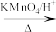
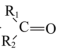 +R3COOH
+R3COOH
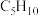 ,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸和丙酸,则此烯烃的结构简式是
,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸和丙酸,则此烯烃的结构简式是
您最近一年使用:0次
5 . 碳和硅是ⅣA族的重要元素,碳可形成多种化合物,硅是信息时代的基石,下面是有关的化合物及其转化。
Ⅰ.乙烯是基本的化工原料,合成乙醇的路线如图
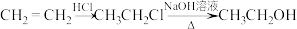
(1)乙烯的电子式为______ ,根据碳氧原子成键特点写出乙醇同分异构体的结构简式______ 。
(2)第二步是取代反应,写出该反应的化学方程式______ 。
Ⅱ. 高温(1100℃)还原
高温(1100℃)还原 可得到高纯硅,实验室用下列装置模拟该过程(部分加热装置省略)
可得到高纯硅,实验室用下列装置模拟该过程(部分加热装置省略)
已知: 沸点33℃,遇水剧烈反应生成硅酸
沸点33℃,遇水剧烈反应生成硅酸______ ,C中发生的反应为______ 。
(4)该装置存在的缺陷是______ 。
(5)碳硅位于同一主族,根据同主族元素递变规律,非金属性碳______ 硅(填“>”或“<”),下列能说明上述规律的是______ 。
a.焦炭与石英砂高温反应制取粗硅;
b.二氧化碳通入水玻璃产生白色沉淀
c.碳化硅与浓强碱发生非氧化还原反应:
d.石灰石和石英高温制玻璃:
Ⅰ.乙烯是基本的化工原料,合成乙醇的路线如图
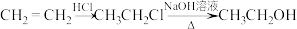
(1)乙烯的电子式为
(2)第二步是取代反应,写出该反应的化学方程式
Ⅱ.
 高温(1100℃)还原
高温(1100℃)还原 可得到高纯硅,实验室用下列装置模拟该过程(部分加热装置省略)
可得到高纯硅,实验室用下列装置模拟该过程(部分加热装置省略)已知:
 沸点33℃,遇水剧烈反应生成硅酸
沸点33℃,遇水剧烈反应生成硅酸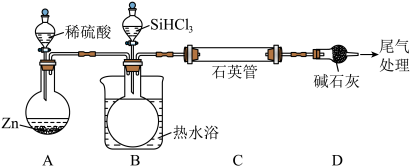
(4)该装置存在的缺陷是
(5)碳硅位于同一主族,根据同主族元素递变规律,非金属性碳
a.焦炭与石英砂高温反应制取粗硅;
b.二氧化碳通入水玻璃产生白色沉淀
c.碳化硅与浓强碱发生非氧化还原反应:

d.石灰石和石英高温制玻璃:

您最近一年使用:0次
解题方法
6 . A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其基态原子的电子排布图为___________ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B-的结构示意图为___________ ,C元素在元素周期表的___________ 区,写出常温下B的单质与C的最高价氧化物对应水化物反应的化学方程式:___________ 。
(3)D元素的正三价离子的3d能级为半充满状态,其基态原子的电子排布式为___________ 。
试根据原子核外电子排布所遵循的原理解释D的二价阳离子具有较强的还原性,易被氧化为正三价离子的原因:___________ 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的价电子排布式为___________ 。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其基态原子的电子排布图为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B-的结构示意图为
(3)D元素的正三价离子的3d能级为半充满状态,其基态原子的电子排布式为
试根据原子核外电子排布所遵循的原理解释D的二价阳离子具有较强的还原性,易被氧化为正三价离子的原因:
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的价电子排布式为
您最近一年使用:0次
7 . 我国的冶金工业十分发达,钢铁年产量已达到十亿吨,占世界产量的一半以上,同时有色金属产量也超过了七千万吨。
(1)铜是人类最早使用的金属,其电阻率小、延展性好,常用于制作电路板,在使用氯化铁溶液蚀刻铜制电路板时,发生反应的化学方程式为___________ 。
(2)铝与 溶液反应的化学方程式为
溶液反应的化学方程式为___________ ;铝的化学性质较活泼,但在空气中不会完全锈蚀,其原因是___________ 。
(3)电镀是一种常见的金属处理工艺,然而在生产过程中,电镀厂会产生大量的高毒性废水,将其直接排放会造成严重的污染。因此,废水的处理是电镀行业面临的主要问题之一。
①在电镀之前,镀件需要用酸性 溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的
溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的 固体,将
固体,将 还原为
还原为 ,则还原过程中发生反应的离子方程式为
,则还原过程中发生反应的离子方程式为___________ ,当有 被完全处理时,理论上需要加入
被完全处理时,理论上需要加入 的质量为
的质量为___________ 。
②为了减缓镀件表面的金属沉积速率,得到均匀、光滑的镀层,电解液中除重金属盐外,还需要加入剧毒的 。已知
。已知 中各原子均满足8电子稳定结构,则
中各原子均满足8电子稳定结构,则 的电子式为
的电子式为___________ 。在碱性的废电解液中通入氯气可以将 氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为___________ 。
(1)铜是人类最早使用的金属,其电阻率小、延展性好,常用于制作电路板,在使用氯化铁溶液蚀刻铜制电路板时,发生反应的化学方程式为
(2)铝与
 溶液反应的化学方程式为
溶液反应的化学方程式为(3)电镀是一种常见的金属处理工艺,然而在生产过程中,电镀厂会产生大量的高毒性废水,将其直接排放会造成严重的污染。因此,废水的处理是电镀行业面临的主要问题之一。
①在电镀之前,镀件需要用酸性
 溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的
溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的 固体,将
固体,将 还原为
还原为 ,则还原过程中发生反应的离子方程式为
,则还原过程中发生反应的离子方程式为 被完全处理时,理论上需要加入
被完全处理时,理论上需要加入 的质量为
的质量为②为了减缓镀件表面的金属沉积速率,得到均匀、光滑的镀层,电解液中除重金属盐外,还需要加入剧毒的
 。已知
。已知 中各原子均满足8电子稳定结构,则
中各原子均满足8电子稳定结构,则 的电子式为
的电子式为 氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
您最近一年使用:0次
8 . Ⅰ.某些有机化合物的模型如图所示。回答下列问题:
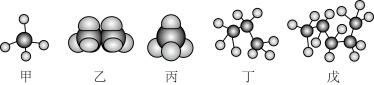
(1)属于填充模型的是___________ (填“甲”、“乙”、“丙”、“丁”或“戊”,下同)。
(2)表示同一种有机化合物的是___________ 。
(3)存在同分异构体的是___________ ,请写出其任意一种同分异构体的结构简式___________ 。
Ⅱ.农药波尔多液的主要成分是CuSO4,下列两个反应都有CuSO4生成。
①Cu+2H2SO4=CuSO4+SO2+2H2O ②CuO+H2SO4=CuSO4+H2O
请回答下列问题:
(4)从分类角度来看CuSO4属于___________。
(5)上述两个反应属于氧化还原反应的是___________ (填序号),其中氧化剂是___________ 。
(6)反应①的副产物SO2是大气污染物,可用NaOH溶液吸收,反应方程式是___________ 。

(1)属于填充模型的是
(2)表示同一种有机化合物的是
(3)存在同分异构体的是
Ⅱ.农药波尔多液的主要成分是CuSO4,下列两个反应都有CuSO4生成。
①Cu+2H2SO4=CuSO4+SO2+2H2O ②CuO+H2SO4=CuSO4+H2O
请回答下列问题:
(4)从分类角度来看CuSO4属于___________。
| A.氧化物 | B.盐 | C.碱 | D.酸 |
(5)上述两个反应属于氧化还原反应的是
(6)反应①的副产物SO2是大气污染物,可用NaOH溶液吸收,反应方程式是
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
9 . 乙烯的组成与结构
| 分子式 | 电子式 | 结构式 | 结构简式 | 分子模型 | |
| 球棍模型 | 填充模型 | ||||
|
| ||||
您最近一年使用:0次
名校
解题方法
10 . 按要求回答下列问题:
(Ⅰ)现有下列物质:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
(1)这些物质中:只含有共价键的是_______ (填序号,下同);只含有离子键的是_______ ;既含有极性共价键又含有离子键的是_______ ;属于离子化合物的是_______ 。
(2)①的结构式是_______ ;⑥的电子式是_______ 。
(3)用电子式表示③的形成:_______ 。
(Ⅱ)为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(4)请补全汞的原子结构示意图_______ 。 、
、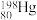 、
、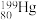 、
、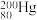 、
、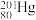 、
、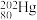 和
和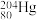 ,其中,
,其中,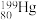 和
和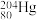 的中子数之比为
的中子数之比为_______ 。
(6)氮、磷、砷都是第VA族元素,下列说法正确的是_______ (填字母)。
a.非金属性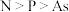 ,所以氮气最活泼
,所以氮气最活泼
b. 与
与 性质相似,
性质相似, 能与
能与 溶液反应
溶液反应
c.As的最高价氧化物对应的水化物是强酸
d.形成的简单氢化物的还原性随着原子序数递增而增强
(Ⅰ)现有下列物质:①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
(1)这些物质中:只含有共价键的是
(2)①的结构式是
(3)用电子式表示③的形成:
(Ⅱ)为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(4)请补全汞的原子结构示意图
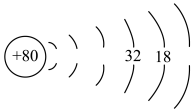
 、
、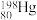 、
、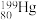 、
、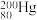 、
、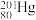 、
、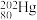 和
和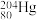 ,其中,
,其中,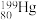 和
和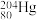 的中子数之比为
的中子数之比为(6)氮、磷、砷都是第VA族元素,下列说法正确的是
a.非金属性
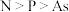 ,所以氮气最活泼
,所以氮气最活泼b.
 与
与 性质相似,
性质相似, 能与
能与 溶液反应
溶液反应c.As的最高价氧化物对应的水化物是强酸
d.形成的简单氢化物的还原性随着原子序数递增而增强
您最近一年使用:0次