名校
1 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.50℃, 的 的 溶液中含有 溶液中含有 的数目为 的数目为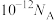 |
B. 的 的 溶液中含 溶液中含 分子的数目为 分子的数目为 |
C. 和 和 于密闭容器中充分反应后,分子总数为 于密闭容器中充分反应后,分子总数为 |
D.浓度均为 的 的 溶液和 溶液和 溶液中, 溶液中, 数目均为 数目均为 |
您最近一年使用:0次
2023-04-28更新
|
764次组卷
|
4卷引用:海南省琼海市2023届高三联考二模化学试题
解题方法
2 . 硫酸锰可为动植物提供微量元素,还可用作工业催化剂等。用 还原
还原 可制备硫酸锰,装置如图所示(夹持装置已省略)。
可制备硫酸锰,装置如图所示(夹持装置已省略)。
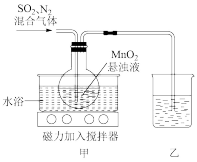
回答下列问题:
(1)实验室中常用70%的浓硫酸和 制备
制备 ,若该制备实验中需70%的浓硫酸49g,则需98%的浓硫酸(浓度为
,若该制备实验中需70%的浓硫酸49g,则需98%的浓硫酸(浓度为 )
)_______ mL(保留一位小数)来配制。这种方法制备 的化学方程式为
的化学方程式为_______ 。
(2)实验中通入 的作用是
的作用是_______ 。
(3)装置甲为制备 的装置,采用水浴加热,而不是采用酒精灯明火加热。相比酒精灯加热,水浴加热的主要优点是
的装置,采用水浴加热,而不是采用酒精灯明火加热。相比酒精灯加热,水浴加热的主要优点是_______ 。
(4)装置甲中 还原
还原 的离子方程式是
的离子方程式是_______ 。
(5)装置乙的作用是防止 逸出对实验者造成毒害,则该装置中的试剂是
逸出对实验者造成毒害,则该装置中的试剂是_______ 。
(6)若检测到制备后的溶液中 ,原因可能是
,原因可能是_______ 。
 还原
还原 可制备硫酸锰,装置如图所示(夹持装置已省略)。
可制备硫酸锰,装置如图所示(夹持装置已省略)。
回答下列问题:
(1)实验室中常用70%的浓硫酸和
 制备
制备 ,若该制备实验中需70%的浓硫酸49g,则需98%的浓硫酸(浓度为
,若该制备实验中需70%的浓硫酸49g,则需98%的浓硫酸(浓度为 )
) 的化学方程式为
的化学方程式为(2)实验中通入
 的作用是
的作用是(3)装置甲为制备
 的装置,采用水浴加热,而不是采用酒精灯明火加热。相比酒精灯加热,水浴加热的主要优点是
的装置,采用水浴加热,而不是采用酒精灯明火加热。相比酒精灯加热,水浴加热的主要优点是(4)装置甲中
 还原
还原 的离子方程式是
的离子方程式是(5)装置乙的作用是防止
 逸出对实验者造成毒害,则该装置中的试剂是
逸出对实验者造成毒害,则该装置中的试剂是(6)若检测到制备后的溶液中
 ,原因可能是
,原因可能是
您最近一年使用:0次
2023-01-14更新
|
133次组卷
|
3卷引用:海南省屯昌县2023届高三二模统考(A)化学试题
3 . 设 NA 为阿伏加 德罗常数的数值。下列说法正确的是
| A.常温下,5.6g 铁粉投入足量的浓硝酸中,转移电子数为 0.3NA |
B.0.5mol 环氧乙烷( )中含有的共价键数目为 1.5NA )中含有的共价键数目为 1.5NA |
| C.2.4g 镁条在足量的N2与O2的混合气体中完全燃烧,转移电子数为 0.2NA |
| D.25℃时,Ksp(BaSO4)=1×10-10,则BaSO4饱和溶液中Ba2+数目为1×10-5NA |
您最近一年使用:0次
4 . 3.0gFe2O3和A12O3组成的混合物全部溶于200mLpH=0的硫酸,反应后向所得溶液中加入100mLNaOH溶液,恰好使Fe3+、A13+完全沉淀,则加入的NaOH的浓度c(NaOH)为
| A.1mol/L |
| B.2mol/L |
| C.4mol/L |
| D.8mol/L |
您最近一年使用:0次
2010·海南·一模
5 . (1)49gH2SO4的物质的量是______ ,将其配制成200mL溶液,所得溶液的物质的量浓度为______ ,其中含SO42-_____ 个,该溶液能与标准状况下的氨气_____ L恰好完全反应生成(NH4)2SO4。
(2)由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol/ L, c(SO42-)=0.8 mol/ L,则c(K+)为_____ 。
(3)将标准状况下a L HCl(g)溶于1000 g水中,得到盐酸的密度为bg/ cm3,则该盐酸的物质的量浓度是______ 。
(2)由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol/ L, c(SO42-)=0.8 mol/ L,则c(K+)为
(3)将标准状况下a L HCl(g)溶于1000 g水中,得到盐酸的密度为bg/ cm3,则该盐酸的物质的量浓度是
您最近一年使用:0次
6 . 下列说法正确的是
| A.O2和O3互为同位素,化学性质相似 |
| B.水是一种非常稳定的化合物,这是由于氢键所致 |
| C.分子晶体中一定存在分子间作用力,但可能没有共价键 |
| D.将标准状况下22.4 L 氨气溶于1 L水配成溶液,可得1 mol·L-1的氨水 |
您最近一年使用:0次
2016-06-27更新
|
127次组卷
|
2卷引用:2016届海南省华侨中学高三考前模拟理综化学试卷



