名校
1 . 氯元素的化合价与部分物质类别的对应关系如图所示,据图判断下列说法错误的是
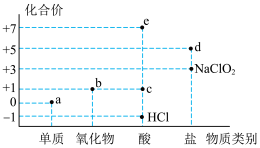
| A.c在光照条件下很容易分解 |
| B.b不是酸性氧化物,因为它没有对应的含氧酸 |
| C.图中a、b、c、d、e五种物质中均含有共价键,且c、d、e属于电解质 |
D.将a通入 溶液中,已知生成 溶液中,已知生成 、 、 和d的混合物,若 和d的混合物,若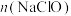 与 与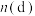 之比为 之比为 ,则氧化剂与还原剂的物质的量之比为 ,则氧化剂与还原剂的物质的量之比为 |
您最近一年使用:0次
2023-11-21更新
|
387次组卷
|
5卷引用:河北省沧衡八校联盟2023-2024学年高三上学期11月期中考试化学试题
名校
解题方法
2 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。
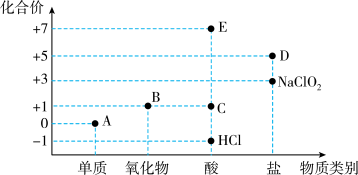
回答下列问题:
(1)已知D可用于实验室制O2,其焰色试验为紫色,D中含有的化学键有_______ ;A、B、C、D四种物质中,属于电解质的是_______ (填化学式)。
(2)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为_______ 。
(3)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为_______ 。
(4)已知A与氢氧化钠溶液反应生成NaCl、NaClO和NaClO3的混合物,若n(NaClO)与n(NaClO3)之比为3∶1,则氧化剂与还原剂的物质的量之比为______ 。
(5)NaClO2、二氧化氯(ClO2)均为高效无毒的消毒剂。
①NaClO2的消毒效率是A的_______ 倍(还原产物都是Cl-,消毒效率以单位物质的量的物质得到的电子数表示)。
②ClO2在杀菌消毒过程中会产生亚氯酸盐( ),需将其转化为Cl-除去,下列试剂可将
),需将其转化为Cl-除去,下列试剂可将 转化为Cl-的是
转化为Cl-的是_________ (填标号)。
A.FeSO4 B.O3 C.KMnO4 D.Na2SO3

回答下列问题:
(1)已知D可用于实验室制O2,其焰色试验为紫色,D中含有的化学键有
(2)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为
(3)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为
(4)已知A与氢氧化钠溶液反应生成NaCl、NaClO和NaClO3的混合物,若n(NaClO)与n(NaClO3)之比为3∶1,则氧化剂与还原剂的物质的量之比为
(5)NaClO2、二氧化氯(ClO2)均为高效无毒的消毒剂。
①NaClO2的消毒效率是A的
②ClO2在杀菌消毒过程中会产生亚氯酸盐(
 ),需将其转化为Cl-除去,下列试剂可将
),需将其转化为Cl-除去,下列试剂可将 转化为Cl-的是
转化为Cl-的是A.FeSO4 B.O3 C.KMnO4 D.Na2SO3
您最近一年使用:0次
2023-06-08更新
|
233次组卷
|
5卷引用:河北省承德市围场满族蒙古族自治县卉原中学2022-2023学年高一上学期期末网考化学试题
名校
解题方法
3 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______ (填化学式)。
(2)将X与Y混合,可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(3)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是_______ (填字母)。
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(4)已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则24 mL 0.05 mol·L-1的Na2SO3溶液与20 mL 0.02 mol·L-1的K2Cr2O7溶液恰好反应时,还原产物中Cr元素的化合价为_______ 。
(5)为了探究Cl2、SO2同时通入H2O中发生的反应,某化学兴趣小组同学设计了如图所示的实验装置。

该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的硫酸为原料制取SO2,采用MnO2和浓盐酸(12 mol·L-1)为原料制取Cl2.在此实验中,仪器F的作用是_______ ;发生装置B应选择如图三种装置中的_______ (填序号)。


(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(2)将X与Y混合,可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为
(3)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(4)已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则24 mL 0.05 mol·L-1的Na2SO3溶液与20 mL 0.02 mol·L-1的K2Cr2O7溶液恰好反应时,还原产物中Cr元素的化合价为
(5)为了探究Cl2、SO2同时通入H2O中发生的反应,某化学兴趣小组同学设计了如图所示的实验装置。

该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的硫酸为原料制取SO2,采用MnO2和浓盐酸(12 mol·L-1)为原料制取Cl2.在此实验中,仪器F的作用是

您最近一年使用:0次
2022-05-13更新
|
248次组卷
|
2卷引用:河北省衡水市深州中学2022-2023学年高三上学期第一次月考化学试题
名校
解题方法
4 .  具有很好的导电性,在光学、电学等行业有着重要的用途,其分子结构如图所示。将干燥的氨气通入
具有很好的导电性,在光学、电学等行业有着重要的用途,其分子结构如图所示。将干燥的氨气通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: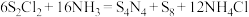 [已知
[已知 (分子结构为
(分子结构为 是硫单质中最稳定的]。下列说法错误的是
是硫单质中最稳定的]。下列说法错误的是

A. 属于分子晶体, 属于分子晶体,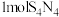 中含有 中含有 极性键 极性键 |
B. 中含有 中含有 非极性键 非极性键 |
C.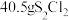 参与上述制备反应,转移 参与上述制备反应,转移 电子 电子 |
D. 的VSEPR模型均为四面体形 的VSEPR模型均为四面体形 |
您最近一年使用:0次
2024-03-03更新
|
383次组卷
|
2卷引用:河北省衡水董子高级中学等校2023-2024学年高三下学期2月 入校考试 化学试题
名校
5 . 以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产Al2O3并获得Fe3O4的部分工艺流程如图所示。请回答下列问题:

(1)“焙烧”时,为使原料快速、充分反应,可采取的措施有______ (答出2条)。此工序中,FeS2被空气中的O2氧化,反应的化学方程式为______ 。加入少量CaO的目的是______ 。
(2)“碱浸”时,溶于NaOH溶液的物质是______ (填化学式)。
(3)若在实验室进行过滤操作,使用的玻璃仪器有______ 。
(4)向“滤液”中通入过量CO2时生成沉淀,该反应的离子方程式为______ 。沉淀经处理可获得Al2O3,Al2O3的用途有______ (答出1条)。
(5)“隔绝空气焙烧”时,理论上反应消耗的n(FeS2):n(Fe2O3)=______ 。

(1)“焙烧”时,为使原料快速、充分反应,可采取的措施有
(2)“碱浸”时,溶于NaOH溶液的物质是
(3)若在实验室进行过滤操作,使用的玻璃仪器有
(4)向“滤液”中通入过量CO2时生成沉淀,该反应的离子方程式为
(5)“隔绝空气焙烧”时,理论上反应消耗的n(FeS2):n(Fe2O3)=
您最近一年使用:0次
2023-11-24更新
|
305次组卷
|
2卷引用:河北省定州市2023-2024学年高二上学期11月期中考试化学试题
名校
6 . 从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,以下是氯元素的“价类二维图”的部分信息。
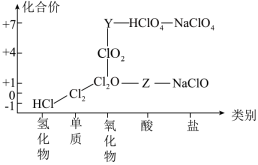
请回答下列问题:
(1)根据图中信息写出Y、Z的化学式__________ 、_________ 。
(2)已知高氯酸(HClO4)是强酸,写出高氯酸与铁反应的离子方程式____________________ .
(3)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式____________ ,该反应中盐酸表现__________ (填字母)。
A.酸性 B.氧化性 C.还原性 D.挥发性
(4)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为2HCl+NaClO=NaCl+Cl2↑+H2O,下列有关该反应说法不正确的是________。
(5)某游泳池常用NaClO来抑制藻类生长,工作人员一次错用H2O2消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了O2和NaCl,写出相应的化学方程式____________________ 。

请回答下列问题:
(1)根据图中信息写出Y、Z的化学式
(2)已知高氯酸(HClO4)是强酸,写出高氯酸与铁反应的离子方程式
(3)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式
A.酸性 B.氧化性 C.还原性 D.挥发性
(4)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为2HCl+NaClO=NaCl+Cl2↑+H2O,下列有关该反应说法不正确的是________。
| A.n(氧化剂):n(还原剂)=1:1 | B.n(氧化剂):n(还原剂)=1:2 |
| C.氧化性:NaClO>Cl2 | D.Cl2既是氧化产物又是还原产物 |
(5)某游泳池常用NaClO来抑制藻类生长,工作人员一次错用H2O2消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了O2和NaCl,写出相应的化学方程式
您最近一年使用:0次
7 . 阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 。
(2)制备 需要在
需要在_______ (填“酸性”“碱性”或“中性”)环境中进行。
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是_______ (填字母)。
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
(4)将 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整:_______ 。
 (胶体)
(胶体)
该反应消耗1个 时,转移的电子数为
时,转移的电子数为_______ 个。
(5)消毒净化 水,至少需要
水,至少需要 的质量为
的质量为_______  。
。 用于饮用水消毒净化的原理是
用于饮用水消毒净化的原理是_______ 。
| 高铁酸钾使用说明书 【化学式】  【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着  减小,稳定性下降,与水反应放出氧气。 减小,稳定性下降,与水反应放出氧气。 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 与水反应还能产生具有强吸附性的 与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用 胶体,可除去水中细微的悬浮物,有净水作用【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化  水投放 水投放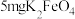 即可达到卫生标准 即可达到卫生标准 |
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在(3)下列关于
 的说法中,不正确的是
的说法中,不正确的是a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
(4)将
 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整: (胶体)
(胶体)
该反应消耗1个
 时,转移的电子数为
时,转移的电子数为(5)消毒净化
 水,至少需要
水,至少需要 的质量为
的质量为 。
。 用于饮用水消毒净化的原理是
用于饮用水消毒净化的原理是
您最近一年使用:0次
解题方法
8 . 高锰酸钾广泛用作氧化剂、消毒剂除臭剂及水处理剂,回答下列问题。
已知:20℃时各物质在水中的溶解度如表所示。
(1)常温下,高锰酸钾与浓盐酸混合发生反应生成氯气的离子方程式为___________ ,当转移2 mol电子时,生成___________ L(换算成标准状况下)氯气。
(2)高锰酸钾的一种制备方法:氢氧化钾(过量)与软锰矿粉(主要成分为MnO2)混合,在240℃下,吸收空气中的氧气,缓慢地转化为锰酸钾(K2MnO4),用水浸取后,过滤,电解滤液得到高锰酸钾粗品。
①该方法中生成锰酸钾的化学方程式为___________ ,该反应的氧化产物为___________ ,反应过程中涉及的物质属于氧化物的为___________ 。
②用惰性电极电解锰酸钾和氢氧化钾的混合溶液,阳极的电极反应式为___________ ,阴极生成一种气体,写出该气体的一种用途:___________ 。
③往锰酸钾溶液中通入足量的CO2,也能生成高锰酸钾和二氧化锰,与电解法相比,该方法的不足之处为___________ 。
已知:20℃时各物质在水中的溶解度如表所示。
| 物质 | KMnO4 | K2MnO4 | KOH | KHCO3 |
| 溶解度/g | 6.4 | 56.7 | 112 | 33.7 |
(2)高锰酸钾的一种制备方法:氢氧化钾(过量)与软锰矿粉(主要成分为MnO2)混合,在240℃下,吸收空气中的氧气,缓慢地转化为锰酸钾(K2MnO4),用水浸取后,过滤,电解滤液得到高锰酸钾粗品。
①该方法中生成锰酸钾的化学方程式为
②用惰性电极电解锰酸钾和氢氧化钾的混合溶液,阳极的电极反应式为
③往锰酸钾溶液中通入足量的CO2,也能生成高锰酸钾和二氧化锰,与电解法相比,该方法的不足之处为
您最近一年使用:0次
2023-07-06更新
|
62次组卷
|
2卷引用:河北省保定市部分示范高中2022-2023学年高二下学期期末调研考试化学试题
9 . 单一盐R仅由Fe、N、O三种元素组成,某化学兴趣小组称取4.84 g盐R进行相关实验,数据和现象如下:
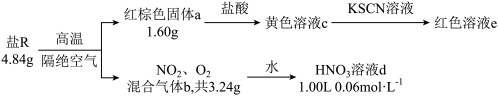
已知:①红棕色固体a为纯净物;
②混合气体b通入足量的水中,完全反应后,仅得到一种生成物;
③不考虑反应过程中的质量损失;
④ 遇KSCN溶液显血红色。
遇KSCN溶液显血红色。
回答下列问题:
(1)红棕色固体a为___________ (填化学式),其在生活中的用途有___________ (填一种即可)。
(2)盐R中Fe元素的化合价为___________ 价。
(3)写出盐R在上述条件下发生反应的化学方程式:___________ ,该反应中氧化产物与还原产物的总物质的量之比为___________ 。
(4)写出上述混合气体b通入水中发生反应的离子方程式:___________ 。
(5)研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铜加入上述所得的稀释后的溶液d中(假设溶液d很稀),恰好完全反应,无气体放出,则消耗铜的质量为___________ g。

已知:①红棕色固体a为纯净物;
②混合气体b通入足量的水中,完全反应后,仅得到一种生成物;
③不考虑反应过程中的质量损失;
④
 遇KSCN溶液显血红色。
遇KSCN溶液显血红色。回答下列问题:
(1)红棕色固体a为
(2)盐R中Fe元素的化合价为
(3)写出盐R在上述条件下发生反应的化学方程式:
(4)写出上述混合气体b通入水中发生反应的离子方程式:
(5)研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铜加入上述所得的稀释后的溶液d中(假设溶液d很稀),恰好完全反应,无气体放出,则消耗铜的质量为
您最近一年使用:0次
2023-04-18更新
|
252次组卷
|
6卷引用:河北省2022-2023学年高一下学期期中考试化学试题
10 . 高钴酸钠 是一种用途广泛的化合物,实验室可通过电解
是一种用途广泛的化合物,实验室可通过电解 与
与 的混合溶液获得
的混合溶液获得 ,并通过一系列反应来制备
,并通过一系列反应来制备 ,相关化学方程式如下:
,相关化学方程式如下: ;
; (未配平);
(未配平); (未配平)。下列说法错误的是
(未配平)。下列说法错误的是
 是一种用途广泛的化合物,实验室可通过电解
是一种用途广泛的化合物,实验室可通过电解 与
与 的混合溶液获得
的混合溶液获得 ,并通过一系列反应来制备
,并通过一系列反应来制备 ,相关化学方程式如下:
,相关化学方程式如下: ;
; (未配平);
(未配平); (未配平)。下列说法错误的是
(未配平)。下列说法错误的是| A.钴元素位于元素周期表的d区 |
| B.电解时阳极得到的气体可用向上排空气法收集 |
C.电解 制备 制备 的过程中添加的 的过程中添加的 可换成 可换成 |
D. 转化为 转化为 的化学方程式中 的化学方程式中 和 和 计量比为4∶7 计量比为4∶7 |
您最近一年使用:0次



