名校
解题方法
1 . 硝酸盐污染已成为一个日益严重的环境问题,甲酸(HCOOH)在纳米级Pd表面分解为活性H2和CO2,再经下列历程实现NO 的催化还原,进而减少污染。已知Fe(II)、Fe(III)表示Fe3O4中二价铁和三价铁。下列说法正确的是
的催化还原,进而减少污染。已知Fe(II)、Fe(III)表示Fe3O4中二价铁和三价铁。下列说法正确的是
 的催化还原,进而减少污染。已知Fe(II)、Fe(III)表示Fe3O4中二价铁和三价铁。下列说法正确的是
的催化还原,进而减少污染。已知Fe(II)、Fe(III)表示Fe3O4中二价铁和三价铁。下列说法正确的是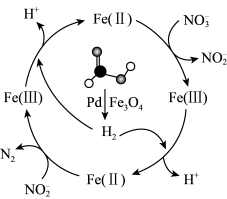
| A.Fe3O4没有参与该循环历程 |
| B.HCOOH分解时,碳氢键和氧氢键发生了断裂 |
C.NO 是NO 是NO 催化还原过程的催化剂 催化还原过程的催化剂 |
D.在整个历程中,每1molH2可还原1 mol NO |
您最近一年使用:0次
2022-02-02更新
|
1742次组卷
|
12卷引用:吉林省长春市第二实验中学2023-2024学年高二上学期10月月考化学试题
吉林省长春市第二实验中学2023-2024学年高二上学期10月月考化学试题福建省泉州市泉港一中、厦门外国语石狮分校2021-2022学年高二下学期期中联考化学试题广东梅州五华县中英文实验学校2023-2024学年高二下学期3月考试化学试题安徽省蚌埠市2021-2022学年高三上学期第二次教学质量检查理综化学试题(已下线)专题04氧化还原反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题07化学反应中的能量变化及反应机理-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题04氧化还原反应-2022年高考真题+模拟题汇编(全国卷)(已下线)专题04氧化还原反应-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题07化学反应中的能量变化及反应机理-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题07化学反应中的能量变化及反应机理-2022年高考真题+模拟题汇编(全国卷)安徽师范大学附属中学2021-2022学年高三下学期第十次综合测试理综化学试题福建省福州高新区第一中学(闽侯县第三中学)2023-2024学年高三上学期12月月考化学试题
名校
2 . 设NA为阿伏加德罗常数的值,下列有关叙述正确的是
| A.1L0.1mol·L-1Na2SO3溶液中阴离子数目为0.1NA |
| B.1.6gCH4含有共价键的数目为0.4NA |
| C.64gCu分别与足量稀硝酸反应时,转移电子数为NA |
| D.2molSO3充入密闭容器中分解所得产物分子的数目为3NA |
您最近一年使用:0次
2021-12-13更新
|
79次组卷
|
2卷引用:吉林省长春外国语学校2021-2022学年高二上学期第二次月考化学试题
3 . 钢铁“发蓝”是将钢铁制品浸到某些氧化性的溶液中,在钢铁的表面形成一层四氧化三铁的技术过程。其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热到130℃反应。其过程可以用如下化学方程式表示。下列说法不正确的是
①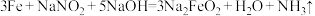
②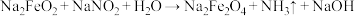 (未配平)
(未配平)
③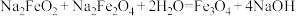
①
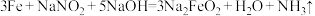
②
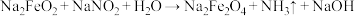 (未配平)
(未配平)③
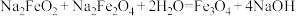
| A.碱性条件下,NaNO2的氧化性比Na2FeO2、Na2Fe2O4都强 |
| B.反应①、②、③均是氧化还原反应 |
| C.反应②配平后,H2O的化学计量数是5 |
| D.整个反应过程中每有16.8gFe参加反应转移0.8mol电子 |
您最近一年使用:0次
2021-12-10更新
|
345次组卷
|
6卷引用:吉林省吉化第一高级中学校2021-2022学年高二下学期复课检测化学试题
吉林省吉化第一高级中学校2021-2022学年高二下学期复课检测化学试题山西省太原市第五中学2021-2022学年高一上学期12月月考化学试题黑龙江省双鸭山市第一中学2021-2022学年高一上学期期末考试化学试题(已下线)第03练 氧化还原反应-2022年【寒假分层作业】高一化学(人教版2019)(已下线)1.3.3 氧化还原反应方程式配平(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)江西省南昌市第八中学2022-2023学年高三上学期10月月考化学试题
名校
4 . I.氯化铁可用于金属蚀刻,污水处理。
(1)25℃时,FeCl3溶液显酸性,原因是(用离子方程式表示)___________ 。把FeCl3溶液蒸干灼烧得到的主要产物是___________ 。
(2)为了探究外界条件对氯化铁水解平衡的影响,某研究性学习小组设计实验方案,获得如下数据:
下列说法正确的是___________ (填序号)。
A.上述实验能判断出温度对氯化铁水解的影响。
B.表格中x>y>z
C.上述实验能得出:增大盐的浓度,水解平衡正向移动,水解程度越大。
II、滴定实验是化学学科中最重要的定量实验之一、葡萄酒中抗氧化剂残留量的测定,常采用氧化还原滴定法。葡萄酒常用Na2S2O5作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

往实验中加入盐酸的目的是将Na2S2O5转化成SO2;滴定过程中发生的反应是:

(3)滴定时,I2溶液应装在___________ (“酸”或“碱”)式滴定管中,该滴定过程的指示剂是___________ ,滴定终点的现象为___________ 。
(4)实验消耗标准I2溶液50.00ml,所测样品中抗氧化剂的残留量(以游离SO2计算)为___________  。
。
(5)下列情形会造成测定结果偏低的是___________(填序号)。
(1)25℃时,FeCl3溶液显酸性,原因是(用离子方程式表示)
(2)为了探究外界条件对氯化铁水解平衡的影响,某研究性学习小组设计实验方案,获得如下数据:
| 实验 | c(FeCl3)/ | V(FeCl3)/mL | 温度/℃ | pH |
| 1 | 0.1 | 5 | 25 | x |
| 2 | 0.1 | 5 | 35 | y |
| 3 | 0.2 | 5 | 25 | z |
下列说法正确的是
A.上述实验能判断出温度对氯化铁水解的影响。
B.表格中x>y>z
C.上述实验能得出:增大盐的浓度,水解平衡正向移动,水解程度越大。
II、滴定实验是化学学科中最重要的定量实验之一、葡萄酒中抗氧化剂残留量的测定,常采用氧化还原滴定法。葡萄酒常用Na2S2O5作抗氧化剂,测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

往实验中加入盐酸的目的是将Na2S2O5转化成SO2;滴定过程中发生的反应是:

(3)滴定时,I2溶液应装在
(4)实验消耗标准I2溶液50.00ml,所测样品中抗氧化剂的残留量(以游离SO2计算)为
 。
。(5)下列情形会造成测定结果偏低的是___________(填序号)。
| A.滴定持续时间稍长,溶液中部分HI被空气氧化 |
| B.盛装标准I2溶液的滴定管用蒸馏水洗净后,未润洗 |
| C.滴定前俯视,滴定后平视 |
| D.滴定前滴定管尖嘴无气泡滴定后有气泡 |
您最近一年使用:0次
名校
解题方法
5 . 将一定量的氯气通入100mL8mol/L热的NaOH浓溶液中,恰好完全反应,溶液中形成NaCl、NaClO和NaClO3的共存体系。下列判断正确的是
| A.与NaOH反应的氯气一定为0.4mol |
| B.反应后的溶液中,n(Na+):n(Cl-)可能为9∶4 |
| C.该反应只有3种产物,其中还原产物为NaCl |
| D.n(NaCl) ∶n(NaClO) ∶n(NaClO3)可能为5∶1∶1 |
您最近一年使用:0次
2021-12-10更新
|
195次组卷
|
3卷引用:吉林省吉化第一高级中学校2021-2022学年高二下学期复课检测化学试题
名校
解题方法
6 . 电视剧中的仙境美轮美奂,其中所需的烟雾是在放于温热石棉网上的NH4NO3和Zn粉的混合物中滴几滴水后产生的白烟:NH4NO3+Zn=ZnO+N2↑+2H2O,下列说法中正确的是
| A.每生成1mol ZnO共转移2mol电子 |
| B.NH4NO3只是氧化剂 |
| C.氧化产物和还原产物的物质的量之比为1:1 |
| D.每产生标准状况下448mLN2共转移0.1mol电子 |
您最近一年使用:0次
2021-12-10更新
|
287次组卷
|
6卷引用:吉林省吉化第一高级中学校2021-2022学年高二下学期复课检测化学试题
7 . 从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,右图为氯元素的“价类二维图”的部分信息。请回答下列问题:
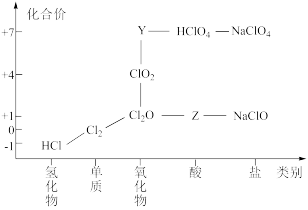
(1)根据图中信息写出Y、Z的化学式___________ 、___________ 。
(2)漂白液的有效成分是___________ ,其使用说明中特别提醒不可与洁厕灵(主要成分盐酸)混合使用,否则会产生Cl2,请用离子方程式表示其原因___________ 。
(3)现以氢氧化钠为原料制备漂白液,需配制100mL 8mol/L NaOH溶液。
①配制NaOH溶液时,需要称取NaOH固体的质量为___________ g;
②下面操作造成所配NaOH溶液浓度偏高的是___________ 。
A.暴露在空气中称量NaOH的时间太长
B.溶解后未冷却至室温就转移至容量瓶
C.若移液前容量瓶内有少量水
D.定容时俯视刻度线
(4)二氧化氯是一种高效消毒剂。工业制备ClO2的反应为:
___NaClO3+___HCl—___ClO2↑+___Cl2↑+___H2O+___NaCl
①配平上述化学方程式并用单线桥 表示反应过程中的电子转移情况。___________
②该反应的氧化剂与还原剂的物质的量之比为___________ ;若反应过程中消耗0.1molNaClO3,转移电子的数目为___________ 。
③ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去,下列试剂中可将ClO
),需将其转化为Cl-除去,下列试剂中可将ClO 转化为Cl-的是
转化为Cl-的是___________ (填字母)。
A.O3 B.FeSO4 C.KI D.KMnO4

(1)根据图中信息写出Y、Z的化学式
(2)漂白液的有效成分是
(3)现以氢氧化钠为原料制备漂白液,需配制100mL 8mol/L NaOH溶液。
①配制NaOH溶液时,需要称取NaOH固体的质量为
②下面操作造成所配NaOH溶液浓度偏高的是
A.暴露在空气中称量NaOH的时间太长
B.溶解后未冷却至室温就转移至容量瓶
C.若移液前容量瓶内有少量水
D.定容时俯视刻度线
(4)二氧化氯是一种高效消毒剂。工业制备ClO2的反应为:
___NaClO3+___HCl—___ClO2↑+___Cl2↑+___H2O+___NaCl
①配平上述化学方程式并用
②该反应的氧化剂与还原剂的物质的量之比为
③ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO
 ),需将其转化为Cl-除去,下列试剂中可将ClO
),需将其转化为Cl-除去,下列试剂中可将ClO 转化为Cl-的是
转化为Cl-的是A.O3 B.FeSO4 C.KI D.KMnO4
您最近一年使用:0次
2021-12-08更新
|
305次组卷
|
2卷引用:吉林省吉化第一高级中学校2021-2022学年高二下学期复课检测化学试题
8 . 神舟十二号飞船的控制计算机、数据管理计算机完全使用国产CPU芯片,制作芯片刻蚀液为硝酸与氢氟酸的混合溶液,其工艺涉及的反应为: ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是| A.H2SiF6中Si元素的化合价为+6价 |
| B.该反应中,HNO3仅作氧化剂 |
| C.该反应中,生成标准状况下2.24LH2时,转移电子的物质的量为0.2mol |
| D.芯片刻蚀液可用硫酸代替 |
您最近一年使用:0次
2021-11-12更新
|
371次组卷
|
4卷引用:吉林省长春市博硕学校(原北师大长春附属学校)2021-2022学年高二下学期期末考试化学试题
吉林省长春市博硕学校(原北师大长春附属学校)2021-2022学年高二下学期期末考试化学试题天津市五校联考2021-2022学年高三上学期期中考试化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)
10-11高一上·江苏南通·期中
9 . 已知反应:①Cl2+2KBr=2KCl+Br2,②KClO3+6HCl=3Cl2↑+KCl+3H2O,③2KBrO3+Cl2=Br2+2KClO3,下列说法正确的是
| A.上述三个反应都有单质生成,所以都是置换反应 |
| B.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2 |
| C.反应②中氧化剂与还原剂的物质的量之比为1:6 |
| D.③中 1 mol 还原剂反应,则氧化剂得到电子的物质的量为 2 mol |
您最近一年使用:0次
2021-11-01更新
|
805次组卷
|
73卷引用:吉林白城市洮南市第一中学2020-2021学年高二下学期期末考试化学试题
吉林白城市洮南市第一中学2020-2021学年高二下学期期末考试化学试题(已下线)2011-2012学年浙江省嘉兴一中高二上学期期中考试化学试卷2016届吉林省长春外国语学校高三上学期二次质检化学试卷云南省富宁县民族中学2019-2020学年高二上学期开学考试化学试题云南省文山州马关县二中2019-2020学年高二上学期9月份考试化学试题吉林省松原市长岭县第三中学2020-2021学年高一上学期期末考试化学试题(已下线)2010年江苏省启东中学高一上学期期中考试化学卷(已下线)2011-2012学年浙江省杭州市高一上学期期中七校联考化学试卷(已下线)2011-2012学年江西省南昌二中高一上学期期中考试化学试卷(已下线)2012届江苏省苏州五中高三上学期期中考试化学试卷(已下线)2013-2014学年河北省遵化市高一上学期期中质量检测化学试卷(已下线)2013-2014学年江苏省泰州市姜堰区高一上学期期中考试化学试卷(已下线)2014-2015学年辽宁省沈阳二中高一上学期期中化学试卷2014-2015学年黑龙江省大庆市铁人中学高一期中化学试卷2014-2015学年江苏省南通中学高一上学期期中化学试卷2014-2015四川省攀枝花市高一上学期期末考试化学试卷2014-2015江西省新余市高一上学期期末考试化学试卷2015-2016学年浙江余姚中学高一上学期期中考试化学试卷2015-2016学年四川省雅安中学高一上期中测试化学试卷2016届福建省福安高级中学、霞浦七中、周宁十中高三上期中联考化学试卷2015-2016学年浙江省嘉兴一中高一上12月月考化学试卷2015-2016学年江西省吉安一中高一上第二次段考化学试卷22015-2016学年安徽省六安一中高一上学期期末化学试卷2015-2016学年广东省深圳市南山区高一上学期期末考试化学试卷2017届广东省仲元中学高三上9月月考化学试卷2017届辽宁省鞍山一中高三上学期第一次模拟化学试卷2016-2017学年浙江省绍兴一中高一上期中化学卷2016-2017学年北京市怀柔区高一上学期期末考试化学试卷黑龙江省大庆铁人中学2017-2018学年高一上学期12月月考化学试题黑龙江省大庆铁人中学2017-2018学年高一12月月考化学试题湖南省石门县第一中学2016-2017学年高一下学期期末考试化学试题新疆自治区北京大学附属中学新疆分校2019届高三上学期10月月考化学试题河北省正定县第三中学2018-2019学年高一上学期期中考试化学试题安徽省滁州市民办高中2018-2019学年高一上学期第三次月考化学试题新疆石河子市兵团八师一四三团第一中学2018-2019学年高一上学期期末考试化学试题云南省澜沧县民中2018-2019学年高一下学期期末考试化学试题云南省绥江县一中2018-2019学年高一下学期期末考试化学试题四川省棠湖中学2019-2020学年高一上学期期中考试化学试题云南省绥江县第三中学2019-2020学年高一上学期期末考试化学试题福建省福州市八县一中2019-2020学年高一年上学期期末联考化学试卷黑龙江省大庆市第四中学2019-2020学年高一上学期第三次月考化学试题湖南省衡东县欧阳遇实验中学2019-2020学年高一下学期选科摸底考试化学试题福建省厦门第一中学2019-2020学年高一上学期12月月考化学试题天津市和平区耀华中学2019-2020学年高一上学期第一次月考化学试题重庆市部分区2019-2020学年高一上学期期末考试化学试题鲁科版(2019)高一必修第一册第二章C 高考挑战区 过模拟 2年模拟精编精练(已下线)1.3.3 氧化还原反应的规律及应用-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)宁夏回族自治区青铜峡市高级中学2021届高三上学期第二次月考化学试题江苏省靖江高级中学2020-2021学年度高一上学期第一次阶段考试化学试题广西壮族自治区南宁市第三十六中学2019-2020学年高一上学期期中考试化学试题浙江省龙港市第二高级中学2020-2021学年高一上学期第一次月考化学试题(已下线)【浙江新东方】35(已下线)【浙江新东方】在线化学 (4).(已下线)【南昌新东方】3.2020 高一上 明德中学 期中 项金辉河南省周口市商水县中英文学校2020-2021学年高一上学期期中考试化学试题重庆市第三十七中学校2021届高三9月月考化学试题河北省石家庄市藁城区第一中学2019-2020学年高一上学期第二次月考化学试题黑龙江省实验中学2020-2021学年高一上学期期末考试化学试题广西北流市实验中学2020-2021学年高一上学期期中考试化学试题重庆市杨家坪中学2020-2021学年高一上学期1月月考化学试题河北省石家庄市第二中学2020-2021学年高一上学期期中模拟试题辽宁省大连市普兰店区第二中学2020-2021学年高一4月阶段性测试化学试题四川省绵阳三台县芦溪中学2020-2021学年高一下学期开学考试化学试题四川省眉山市仁寿第一中学南校区2021-2022学年高一(强基班)上学期入学考试化学试题天津市杨村第一中学等七校2020-2021学年高一上学期期中联考化学试题天津市和平区耀华中学2021-2022学年高一上学期9月月考化学试题江苏省南京市金陵中学2020-2021学年高一上化学12月月考化学试题重庆市杨家坪中学2021-2022学年高一上学期第二次月考化学试题重庆市沙坪坝实验中学校2021-2022学年高一上学期期末考试化学试题山西省晋中市平遥二中2021-2022学年上学期期中考试高一化学试题河南省周口市项城市第三高级中学2022-2023学年高一下学期开学考试化学试题湖南省株洲市炎陵县湘山高级中学等2校2022-2023学年高一下学期开学考试化学试题浙江省余姚中学2023-2024学年高一上学期期中考试化学试题
10 . 在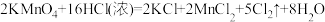 反应中氧化剂与还原剂个数之比为
反应中氧化剂与还原剂个数之比为
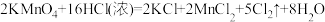 反应中氧化剂与还原剂个数之比为
反应中氧化剂与还原剂个数之比为| A.1∶8 | B.8∶1 | C.1∶5 | D.5∶l |
您最近一年使用:0次
2021-10-24更新
|
802次组卷
|
17卷引用:吉林省扶余一中2016-2017学年高二下学期期末考试化学试题
吉林省扶余一中2016-2017学年高二下学期期末考试化学试题吉林省扶余市第一中学2016-2017学年高二下学期期末考试化学试题云南省通海县第一中学2019-2020学年高二上学期开学考试化学试题河南省林州市第一中学2017-2018学年高一(火箭班)10月调研化学试题江西省信丰中学2017-2018学年高一上学期第三次月考化学试题辽宁省阜新二高2017-2018学年高一上学期第二次月考化学试卷云南省麻栗坡民族中学2018-2019学年高一上学期9月份考试化学试题(已下线)【新东方】高中化学5037安徽省定远县育才学校2020-2021学年高一上学期第二次月考化学试题甘肃省玉门市油田第一中学2020-2021学年高一上学期期末考试化学试题宁夏石嘴山市第三中学2020-2021学年高一上学期期末考试化学试题浙江省杭州市富阳区实验中学2021-2022学年高一上学期10月月考化学试题天津市静海区四校2021-2022学年高一上学期12月阶段性检测化学试题云南省昭通市昭阳区2021-2022学年高一下学期期末考试化学试题山东省“学情空间”区域教研共同体2022-2023学年高一上学期10月联考(人教版)化学试题作业(六) 氧化剂和还原剂甘肃省部分学校2023-2024学年高一上学期10月期中考试化学试题



